
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的悬浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:

(1)A点→B点反应的离子方程式为_______________________。
(2)原混合物中AlCl3的物质的量为______,NaOH的物质的量为_____。
(3)C点加入的HCl溶液体积为_____________。
【答案】AlO2-+H++H2O=Al(OH)3↓ 0.02 mol 0.13 mol 130 mL
【解析】
①盐酸加入量在0—10 mL时,沉淀的质量没有改变,说明把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后氢氧化钠有剩余,溶液中溶质为NaAlO2和NaOH,1.16 g白色沉淀是氢氧化镁,盐酸加入量在0—10 mL时,发生反应是H++OH-=H2O,②加入盐酸10—30 mL过程中,发生反应为:AlO2-+H++H2O=Al(OH)3↓,B点沉淀为Mg(OH)2、Al(OH)3,B→C发生反应为Mg(OH)2+ 2H+=Mg2++2 H2O、Al(OH)3+ 3H+=Al3++3H2O;
(1)A点→B点沉淀质量增大,该过程为NaAlO2与盐酸反应生成氢氧化铝沉淀和氯化钠,反应的离子方程式为AlO2-+H++H2O=Al(OH)3↓。
(2)A点→B点的反应离子方程式AlO2-+H++H2O=Al(OH)3↓,A点→B点消耗盐酸的体积为20mL,n(HCl)= 1 mol·L-1×0.02L=0.02mol,所以n(AlO2-)=0.02mol,根据铝元素守恒,原混合物中AlCl3的物质的量为0.02mol;根据纵坐标可以知道氢氧化镁的物质的量是![]() 0.02mol,根据镁元素守恒,原混合物中MgCl2的物质的量为0.02mol;原混合物溶于水时,发生了反应:Al3++4OH-=AlO2-+2H2O和Mg2++2OH-=Mg(OH)2↓,AlCl3和MgCl2消耗的NaOH的物质的量为0.02×4+0.02×2=0.12mol;根据图像,盐酸加入量在0—10 mL时,发生反应H++OH-=H2O,所以原混合物溶于水发生反应后剩余的NaOH为0.01mol,所以原有NaOH的物质的量为0.12mol+0.01mol=0.13mol。
0.02mol,根据镁元素守恒,原混合物中MgCl2的物质的量为0.02mol;原混合物溶于水时,发生了反应:Al3++4OH-=AlO2-+2H2O和Mg2++2OH-=Mg(OH)2↓,AlCl3和MgCl2消耗的NaOH的物质的量为0.02×4+0.02×2=0.12mol;根据图像,盐酸加入量在0—10 mL时,发生反应H++OH-=H2O,所以原混合物溶于水发生反应后剩余的NaOH为0.01mol,所以原有NaOH的物质的量为0.12mol+0.01mol=0.13mol。
(3)B点沉淀为Mg(OH)2、Al(OH)3,根据(2)可知氢氧化铝和氢氧化镁的物质的量均为0.02mol,B→C发生反应为Mg(OH)2 + 2H+ = Mg2+ +2 H2O、Al(OH)3 + 3H+ = Al3+ + 3H2O;所以B→C消耗盐酸的物质的量是0.02mol×2+0.02mol×3=0.1mol,盐酸的体积是![]() 0.1L=100mL,C点加入的HCl溶液体积为100mL+30mL=130mL。
0.1L=100mL,C点加入的HCl溶液体积为100mL+30mL=130mL。


科目:高中化学 来源: 题型:
【题目】工业上用闪锌矿(主要成分为ZnS,还含有Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:

(1)滤渣A经CS2提取后可获得一种淡黄色副产品,其化学式为____。
(2)浸取过程中Fe2(SO4)3的作用是________ (氧化剂或还原剂)。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为_________。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是________。
(4)置换法除重金属离子所用物质C为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下:

(1)NiC2O4·2H2O中C的化合价是___。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为___。
(2)“滤渣Ⅰ”的主要成分是___。
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是___。
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
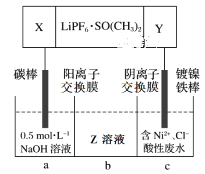
①电极X的反应材料是___(填化学式);中间隔室b可以得到的主要物质Z是___(填化学式)。
②电解总反应的离子方程式为___。
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni___g(写出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
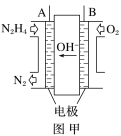
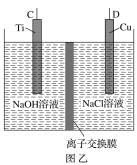
(1)上述装置中D电极应连接肼燃料电池的________极(填“A”或“B”),该电解池中离子交换膜为________离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为________________________________________,
肼燃料电池中A极发生的电极反应为____________________________。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
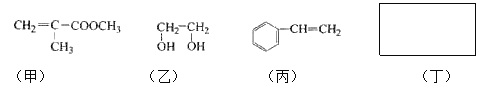
填写下列空白:
(1)甲中不含氧原子的官能团是____________;下列试剂能与甲反应而褪色的是___________(填标号)
a. Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:_______
(3)淀粉通过下列转化可以得到乙(其中A—D均为有机物):

A的分子式是___________,试剂X可以是___________。
(4)已知: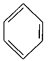 +RCl
+RCl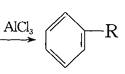 +HCl(-R为烃基)
+HCl(-R为烃基)
 +H2
+H2
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 ______________ 。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种正投入生产的大型蓄电系统,放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是( )
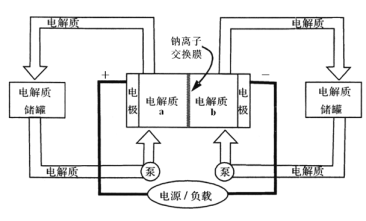
A. 放电时,负极反应为3NaBr-2e-=NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-=Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24 L H2时,b池生成17.40gNa2S4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,将浓度均为
时,将浓度均为![]() 、体积分别为
、体积分别为![]() 和
和![]() 的
的![]() 溶液与
溶液与![]() 溶液按不同体积比混合,保持
溶液按不同体积比混合,保持![]() ,
,![]() 、
、![]() 与混合液的
与混合液的![]() 的关系如图所示,下列说法不正确的是( )
的关系如图所示,下列说法不正确的是( )
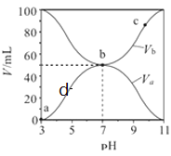
A.![]() 的数量级约为
的数量级约为![]()
B.b点时![]()
C.a、b、d几点中,水的电离程度![]()
D.![]() 点过程中,可能存在
点过程中,可能存在![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化钠是一种重要的基本化工原料,同时也是一种剧毒物质。一旦泄漏需要及时处理,一般可以通过喷洒双氧水或过硫酸钠(Na2S2O8)溶液来处理,以减轻环境污染。
I.已知:氯化钠是一种白色结晶颗粒,化学式为NaCN,有剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)请设计实验证明N、C元素的非金属性强弱:______________________。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的离子方程式是______________________。
Ⅱ.工业制备过硫酸钠的反应原理如下:
主反应:(NH4)2S2O8+2NaOH![]() Na2S2O8+2NH3↑十2H2O
Na2S2O8+2NH3↑十2H2O
副反应:2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
某化学兴趣小组利用上述原理在实验室制备过硫酸钠并检测用过硫酸钠溶液处理后的氰化钠废水是否达标排放。
(实验一)实验室通过如图所示装置制备Na2S2O8。
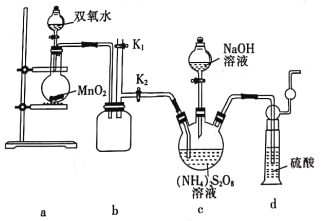
(3)装置b的作用是______________________。
(4)装置a中反应产生的气体需要持续通人装置c的原因是______________________。
(5)上述装置中还需补充的实验仪器或装置有___________(填字母)。
A温度计 B洗气瓶 C.水浴装置 D.酒精灯
(实验二)测定用过硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg·L-1。
②Ag++2CN-===[Ag(CN)2]-,Ag++I-===AgI↓,AgI呈黄色,且CN-优先与Ag+反应。实验如下:取100.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂用1.00×10-4mol·L-1的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
(6)滴定终点的现象是____________________________________________。
(7)处理后的废水中氰化钠的浓度为___________mg·L-1;处理后的废水是否达到排放标准?___________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 增大压强或升高温度,—定能使化学反应速率加快
B. 己知 Ni(CO)4(g)=Ni(s)+4CO(g) △H=QkJ/mol,则 Ni(s) +4CO(g)=Ni(CO)4(g) △H=-QkJ/mol
C. 500°C、30 MPa下, 0.5 mol N2(g)和1.5mol H2(g)反应生成NH3(g) 放热QkJ,其热化学方程式为N2(g)+3 H2(g)![]() 2 NH3(g) △H=-2QkJ/mol
2 NH3(g) △H=-2QkJ/mol
D. 己知两个平衡体系:2NiO(s)![]() 2Ni(s)+O2(g) 2CO(g)+O2(g)
2Ni(s)+O2(g) 2CO(g)+O2(g)![]() 2CO2(g)是平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g)
2CO2(g)是平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g)![]() Ni(s)+CO2(g)的平衡常数为
Ni(s)+CO2(g)的平衡常数为![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com