
【题目】下列有机物中碳原子一定在一个平面内的是:( )
A、2-丁烯 B、丁烷 C、苯乙烯 D、环己烷
 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】铝用途广泛,用铝土矿(主要成分为Al2O3·nH2O、少量SiO2和Fe2O3)制取Al有如下途径:

(1)滤液A可用于净水,其净水原理用离子方程式表示为_________________。
(2)灼烧时盛放药品的仪器名称是______________
(3)步骤Ⅴ中发生反应的化学方程式是________________________。
(4)步骤Ⅲ中生成固体C的离子反应方程式为__________________________。
(5)取滤液B 100 mL,加入1 mol/L盐酸200 mL,沉淀量达到最大且质量为11.7 g。则滤液B中c(Al O2-)=_____________。(4分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如下:
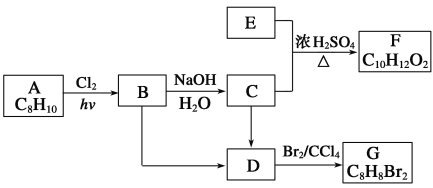
请回答下列问题:
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为 。
(2)A为一取代芳香烃,B中含有一个甲基。由B生成C的化学方程式为______________。
(3)由B生成D的反应条件是 ;由C生成D的反应类型是 。
(4)F存在于栀子香油中,其结构简式为________________________。
(5)在G的同分异构体中,苯环上一硝化的产物只有一种的共有 种,其中核磁共振氢谱有两组峰,且峰面积比为1∶1的是___________________(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】250℃和 1.01×105Pa时,2N2O5(g)= 4NO2(g)+ O2(g) △H=+56.76 kJ/mol 能自发进行,其自发进行的原因是
A.是吸热反应
B.是放热反应
C.是熵减少的反应
D.熵增效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚硫酸为二元中强酸,不稳定,易被氧化。请回答下列问题:
(1)下列有关亚硫酸的性质的判断正确的是______(填标号)。
a.具有酸性 b.具有氧化性 c.具有还原性 d.有刺激性气味
(2)亚硫酸在水中电离的方程式为______________________。
(3)将亚硫酸钠(Na2SO3)溶液滴人到几种不同溶液中的现象如下表所示:
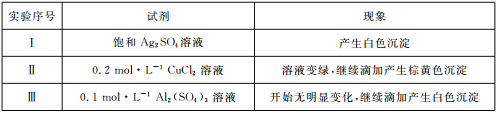
①经检验,实验I中的白色沉淀是Ag2SO3。用离子方程式解释:__________________。
②经检验,实验Ⅱ中的棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。推测反应后的溶液中一定含有溶质电离出的阴离子是______________,请选用合适的试剂分别验证这些离子:________________。
③已知:Al2(SO3)3在水溶液中不存在。经检验,实验Ⅲ中的白色沉淀中无SO2,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。推测沉淀中含有的阴离子为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生做乙酸乙酯的制备实验装置如图所示。

(1)写出该反应的方程式_____________________。
(2)若用18O标记乙醇中的氧元素,则18O出现在 中,(填“乙酸乙酯”或“水”)。
(3)饱和碳酸钠溶液的作用是: 。
(4)分离产物与碳酸钠溶液的方法是: 。
(5)在反应中,浓硫酸的作用 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇。在化学实验、电镀、食品添加剂、烧制青花瓷时可用于绘画等方面有广泛用途。已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:
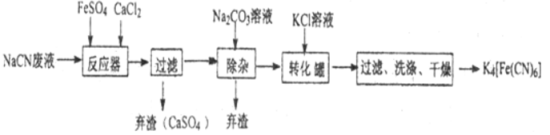
(1)常温下,NaCN水溶液的pH 7(填“>”、“<”、“ = ”),实验室用NaCN固体配制NaCN溶液时,应先将其溶于 溶液,再用蒸馏水稀释。
(2)反应器中发生的主要反应的化学方程式为 。
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、 。
(4)转化器中生成K4[Fe(CN)6]的反应类型是 ,相同温度下,溶解度:K4[Fe(CN)6] Na4[Fe(CN)6](填“>”“ = ”“<”),过滤后洗涤K4[Fe(CN)6]使用的试剂是 。
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为 。
(6)含有14.7kgNaCN的工业废水可生产出9.2kg的K4[Fe(CN)6],则K4[Fe(CN)6]的产率是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.Fe(NO3)2溶液中滴入一定量盐酸:3Fe2++4H++NO3-=2H2O+NO↑+3Fe3+
B.向氯化铵的溶液中加入足量浓NaOH溶液并加热:NH4++OH-![]() NH3·H2O
NH3·H2O
C.Ba(OH)2溶液与H2SO4溶液混合产生沉淀:Ba2++ SO42-=BaSO4↓
D.往NaOH溶液中通入过量SO2:SO2+2OH-=SO32- +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备
过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备

步骤①加入氨水的目的是________________。小火煮沸的作用是使沉淀颗粒长大,有利于__________________。
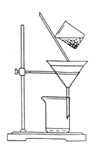
(2)如图是某学生的过滤操作示意图,其操作不规范的是_________(填标号)。
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备
![]()
(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈_______性(填“酸”、“碱”或“中”)。将溶液煮沸,趁热过滤。将溶液煮沸的作用是______________。
(4)步骤③中反应的化学方程式为____________________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是___________。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是______________,产品的缺点是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com