
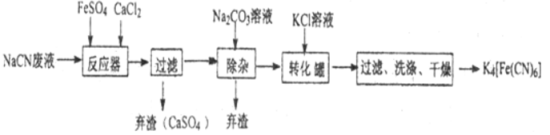
【题目】亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇。在化学实验、电镀、食品添加剂、烧制青花瓷时可用于绘画等方面有广泛用途。已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:
(1)常温下,NaCN水溶液的pH 7(填“>”、“<”、“ = ”),实验室用NaCN固体配制NaCN溶液时,应先将其溶于 溶液,再用蒸馏水稀释。
(2)反应器中发生的主要反应的化学方程式为 。
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、 。
(4)转化器中生成K4[Fe(CN)6]的反应类型是 ,相同温度下,溶解度:K4[Fe(CN)6] Na4[Fe(CN)6](填“>”“ = ”“<”),过滤后洗涤K4[Fe(CN)6]使用的试剂是 。
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为 。
(6)含有14.7kgNaCN的工业废水可生产出9.2kg的K4[Fe(CN)6],则K4[Fe(CN)6]的产率是 。
【答案】(1)>;浓NaOH;
(2)6NaCN+FeSO4+CaCl2=Na4[Fe(CN)6]+ CaSO4↓+2NaCl;
(3)玻璃棒;(4)复分解反应;<;乙醇;
(5)K++Fe3++ [Fe(CN)6]4-=KFe[Fe(CN)6]↓;(6)50% 。
【解析】
试题分析:(1)HCN为极弱的酸,NaCN为强碱弱酸盐,CN- + H2O![]() HCN + OH-,水溶液显碱性,则pH>7,配制NaCN溶液,为防止其发生水解,先溶解到浓NaOH溶液中,然后加水稀释;(2)根据流程图,6NaCN + FeSO4 + CaCl2 = CaSO4↓ + 2NaCl + Na4[Fe(CN)6];(3)过滤需要用到玻璃仪器有漏斗、玻璃棒、烧杯;(4)转化器中发生的反应是:Na4[Fe(CN)6] + KCl = K4[Fe(CN)6]↓ + NaCl,此反应属于复分解反应,得出K4[Fe(CN)6]溶解度小于Na4[Fe(CN)6],亚铁氰化钾可溶于水,不溶于乙醇,因此洗涤沉淀用乙醇;(5)根据信息,K++Fe3++ [Fe(CN)6]4-=KFe[Fe(CN)6]↓;(6)根据CN-守恒,n[K4(Fe(CN)6] = 14.7/(49 × 6)mol = 0.05mol,则m[K4(Fe(CN)6] = 0.05 × 368g = 18.4g,产率为9.2/18.4 × 1005 = 50%。
HCN + OH-,水溶液显碱性,则pH>7,配制NaCN溶液,为防止其发生水解,先溶解到浓NaOH溶液中,然后加水稀释;(2)根据流程图,6NaCN + FeSO4 + CaCl2 = CaSO4↓ + 2NaCl + Na4[Fe(CN)6];(3)过滤需要用到玻璃仪器有漏斗、玻璃棒、烧杯;(4)转化器中发生的反应是:Na4[Fe(CN)6] + KCl = K4[Fe(CN)6]↓ + NaCl,此反应属于复分解反应,得出K4[Fe(CN)6]溶解度小于Na4[Fe(CN)6],亚铁氰化钾可溶于水,不溶于乙醇,因此洗涤沉淀用乙醇;(5)根据信息,K++Fe3++ [Fe(CN)6]4-=KFe[Fe(CN)6]↓;(6)根据CN-守恒,n[K4(Fe(CN)6] = 14.7/(49 × 6)mol = 0.05mol,则m[K4(Fe(CN)6] = 0.05 × 368g = 18.4g,产率为9.2/18.4 × 1005 = 50%。


科目:高中化学 来源: 题型:
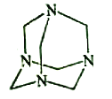
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( )
A.1:1 B.2:3 C.3:2 D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(如图所示)在大试管里加入3mL乙醇、2mL冰醋酸,再缓缓加入2mL浓硫酸,边加边振荡。在另一支试管中加入饱和碳酸钠溶液用来吸收反应生成物。
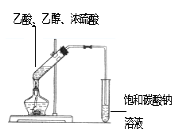
小心均匀加热大试管3-5min.请回答问题:
(1)在大试管中的反应化学方程式: ,
反应类型为_________________。
(2)用来吸收反应生成物的试管里要装饱和碳酸钠溶液的原因是: 。
(3)出气导管口不能插入碳酸钠液面的原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中A与B反应生成C,其反应速率分别用v (A)、v (B)、v (C)表示。已知v (A)、v (B)、v (C)之间有以下关系2 v (B) = 3 v (A)、3 v (C) = 2 v (B)。则此反应可表示为
A.2A + 3B = 2C B.A + 3B = 2C C.3A + B = 2C D.A + B = C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。A为 ,B为 ,C为 ,D的最高价氧化物的水化物是 。 (用化学式填空)
Ⅱ.一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示: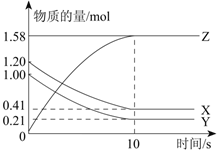
(1)反应开始到10 s,用Z表示的反应速率为 mol/(Ls)。
(2)反应开始到10 s,X的物质的量浓度减少了 mol/L。
(3)反应的化学方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6是一种优良的绝缘气体,分子结构中存在S-F键.已知1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F、S-F键需吸收的能量分别为160kJ、330kJ。则发生反应S(s)+3F2(g)═SF6(g),生成1molSF6时能量变化为( )
A、释放1220KJ B、吸收1780KJ C、 吸收1220KJ D、释放1780KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5mol某羧酸与足量乙醇发生酯化反应,生成酯的质量比原羧酸的质量增加了28g,则原羧酸可能是
A. 甲酸 B. 乙二酸 C. 丙酸 D. 丁酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
A.Na+、K+ 、OH—、Cl— B.Na+、Cu2+、SO42—、NO3—
C.K+、Mg2+、SO42—、Cl— D.Ba2+、HCO3—、NO3—、K+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com