
【题目】已知亚硫酸为二元中强酸,不稳定,易被氧化。请回答下列问题:
(1)下列有关亚硫酸的性质的判断正确的是______(填标号)。
a.具有酸性 b.具有氧化性 c.具有还原性 d.有刺激性气味
(2)亚硫酸在水中电离的方程式为______________________。
(3)将亚硫酸钠(Na2SO3)溶液滴人到几种不同溶液中的现象如下表所示:
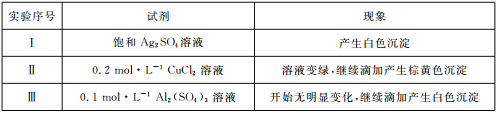
①经检验,实验I中的白色沉淀是Ag2SO3。用离子方程式解释:__________________。
②经检验,实验Ⅱ中的棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。推测反应后的溶液中一定含有溶质电离出的阴离子是______________,请选用合适的试剂分别验证这些离子:________________。
③已知:Al2(SO3)3在水溶液中不存在。经检验,实验Ⅲ中的白色沉淀中无SO2,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。推测沉淀中含有的阴离子为_______。
【答案】(1) abcd;(2) H2SO3![]() H++HSO3-、HSO3-
H++HSO3-、HSO3-![]() H++ SO32-;(3)①2Ag++SO32-=Ag2SO3↓; ②SO42-、Cl-,取少量滤液,用足量盐酸酸化后滴加氯化钡溶液,有白色沉淀生成,证明含SO42-;另取少量滤液,用足量硝酸酸化后滴加足量硝酸钡溶液,过滤,向所得滤液中滴加硝酸银溶液,有白色沉淀生成,证明含Cl-;③SO32-、OH-。
H++ SO32-;(3)①2Ag++SO32-=Ag2SO3↓; ②SO42-、Cl-,取少量滤液,用足量盐酸酸化后滴加氯化钡溶液,有白色沉淀生成,证明含SO42-;另取少量滤液,用足量硝酸酸化后滴加足量硝酸钡溶液,过滤,向所得滤液中滴加硝酸银溶液,有白色沉淀生成,证明含Cl-;③SO32-、OH-。
【解析】
试题分析:(1)a、亚硫酸是二元中强酸,具有酸性,故正确;b、亚硫酸中S显+4价,处于中间价态,具有氧化性,故正确;c、根据b的分析,故正确;d、亚硫酸不稳定,易分解成SO2,因此具有刺激性气味,故正确;(2)亚硫酸是二元中强酸,H2SO3![]() H++HSO3-,HSO3-
H++HSO3-,HSO3-![]() H++SO32-;(3)①根据信息,2Ag++SO32-=Ag2SO3↓;②根据反应元素守恒,溶液中含有阴离子有:Cl-, 沉淀中不含SO42-,说明溶液中含有SO42-,取少量滤液,用足量盐酸酸化后滴加氯化钡溶液,有白色沉淀生成,证明含SO42-;另取少量滤液,用足量硝酸酸化后滴加足量硝酸钡溶液,过滤,向所得滤液中滴加硝酸银溶液,有白色沉淀生成,证明含Cl-;③沉淀能使酸性高锰酸钾溶液褪色,说明含还原性离子存在,因此沉淀中含有SO32-,能溶于强酸,说明含有OH-,能溶于碱,说明含有Al3+。
H++SO32-;(3)①根据信息,2Ag++SO32-=Ag2SO3↓;②根据反应元素守恒,溶液中含有阴离子有:Cl-, 沉淀中不含SO42-,说明溶液中含有SO42-,取少量滤液,用足量盐酸酸化后滴加氯化钡溶液,有白色沉淀生成,证明含SO42-;另取少量滤液,用足量硝酸酸化后滴加足量硝酸钡溶液,过滤,向所得滤液中滴加硝酸银溶液,有白色沉淀生成,证明含Cl-;③沉淀能使酸性高锰酸钾溶液褪色,说明含还原性离子存在,因此沉淀中含有SO32-,能溶于强酸,说明含有OH-,能溶于碱,说明含有Al3+。


科目:高中化学 来源: 题型:
【题目】能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________(填序号)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
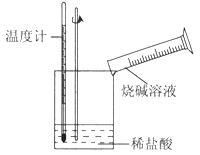
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是__________(填“吸热”或“放热”)反应,其离子方程式是_________________________。
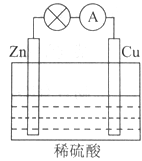
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是____________________,正极上能够观察到的现象是____________________________,正极的电极反应式是_________________________。原电池工作一段时间后,若消耗锌6.5g,则放出标准状况下气体__________L,电路中通过的电子数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(如图所示)在大试管里加入3mL乙醇、2mL冰醋酸,再缓缓加入2mL浓硫酸,边加边振荡。在另一支试管中加入饱和碳酸钠溶液用来吸收反应生成物。
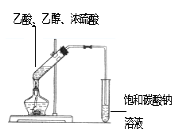
小心均匀加热大试管3-5min.请回答问题:
(1)在大试管中的反应化学方程式: ,
反应类型为_________________。
(2)用来吸收反应生成物的试管里要装饱和碳酸钠溶液的原因是: 。
(3)出气导管口不能插入碳酸钠液面的原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近《科学》杂志评出10大科技突破,其中“火星上‘找’到水的影子”名列第一。下列关于水的说法中正确的是
A水的电离过程是放热的过程
B水的电离和电解都需要电
C冰熔化成水是一个吸热的过程
D加入电解质一定会破坏水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中A与B反应生成C,其反应速率分别用v (A)、v (B)、v (C)表示。已知v (A)、v (B)、v (C)之间有以下关系2 v (B) = 3 v (A)、3 v (C) = 2 v (B)。则此反应可表示为
A.2A + 3B = 2C B.A + 3B = 2C C.3A + B = 2C D.A + B = C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6是一种优良的绝缘气体,分子结构中存在S-F键.已知1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F、S-F键需吸收的能量分别为160kJ、330kJ。则发生反应S(s)+3F2(g)═SF6(g),生成1molSF6时能量变化为( )
A、释放1220KJ B、吸收1780KJ C、 吸收1220KJ D、释放1780KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚碳酸酯无色透明,具有优异的抗冲击性,能用于制造宇航员的面罩、智能手机机身外壳等。双酚化合物是合成聚碳酸酯的单体之一,某种双酚化合物G的合成路线如下:
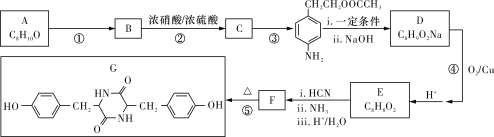
已知:![]()
NO2![]() NH2
NH2
(1)G中所含的官能团的名称是酰胺键和____________;B的核磁共振氢谱有________个峰。
(2)写出反应类型:反应① __________;反应③____________。
(3)写出A的名称 ______________;F的结构简式_____________________。
(4)写出反应④的化学方程式:_________________________。
(5)C有多种同分异构体,写出同时满足下列条件的同分异构体的结构简式________________________。
(Ⅰ)属于α-氨基酸,且苯环上有三个互为间位的取代基
(Ⅱ)与FeCl3溶液作用无显色现象
(Ⅲ)1 mol该同分异构体与足量NaOH溶液反应时消耗3 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com