
【题目】通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
A.硝酸钠、氢氧化钠 B.氧化铜、二氧化锰
C.氯化钾、二氧化锰 D.硫酸铜、氢氧化钙
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为W,物质的量浓度为c mol/L,则下列选项不正确的是( )
A.ρ=(17V+22400)/(22.4+22.4V)
B.W=17c/(1000ρ)
C.W=17V/(17V+22400)
D.c=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5物质结构与性质]
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)基态铁原子的外围电子层排布为 ,该元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4, B原子的杂化方式为 。
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“不是”)平面型分子。

(4)依据第二周期元素第一电离能的变化规律,参照图中B、C、O、F元素的位置,用小黑点表示N元素的相对位置。

(5)Al单质为面心立方晶体,其晶体参数a=0.405nm,列式表示Al单质的密度: g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下图是自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中的实验完全相同。回答下列问题:
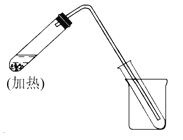
①左边大试管中要加入几片碎瓷片,其作用是 。
②该装置中使用的玻璃导管较长,其作用是 。
③烧杯中还要盛有的物质是 。
(2)如下图所示a、b、c、d分别是几种常见漏斗的上部,A、B、C、D是实际操作中各漏斗的下部插入容器中的示意图,请指出A、B、C、D分别与a、b、c、d相匹配的组合及其组合后装置在实验中的应用,例如:C和a组合,用于制取气体。

①A与 组合,用于 ,②B与 组合,用于 ,
③B与 组合,用于 ,④D与 组合,用于 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某些反应看,NH3 和H2O、NH4+ 和H3O+、NH2- 和OH-、N3- 和O2- 两两类似。据此判断下列反应正确的是
①CaO+2NH4Cl=CaCl2+2NH3↑+H2O
②2Na+2NH3=2NaNH2+H2↑
③3Mg(NH2)2=Mg3N2+4NH3↑
④NH4Cl+NaNH2=NaCl+2NH3↑
A.只有③ B.只有① C.①和② D.都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过电解MnSO4和ZnSO4制取Zn和MnO2,原料为软锰矿和闪锌矿,软锰矿中含MnO2约a%,SiO2约20%,Al2O3约4%,其余为水分,闪锌矿中含ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分。
I.(1)为了测量软锰矿中MnO2含量的测定,现将14.5g软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取25.00ml该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用0.1000molL﹣1的标准Na2S2O3溶液滴定,消耗标准液50.00ml,则软锰矿中MnO2含量 。(已知:2KI+2H2SO4+MnO2=I2+2H2O+MnSO4+K2SO4; I2+2S2O32﹣=2I﹣+S4O62﹣)
Ⅱ.研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示。

请回答下列问题:
(2)反应I的滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等.试完成反应I中生成CuSO4和MnSO4的化学方程MnO2+CuS+ = + +CuSO4+MnSO4。
(3)反应Ⅱ加入适量锌的作用是 ;如果锌过量,还会进一步发生反应的离子方程式为 。
(4)图2是Na2SO4和Na2SO410H2O的溶解度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶→ →用乙醇洗涤→干燥.用乙醇洗涤而不用水洗的原因是 。

(5)用惰性电极电解MnSO4和ZnSO4制得Zn和MnO2的总反应是: 。
(6)本工艺可以循环利用的物质除MnO2、MnCO3、ZnCO3以外,还有 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2S溶液存在水解平衡:S2-+H2O![]() HS-+OH-。下列说法正确的是( )
HS-+OH-。下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.通入H2S,HS—浓度增大
C.升高温度,c(HS—)/c(S2—)减小
D.加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超氧化钾(KO2)又称为化学氧自救剂,容易与空气中的水、二氧化碳等发生反应,主要用于煤矿井下急救。某兴趣小组拟选用如下装置制备超氧化钾(部分夹持仪器已略去).

请回答下列问题:
(1)请选择必要的装置,按气流方向的连接顺序为 (填仪器接口的字母)。
(2)请根据完整的实验装置,完成下列实验步骤:① ;②装入药品,打开分液漏斗活塞;③持续通入气体一段时间后,点燃酒精灯进行反应;④反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;⑤拆除装置,取出产物.
(3)数据记录如下:
空陶瓷管的质量 | 陶瓷管与钾的总质量 | 陶瓷管与产物的总质量 |
14.80g | 15.19g | 15.47g |
根据数据计算可得实验式KOx,则x= 。
(4)超氧化钾可吸收二氧化碳,并生成氧气,因此可以作为飞船、潜艇等密闭系统的氧气再生剂。写出超氧化钾与二氧化碳反应的化学方程式: 。与过氧化钠相比,其优点是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com