
����Ŀ�������£��������ؾ����������ṹ�����������Ļ��ϼ۲���Ϊ0�ۣ�����Ϊ��2�ۣ�����ͼ��ʾΪ�������ؾ����һ��������������˵����ȷ���ǣ� �� 
A.�������صĻ�ѧʽΪKO2 �� ÿ����������4��K+��4��O2��
B.������ÿ��K+��Χ��8��O2�� �� ÿ��O2����Χ��8��K+
C.��������ÿ��K+���������K+��8��
D.��������ÿ��K+���������K+��6��
���𰸡�A
���������⣺A������ͼ֪���þ����м����Ӹ���=8�� ![]() +6��
+6�� ![]() =4�����������Ӹ���=1+12��
=4�����������Ӹ���=1+12�� ![]() =4��������Ӻͳ��������Ӹ���֮��=4��4=1��1�������仯ѧʽΪKO2 �� ÿ����������4��K+��4��O2�� �� ��A��ȷ��B������ͼ֪��ÿ����������Χ��6�����������ӡ�ÿ��������������Χ��6�������ӣ�������������λ����6����B����
=4��������Ӻͳ��������Ӹ���֮��=4��4=1��1�������仯ѧʽΪKO2 �� ÿ����������4��K+��4��O2�� �� ��A��ȷ��B������ͼ֪��ÿ����������Χ��6�����������ӡ�ÿ��������������Χ��6�������ӣ�������������λ����6����B����
C������ͼ֪��ÿ�������Ӿ�������ļ�������3��8�� ![]() ��=12����C����
��=12����C����
D������ͼ֪��ÿ�������Ӿ�������ļ�������3��8�� ![]() ��=12����D����
��=12����D����
��ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��AΪ�����Ķ��������������A�ĺϽ���ϳ����ڻ�����ɻ����ִ�������ҵ��B��һ���Σ��ڹ�ũҵ��������;�Ϲ㣻C��F��HΪ�����ǽ������ʣ�������C��F��I��E��J��KΪ���壻E�Կ���������ܶ�Ϊ0.586��GΪҺ�壮�й����ʼ��ת����ϵ��ͼ��ͼ�в��ַ�Ӧ��������ʡ�ԣ���
����գ�
��1��B�ĵ���ʽΪ��I���ӵĿռ乹��Ϊ ��
��2����Ӧ�ڵ�ʵ������Ϊ ��
��3������a������HCl�����м��ȵ���ˮ���ԭ����������bΪ ��
��4����Ӧ�ٵ����ӷ�Ӧ����ʽΪ����Ӧ�۵Ļ�ѧ��Ӧ����ʽΪ ��
��5����֪C��ȼ����Ϊ286 kJ/mol����д����ʾ1g C��F����ȫȼ������Һ��G���Ȼ�ѧ��Ӧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е����ӣ�����ˮ��Һ�д����������( )��
A. K+��H+��SO42-��OH- B. Na+��Ca2+��CO32-��NO3-
C. Na+��H+��Cl-��CO32- D. Na+��Cu2+��SO42-��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��ɫ����Һ����ȷ���Ƿ����������ӣ�K+��Mg2+��Al3+��Fe2+��Ba2+��NO3����SO42����Cl����I����HCO3�� �� ȡ����Һ��ʵ�����£�
ʵ�鲽�� | ʵ������ |
��1��ȡ��������Һ���Ӽ��μ��� | ��Һ���ɫ |
��2��ȡ��������Һ����Ũ������CuƬ��Ũ���ᣬ���� | ����ɫ����������������������Ա�ɺ���ɫ |
��3��ȡ��������Һ����BaCl2��Һ | �а�ɫ�������� |
��4��ȡ��3���е��ϲ���Һ����AgNO3��Һ | ���ȶ��İ�ɫ�������ɣ��Ҳ�����ϡ���� |
��5��ȡ��������Һ������NaOH��Һ | �а�ɫ�������ɣ���NaOH����ʱ�����������ܽ� |
�ɴ��жϣ�����˵����ȷ���ǣ� ��
A.����ʵ�飨1������ȷ����Һ�в�����HCO![]() ��I�� �� ��Ϊ������������Ӧ����Ϊ����
��I�� �� ��Ϊ������������Ӧ����Ϊ����
B.��Һ��һ�����ڵ�������NO![]() ��SO
��SO![]() ��Cl����Mg2+��Al3+����Һ�п϶������ڵ������ǣ�Fe2+��HCO
��Cl����Mg2+��Al3+����Һ�п϶������ڵ������ǣ�Fe2+��HCO![]() ��I����Ba2+
��I����Ba2+
C.Ϊ��һ��ȷ���������ӣ�Ӧ�ò�����ɫ��Ӧ��ʵ��������K+�Ϳ���
D.ͨ��ʵ�飨1���ͣ�2���Ϳ���ȷ����Һ��һ������NO![]() ��һ��������Fe2+��I����HCO
��һ��������Fe2+��I����HCO![]() ������ʵ�鲽�裨4��������Ǵ����
������ʵ�鲽�裨4��������Ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������������������Ҫװ����ͼ1��ʾ����Ҫ�������a�Թ��а�2��3��2�����������Ũ���ᡢ�Ҵ�������Ļ���
�ڰ�Aͼ����װ�ã�ʹ����������������ͨ��b�Թ���ʢ�ı���̼������Һ�����뼸�η�̪��Һ���У�
��С�����a�Թ��еĻ��Һ��
�ܵ�b�Թ����ռ���Լ2mL����ʱֹͣ���ȣ�����b�Թܲ�������Ȼ���ô�����Һ��ֲ㣻
�ݷ��������������������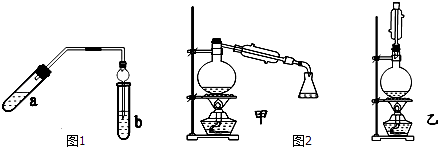
��ش��������⣺
��1��������пɹ۲쵽b�Թ�����ϸС������ð����д���÷�Ӧ�����ӷ���ʽ�� ��
��2��Aװ����ʹ�����ιܳ������������⣬��һ��Ҫ������ �� ������з���������������ʹ�õ�һ�������� ��
��3��Ϊ֤��Ũ�����ڸ÷�Ӧ�����˴�������ˮ�������ã�ijͬѧ������ͼA��ʾװ�ý���������4��ʵ�飮ʵ�鿪ʼ���þƾ�����3min���ټ���ʹ֮����3min��ʵ�����������С�Թ�b�ٲ��л���ĺ�ȣ�ʵ���¼���£�
ʵ���� | �Թ�a���Լ� | �Թ�b���Լ� | ����л���ĺ��/cm |
A | 3mL�Ҵ���2mL���ᡢ1mL18molL��1 Ũ���� | ����Na2CO3��Һ | 5.0 |
B | 3mL�Ҵ���2mL���� | 0.1 | |
C | 3mL�Ҵ���2mL���ᡢ6mL 3molL��1 H2SO4 | 1.2 | |
D | 3mL�Ҵ���2mL���ᡢ���� | 1.2 |
��ʵ��D��Ŀ������ʵ��C����գ�֤��H+��������Ӧ���д����ã�ʵ��D��Ӧ��������������Ũ�ȷֱ���mL��molL��1 ��
�ڷ���ʵ������ʵ���ţ������ݣ������Ʋ��ŨH2SO4����ˮ����������������IJ��ʣ�Ũ�������ˮ���ܹ���������������ʵ�ԭ���� ��
�ۼ���������������������IJ��ʣ���ʵ�鷢���¶ȹ������������IJ��ʷ������ͣ����ܵ�ԭ���� ��
�ܷ�����������������ϴ�����ʣ�Ϊ�˸�������������ѡ�õĸ����Ϊ������ĸ�� ��
A��P2O5 B����ˮNa2SO4 C����ʯ�� D��NaOH����
��Ϊ������÷�Ӧ���ͬѧ�������ͼ2�мס�������װ�ã�������װ��ʱ������Ӧ�����ȴ�����ñ���̼������Һ��ȡ��ƿ�еIJ��������Ϊ���������� �� �����ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У������ڶ����ЧӦ����( )
A. ��ˮ B. �� C. Fe(OH)3���� D. ��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��T��Y��ZΪ1��36��Ԫ�أ���ԭ������������������Ԫ�ص����ʻ�ṹ��Ϣ������������Ϣ�ش��������⣮
Ԫ�� | T | X | Y | Z |
���ʽṹ��Ϣ | ԭ�Ӻ���s������������p���������������ں�������Ԫ�أ����䵥���dz�������ȼ�� | ����Ϊ˫ԭ�ӷ��ӣ������к���3�Թ��õ��Ӷԣ������µ��������ȶ�������ԭ�ӽϻ��� | ��3����Ԫ�صļ������а뾶��С | ��4����Ԫ�أ�M���Ӳ�Ϊȫ����״̬�������ֻ��һ�����ӵ�ԭ�� |
��1��д��Ԫ��T�����ӽṹʾ��ͼ��д��Ԫ��X����̬�⻯��ĵ���ʽ��X�γɵĵ��ʷ��ӣ������Ҽ������м���д��ZԪ��ԭ�ӵ���Χ�����Ų�ʽ��Ԫ��Y��ԭ�Ӻ��������״��ͬ�ĵ����ƣ�
��2��Y����������������Һ��Ӧ�����ӷ���ʽ�� ��
��3��Ԫ��T���Ԫ����ȣ��ǽ����Խ�ǿ��������Ԫ�ط��ű�ʾ�������б�������֤����һ��ʵ�������������ĸ����
a�������·�������ɫ��T���ʵ���ɫ��
b��������T���⻯����ҷ�Ӧ������T�ĵ���
c������T�γɵĻ�������TԪ�س�����̬
d���Ƚ���Ԫ�صĵ�������������ʱ�õ��ӵ���Ŀ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B����������֪A�ķ���ʽΪC5Hm �� ��B�����ʽΪC5Hn��m��n��Ϊ������������ش��������⣺
��1�����й�����A����B��˵������ȷ����������ţ���
a����A����B���ܻ�Ϊͬϵ��
b����A����B���ܻ�Ϊͬ���칹��
c����m=12ʱ����Aһ��Ϊ����
d����n=11ʱ����B���ܵķ���ʽ��2��
��2������AΪ�������ҷ���������̼ԭ�Ӷ���ͬһ��ֱ���ϣ���A�Ľṹ��ʽΪ ��
��3������AΪ�������ҷ���������̼ԭ��һ�����棬��һ�������£�1mol A������1mol H2�ӳɣ���A�������� ��
��4������BΪ����ͬϵ�ȡһ��������B��ȫȼ�պ���������ͨ��������Ũ���ᣬŨ�������������1.26g����ͨ�������ļ�ʯ�ң���ʯ�ҵ���������4.4g������B�ķ���ʽΪ�����䱽���ϵ�һ�����ֻ��һ�֣�����ϴ���������B���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����ܽ�![]() ����Ϊ
����Ϊ![]() �������ʷ�Ӧ��һ����ʹKSCN��Һ������
�������ʷ�Ӧ��һ����ʹKSCN��Һ������![]()
![]() ������Fe��
������Fe��![]() ��Ӧ
��Ӧ
![]() ����ϡ���ᷴӦ
����ϡ���ᷴӦ
![]() ��Һ��ͨ������
��Һ��ͨ������![]()
![]() ��
��![]() �Ļ��������������
�Ļ��������������
![]() ��
��![]() ��Һ�м������ϡ���ᣮ
��Һ�м������ϡ���ᣮ
A. ֻ��![]() B. ֻ��
B. ֻ��![]() C. ֻ��
C. ֻ��![]() D. ȫ��
D. ȫ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com