


 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
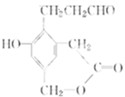 .该有机物水解后的生成物分别能与金属钠、氢氧化钠、新制氢氧化铜发生反应,从理论上可以算出1mol生成物分别与上述三种无机物反应所消耗的物质的量的比为( )
.该有机物水解后的生成物分别能与金属钠、氢氧化钠、新制氢氧化铜发生反应,从理论上可以算出1mol生成物分别与上述三种无机物反应所消耗的物质的量的比为( )| A、1:1:1 |
| B、3:2:2 |
| C、3:2:3 |
| D、6:4:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2F2+2H2O=4HF+O2 | ||||
| B、AgNO3+NaCl=AgCl↓+NaNO3 | ||||
C、3CO+Fe2O3
| ||||
D、MgCl2 (熔融)
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用Na2CO3溶液作洗涤剂:CO32-+2H2O?H2CO3+2OH- | ||||
B、用铜作电极电解氢氧化钠溶液:2H2O
| ||||
C、“银镜反应”:RCHO+2Ag(NH3)2++2OH-
| ||||
| D、交警用酸化的含Cr2O72-的硅胶检测司机酒后驾驶的反应:2Cr2O72-+3C2H5OH+16H+→4Cr3++3CH3COOH+11H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com