
【题目】下列事实不能说明元素的金属性或非金属性相对强弱的是
选项 | 事实 | 推论 |
A | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
B | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
C | SO2与NaHCO3溶液反应生成CO2 | 非金属性:S>C |
D | t℃时,Br2+H2 I2+H2 | 非金属性:Br>I |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】氯喹(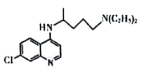 )对治疗新冠病毒肺炎有明确疗效,氯喹的合成方法如下。
)对治疗新冠病毒肺炎有明确疗效,氯喹的合成方法如下。
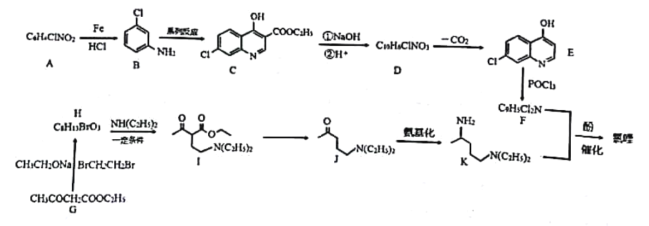
回答下列问题
(1)A中所含官能团的名称是_______________;
(2)写出G到H的反应类型_______________;
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。B与足量氢气反应生成物X,写出X的结构简式.并用星号(*)标出X中的手性碳__________________;
(4)写出C到D过程中①的反应方程式________________________;
(5)写出具有醛基、羧基、核磁共振氢谱只有四组峰的G的同分异构体所有的结构简式(不考虑立体异构)__________________________。
(6)参考以上合成路线,设计由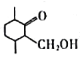 、1一溴丙烷为原料合成
、1一溴丙烷为原料合成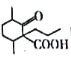 的合成路线_________________________(无机试剂与含两个碳的有机物任选)。
的合成路线_________________________(无机试剂与含两个碳的有机物任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种用途广泛的常见氧化剂,主要用于化工、防腐及制药工业等。
I.某课外小组设计以锰酸钾制备高锰酸钾的方案如下:
i.锰酸钾的制备:
(1)将二氧化锰、氨酸钾和氢氧化钾固体放入______(填字母)中熔融制锰酸钾。
A.烧杯B.瓷坩埚C.蒸发皿D.铁坩埚
ii.高锰酸钾的制备(装置如图所示,加热及夹持装置省略):
将i中制得的锰酸钾加少量蒸馏水溶解,得墨绿色溶液,倒入三颈烧瓶中。打开甲装置中的分液漏斗活塞加入稀硫酸,加热,使生成的乙酸进入乙装置中并水浴加热。搅拌丙装置中的溶液,锰酸钾在酸性条件下反应生成高锰酸钾和二氧化锰。
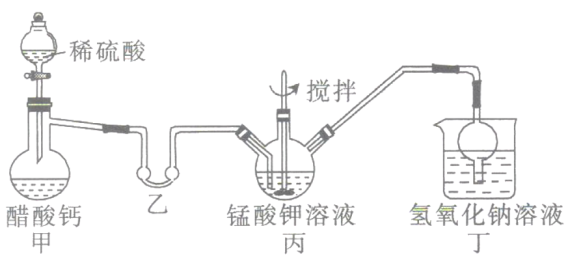
(2)检验该装置气密性的方法:连接好装置,_________________。
(3)乙装置的作用是___________;丁装置中NaOH溶液的作用是____________________。
(4)将三颈烧瓶中所得产物进行过滤,将滤液倒入蒸发皿中,_______、______、抽滤,得到针状的高锰酸钾晶体。高锰酸钾晶体只能低温烘干,其原因为_____________________。
II.利用氧化还原滴定法测定高锰酸钾的纯度,发生反应的化学方程式为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
(5)量取一定体积的高锰酸钾溶液需使用滴定管_______(填字母)。

(6)若在实验过程中存在下列操作,会使所测KMnO4浓度偏高的是____(填字母)。
A锥形瓶用水洗之后末用待测液润洗
B.盛草酸溶液的滴定管滴定前尖嘴部分有气泡,滴定终点时无气泡
C.滴定时,草酸溶液洒落瓶外
D.盛装KMnO4溶液的滴定管用水洗后,未用KMnO4溶液润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E原子序数依次增大。A元素原子半径小于B,元素A、 E同主族。B是组成有机物的必要元素,C元素最高价氧化物对应水化物X与其氢化物Y反应生成一种盐。D元素的原子最外层电子数是其电子层数的3倍。
(1) E元素在周期表中的位置是__________; X和Y形成的化合物的化学式为___________;
(2)A、D两元素形成的原子个数比为1: 1的化合物的电子式为____________;
(3) Y的水溶液与氯化镁溶液反应的离子方程式为______________;
(4)元素B的单质能在加热条件下与浓硫酸反应,产物中含有两种气体物质,该反应的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.向Ba(AlO2)2溶液中加入过量NaHSO4溶液:Ba2++SO42-=BaSO4↓
B.泡沫灭火器中Al(SO4)3和NaHCO3溶液混合:Al3++3HCO3-=Al(OH)3↓+3CO2↑
C.以铜为电极,电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.向Cu(OH)2浊液中滴加饱和FeCl3溶液产生红褐色沉淀:Cu(OH)2+Fe3+Fe(OH)3+Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 0.50molL﹣1NaOH标准液10.00mL,将未知浓度的盐酸20.00mL恰好滴定至终点,下列说法正确的是( )
A. 若滴定完毕,滴定管尖嘴悬有一滴液体,则所测的盐酸浓度偏大
B. 用量筒量取上述盐酸
C. 若选用酚酞作指示剂,终点时,液体恰好褪色
D. 盐酸的浓度为1.00 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的离子方程式书写正确的是
A.向氯化铁溶液中加入铁粉,颜色变浅:2Fe3++Fe=3Fe2+
B.向碳酸氢钠溶液中滴加稀盐酸,产生气体:![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
C.向稀硝酸溶液加入少量锌粉:Zn+2H+=Zn2++H2↑
D.向氢氧化钡溶液中滴加稀硫酸,生成沉淀:Ba2++![]() =BaSO4↓
=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池应用很广。某种锂离子二次电池的电极材料主要是钴酸锂(LiCoO2)和石墨。钴是一种稀有的贵重金属,废旧锂离子电池电极材料的回收再生意义重大。
(1)锂离子电池(又称锂离子浓差电池)的工作原理:
ⅰ.充电过程:Li+从含LiCoO2的电极中脱出,正三价Co被氧化,此时该极处于贫锂态(Li1-xCoO2)。
ⅱ.放电过程原理示意图如图所示:
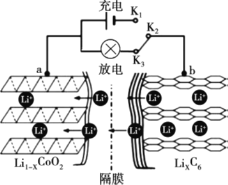
① 放电时,电子的流动方向为______。(用a、b、K2、K3)
② 放电时,正极的电极反应式为______。
(2)钴酸锂回收再生流程如下:
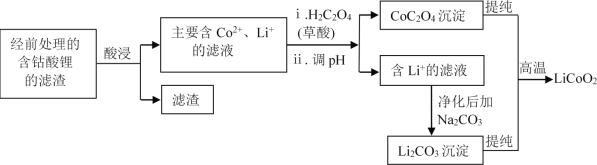
① 用H2SO4酸浸时,通常添加30%的H2O2以提高浸出效率,其中H2O2的作用是______。
② 用盐酸代替H2SO4和H2O2,浸出效率也很高,但工业上不使用盐酸。主要原因是:
ⅰ.会产生有毒、有污染的气体。写出相应反应的化学方程式_______。
ⅱ.Cl-对建筑材料的腐蚀及带来的水体问题等。
③ 其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30% H2O2 混合液中的浸出率曲线如图,请解释随着温度升高,钴的浸出率先升高后降低的原因:______。
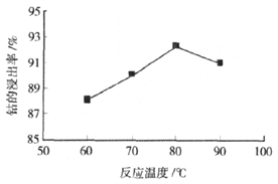
④ 已知草酸为二元弱酸,应用化学平衡移动原理,结合化学用语解释CoC2O4沉淀的同时溶液酸性增强的原因:______。
⑤ 高温下,在O2存在时纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com