
【题目】五种短周期元素A、B、C、D、E原子序数依次增大。A元素原子半径小于B,元素A、 E同主族。B是组成有机物的必要元素,C元素最高价氧化物对应水化物X与其氢化物Y反应生成一种盐。D元素的原子最外层电子数是其电子层数的3倍。
(1) E元素在周期表中的位置是__________; X和Y形成的化合物的化学式为___________;
(2)A、D两元素形成的原子个数比为1: 1的化合物的电子式为____________;
(3) Y的水溶液与氯化镁溶液反应的离子方程式为______________;
(4)元素B的单质能在加热条件下与浓硫酸反应,产物中含有两种气体物质,该反应的化学方程式为_____________。
【答案】第三周期第IA族 NH4NO3 ![]() 2NH3H2O + Mg2+ = Mg(OH)2↓+ 2
2NH3H2O + Mg2+ = Mg(OH)2↓+ 2![]() C+ 2H2SO4(浓)
C+ 2H2SO4(浓)![]() CO2↑+2SO2↑+ 2H2O
CO2↑+2SO2↑+ 2H2O
【解析】
五种短周期元素A、B、C、D、E原子序数依次增大。B是组成有机物的必要元素,说明B为碳元素,D元素的原子最外层电子数是其电子层数的3倍,说明D为氧元素,C为氮元素,A元素原子半径小于B,说明不在同一周期,应为氢元素,A和E同主族,E为钠元素。C元素最高价氧化物对应水化物X为硝酸,氢化物Y为氨气。
(1) E元素为钠元素,在周期表中的位置是第三周期第IA族; 硝酸和氨气形成的化合物的化学式为NH4NO3;
(2)H、O两元素形成的原子个数比为1: 1的化合物为过氧化氢,电子式为![]() ;
;
(3) Y的水溶液为氨水,与氯化镁溶液反应的离子方程式为2NH3H2O + Mg2+ = Mg(OH)2↓+ 2![]() ;
;
(4)元素B的单质为碳,能在加热条件下与浓硫酸反应,产物中含有两种气体物质,该反应的化学方程式为C+ 2H2SO4(浓)![]() CO2↑+2SO2↑+ 2H2O。
CO2↑+2SO2↑+ 2H2O。


 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】某温度下,在2L容器中发生反应,A、B、C物质的量随时间变化的曲线如图所示。下列叙述中正确的是
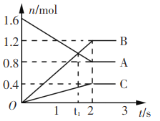
A.该反应的化学方程式为2A![]() B+3C
B+3C
B.反应开始至2s时,A的平均反应速率为0.4 mol(/L·s)
C.t1时刻,该反应达到化学平衡状态
D.反应开始至1s时,生成C的物质的量大于0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烃的说法错误的是( )

A.该烃分子中共面的碳原子最多为 14 个
B.该烃分子中共直线的碳原子最多为 6 个
C.该烃存在顺反异构
D.该物质可以发生氧化反应、取代反应、加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用软锰矿浆(主要成分是MnO2)吸收工业废气中的SO2,并制备硫酸锰的生产流程如下(浸出液的pH<2,其中除含Mn2+外,还含有少量Fe2+、Al3+、Ca2+等金属离子):

“操作1”的滤液通过阳离子吸附剂除去Ca2+。金属离子形成氢氧化物沉淀时的pH见下表:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 7.6 | 9.7 |
Fe3+ | 2.7 | 3.7 |
Al3+ | 3.8 | 4.7 |
Mn2+ | 8.3 | 9.8 |
(1)浸出过程中被氧化的物质的化学式为____________。
(2)氧化过程中主要反应的离子方程式为_____________
(3)在氧化后的液体中加入石灰浆调节pH, pH 的范围是__________。
(4)操作2包括蒸发浓缩、__________、 过滤、 洗涤、干燥等操作。
(5)为测定所得MnSO4·H2O的纯度,准确称取上述样品1.720 g加入适量H2SO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+后,配成200 mL溶液。取20.00 mL该溶液,向其中逐滴加入0.0500 mol·L-1的FeSO4溶液,发生如下反应: Fe2+ +Mn3+=== Fe3+ + Mn2+当反应恰好完全进行时,共消耗FeSO4溶液19.50 mL。计算MnSO4·H2O的纯度(写出计算过程,结果保留四位有效数字)__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼钼的化学原理为:
①2MoS2+7O2![]() 2MoO3+4SO2
2MoO3+4SO2
②MoO3+2NH3·H2O=(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl
④H2MoO4![]() MoO3+H2O
MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法中正确的是
A.MoS2煅烧产生的尾气可以直接排到空气中
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能说明元素的金属性或非金属性相对强弱的是
选项 | 事实 | 推论 |
A | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
B | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
C | SO2与NaHCO3溶液反应生成CO2 | 非金属性:S>C |
D | t℃时,Br2+H2 I2+H2 | 非金属性:Br>I |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素a、b、c、d、e,其原子半径与原子序数的关系如图,下列说法错误的是
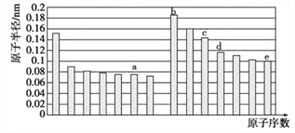
A. c元素的离子半径比e的离子半径小
B. d元素对应的最高价氧化物的水化物酸性比e元素弱
C. b、c、d三种元素对应的最高价氧化物的水化物相互间能发生反应
D. a与b两种元素可形成既有离子键又有非极性共价键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿“烧渣”(主要成分Fe3O4,Fe2O3,FeO和部分难溶于酸的杂质)制备绿矾(FeSO47H2O)的流程如下:

已知:FeS2(S的化合价为-1)难溶于水。
(1)①中加入的酸为____________(填名称)。
(2)①中生成Fe3+的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O、____________。
(3)检验②中Fe3+已经完全转化为Fe2+实验方法:取适量溶液2,____________。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、____________、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L的恒容密闭容器中,X、Y、Z三种无色气体的物质的量随时间的变化曲线如图所示。
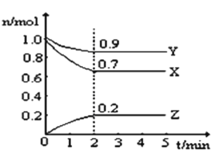
(1)起始时X的浓度为c(X)=_______;反应从开始至2分钟末,Y的转化率为α(Y)=________;用Z的浓度变化表示0-2分钟内的平均反应速率为v(Z)=___________。
(2)由图中所给数据进行分析,该反应的化学方程式为___________。
(3)能说明该反应已达到平衡状态的是___________
A.![]() (X)=3
(X)=3![]() (Y)
(Y)
B.容器内气体密度不变
C.2![]() 逆(X)=3
逆(X)=3![]() 正(Z)
正(Z)
D.各组分的物质的量相等
E.混合气体的平均相对分子质量不再改变的状态
F.容器内气体颜色不再发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com