
【题目】工业上用氟硅酸钠(Na2SiF6)生产冰晶石(Na3AlF6)的工艺流程如下:
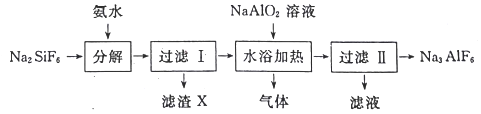
(1)分解过程发生的反应为:Na2SiF6+4NH3H2O═2NaF+4NH4F+X↓+2H2O。工业上把滤渣X叫白炭黑,其化学式为______________________。
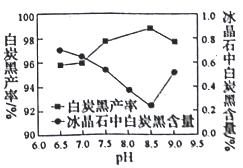
(2)分解时白炭黑产率和冰晶石纯度与pH的关系如图所示,分解时需要控制溶液的pH=________;能提高其分解速率的措施有___________ (填标号)。
A.快速搅拌B.加热混合液至100℃C.降低氨水浓度
(3)流程中可循环利用的物质为_________(写化学式);冰晶石在电解冶炼铝中的作用是降低氧化铝的熔融温度、________________________和提髙产率。
(4)水浴加热过程中生成冰晶石的化学方程式为_____________________________。
【答案】 SiO2 8.5 A NH3(或NH3·H2O) 减少能源消耗(或降低生产成本) 2NaF+4NH4F+NaAlO2 ![]() NaAlF6↓+4 NH3↑+2 H2O
NaAlF6↓+4 NH3↑+2 H2O
【解析】(1)分解过程发生的反应为:Na2SiF6+4NH3H2O=2NaF+4NH4F+X↓+2H2O,化学反应前后原子守恒,则X为SiO2;(2)从图可知,pH为8.5时,冰晶石中白炭黑的含量较低,冰晶石纯度较高;能提高其分解速率的措施有A.快速搅拌可以加快反应速率,A正确;B.加热混合液至100℃,氨水受热分解,反应物浓度小,化学反应速率减慢,B错误;C.降低氨水浓度,化学反应速率减慢,C错误;答案选A;(3)第二次过滤所得滤液为氨气水溶液,可循环使用;冰晶石降低氧化铝的熔融温度,减少能源消耗(或降低生产成本);(4)根据以上分析可知水浴加热过程中生成冰晶石的化学方程式为2NaF+4NH4F+NaAlO2 ![]() NaAlF6↓+4 NH3↑+2H2O。
NaAlF6↓+4 NH3↑+2H2O。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】碳酸铵[(NH4)2CO3]室温下能自发地分解产生氨气,对其说法正确的是
A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大
B.碳酸铵分解是因为外界给予了能量
C.该反应的ΔH-TΔS>0
D.碳酸盐都不稳定,都能自发分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究有机物的方法有很多,常用的有①核磁共振氢谱②蒸馏③重结晶④萃取⑤红外光谱⑥过滤,其中用于有机物分离或提纯的方法有____,用于分子结构确定的有____(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识填空。
(1)与标准状况下4.48L CO2中所含氧原子数目相同的水的质量是g;
(2)V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中SO42﹣的物质的量浓度为mol/L;
(3)9.2g氮的氧化物(NOx)中含氮原子0.2mol,则x的数值为;
(4)0.4mol某气体的体积为9.8L,则该气体的摩尔体积为 , 气体所处的条件(填“是”或“不是”)标准状况.
(5)下列是常用的中和胃酸的药物:
药名 | 胃舒平 | 达喜 |
有效成分的化学式 | Al(OH)3 | Al2Mg6(OH)16CO34H2O |
相对分子质量 | 78 | 530 |
每片含有效成份的药量 | 0.245g | 0.5g |
估算10片胃舒平和5片达喜,含铝的物质的量较多的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解CuCl2和NaCl的混合溶液,阴极和阳极上分别析出的物质是( )
A. H2和Cl2 B. Cu和Cl2 C. H2和O2 D. Cu和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列说法正确的是
A. 标准状况下,11.2LH2O中含有的氧原子数为0.5NA
B. 14g由CO和N2组成的混合气体中含有的分子总数为0.5NA
C. 1L0.5mol·L-1醋酸溶液中含有的氢离子数目为0.5NA
D. H2O2分解制取O2的反应中,每生成0.125molO2,转移的电子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 可用蘸有浓盐酸的棉棒检验输送氨气的管道是否漏气
B. 浓硝酸保存在无色玻璃试剂瓶中
C. 铵态氮肥不能与草木灰混合使用,但可以暴晒在太阳底下
D. SO2具有漂白性,故可使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.标准状况下,11.2 L的己烷所含的分子数为0.5NA
B.28 g乙烯所含共用电子对数目为6NA
C.11.2L一氯甲烷所含分子数为0.5NA
D.1mol甲基所含的电子总数为9NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com