
将钠、铁、镁、铝各取0.1mol,分别投入足量的稀H2SO4中,充分反应后,放出的气体( )。
A.钠最多 B.一样多 C.铁最多 D.铝最多
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.只有反应体系中所有分子同时都发生有效碰撞的反应才是放热反应
B.通常条件下能够自发进行的反应必须具备△H和△S均大于0
C.任何化学反应只要是自发进行的放热反应都可以设计成原电池,为外界提供电能
D.实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配置氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定的温度下,在固定容积的密闭容器中,能表示反应X(气)+2Y(气)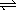 2Z(气)一定达到化学平衡状态的是:
2Z(气)一定达到化学平衡状态的是:
①.容器内压强不随时间改变; ②.C(x)·C2(Y) =C2(z)
③.生成Z的速率与生成Y的速率相等; ④.容器内混合气体的密度不随时间改变
⑤.X、Y、Z的物质的量之比 1∶2∶2
⑥.一定温度下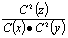 为一常数
为一常数
A.①③⑤ B.①③⑥ C.②④⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol[Ag (NH3)2]OH配合物中含有9NA个σ键
B.标准状况下,22.4L C2H6O中含C-H键5NA
C.1mol冰醋酸和lmol乙醇在加热和浓硫酸条件下充分反应生成的水分子数为NA
D.KClO3+6HCl ===KCl+3Cl2↑+3H2O反应中,生成71g Cl2时,转移的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某合成氨厂利用附近化工厂副产品CaSO4设计了以下制备(NH4)2SO4的工艺流程:
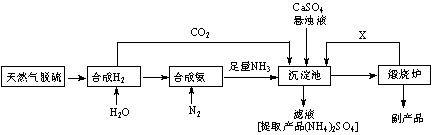 |
请回答以下问题:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,
得到单质硫并使吸收液再生,写出再生反应的化学方程式: 。
(2)工业上在500℃左右使用铁触媒作为催化剂合成NH3,
①铁触媒中含有Fe3+,,则Fe3+的核外电子排布式为
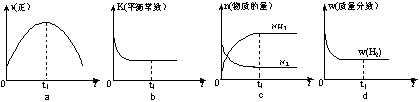
②500℃时,合成塔中的反应为:N2(g)+3H2(g)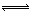 2NH3(g) ∆H= -92.4kJ/mol在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是 (填字母编号)。
2NH3(g) ∆H= -92.4kJ/mol在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是 (填字母编号)。
 |
(3)沉淀池中反应的化学方程式为
(4)在上述流程中可以循环使用的X是 (填化学式),从(NH4)2SO4溶液中获得
(NH4)2SO4晶体操作的步骤是是加热浓缩、 、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
把足量的铁粉投入到溶解有硫酸和硫酸铜的溶液中,充分反应后,剩余金属粉末的质量与原加入铁粉的质量相等,则原溶液中H+与SO42-的物质的量浓度之比为( )。
A.1∶4 B.2∶7 C.1∶2 D.3∶8
查看答案和解析>>
科目:高中化学 来源: 题型:
图表归纳是学习化学的一种常用方法,某同学如下归纳的下表与上图中对应正确的是
| 选项 | X | Y | Z |
|
| A | 胶体 | 混合物 | 淀粉溶液 | |
| B | 化合物 | 酸性氧化物 | 一氧化氮 | |
| C | 气态氢化物 | 化合物 | 液溴 | |
| D | 强电解质 | 强酸 | 硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2===LiNH2+LiH,下列有关说法正确的是( )
A.Li2NH中N的化合价是-1
B.该反应中H2既是氧化剂又是还原剂
C.Li+和H-的离子半径相等
D.此法储氢和钢瓶储氢的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液,同时开始反应,出现浑浊最早的是
A.20℃时 5mL 0.05mol·L-1 Na2S2O3溶液与5mL 0.1mol·L-1硫酸混合
B.20℃时 50mL 0.1mol·L-1 Na2S2O3溶液与50mL 0.1mol·L-1硫酸混合
C.10℃时 5mL 0.05mol·L-1 Na2S2O3溶液与5mL 0.1mol·L-1硫酸混合
D.10℃时 5mL 0.1mol·L-1 Na2S2O3溶液与5mL 0.1mol·L-1硫酸混合
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com