
【题目】某学生用如图所示装置进行化学反应X+2Y![]() 2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述中正确的是
2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述中正确的是

①该反应为放热反应;②该反应为吸热反应;③生成物的总能量比反应物的总能量更高;④反应物的总能量比生成物的总能量更高;⑤该反应过程可以看成是“贮存“于X、Y内部的部分能量转化为热能而释放出来。
A. ①④⑤ B. ①④ C. ①③ D. ②③⑤
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,根据所给的10种元素,完成以下各小题..
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
二 | C | N | O | Ne | ||||
三 | Na | Mg | Al | Si | S | Cl |
(1)镁的原子结构示意图为 .
(2)H2SO4与HClO4中,酸性较强的是 .
(3)NaOH与Al (OH)3中,属于两性氢氧化物的是 . 它常用作治疗胃酸(含盐酸)过多的药物,该反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在新制氯水中滴加NaOH 溶液,溶液中水电离出来的c水(H+)的对数与NaOH 溶液体积之间的关系如图所示。下列推断正确的是
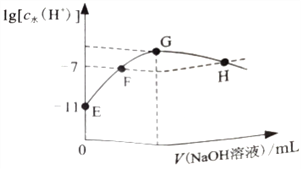
A. 用pH试纸测定E点对应的溶液,其pH=3
B. F、H点对应的溶液中都存在c(Na+)=c(Cl-)+c(ClO-)
C. 加水稀释H点对应的溶液,溶液的pH增大
D. G点对应的溶液中c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、已知34Se的原子结构示意图如图所示,回答下列问题:

(1)Se在元素周期表中的位置是__________。
(2)由Se在周期表中的位置分析判断下列说法正确的是__________。
A.热稳定性:PH3>H2S>H2Se B.还原性:H2Se>HBr>HCl
C.离子半径:Se2->Cl->K+ D.酸性:HClO3>HBrO3>H2SeO3
Ⅱ、已知:X表示卤族元素
(1)HClO的电子式是__________。
(2)氯气通入Ca(OH)2可以制得漂白粉,反应的化学方程式为__________。
(3)共价键的极性随着两元素的非金属性差异增大而增强,HX共价键的极性由强到弱的顺序是__________。
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列方程式
(1)浓硫酸和碳反应的化学方程式是__________________________________________;
(2)过氧化钠与二氧化碳反应的化学方程式为______________________________;
(3)高锰酸钾溶液与浓盐酸反应的离子方程式为_____________________________;
(4)氧化铝与氢氧化钠溶液反应的离子方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能成功的是:
①将乙酸和乙醇混合加热制乙酸乙酯
②苯和浓溴水反应制溴苯
③CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型
④用2mL0.1mol/L的CuSO4溶液和2mL0.1mol/L的NaOH溶液混合,然后加入几滴乙醛,加热,根据是否产生红色沉淀来检验醛基。
A.①②③④ B.①③④ C.①②③ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(NH2COONH4)是一种白色固体,易分解,易水解,可用作肥料、灭火剂、洗涤剂等。实验室制备氨基甲酸铵的反应如下:2NH3(g)+CO2(g) ![]() NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:
NH2 COONH4(s) △H<0,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则水解生成碳酸铵或碳酸氢铵。某化学兴趣小组按下图装置进行如下实验:
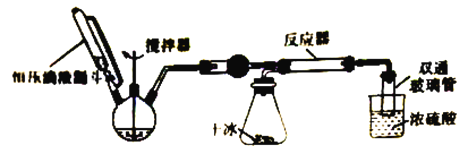
步骤1:按图连接好实验装置,____________________。
步骤2:在相应仪器中装入药品,其中1在三颈烧瓶中加入足量的氢氧化钠固体,在恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品。
……
请回答下列问题:
(1)将步骤1补充完整:________________________
(2)干燥管中盛放的药品是___________________________
(3)对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点有____________________(写出一种即可)。
(4)三颈烧瓶中产生氨气的原理是________________________________。
(5)反应后期随着产生CO2气流减慢,导致反应物比例不当,可采取的措施是________________。
(6)尾气处理装置中双通玻璃管的作用是_________________(用文字叙述),浓硫酸的作用是_______________、______________。
(7)取部分变质(混有碳酸氢铵的氨基甲酸铵)样品1.173g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500g。则样品中氨基甲酸铵的物质的量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列平衡体系中,升温或减压都能使平衡向正反应方向移动的是(ΔH<0表示放热)( )
A.N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
B.N2(g)+O2(g) ![]() 2NO(g) ΔH<0
2NO(g) ΔH<0
C.2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
D.C(s)+2H2O(g) ![]() CO2(g)+2H2(g) ΔH>0
CO2(g)+2H2(g) ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com