
����Ŀ����500��ʱ����4molSO2��2molO2����4L���ܱ������У�5���Ӻ�Ӧ�ﵽƽ�⣺2SO2��O2![]() 2SO3�����ƽ��ʱSO3��Ũ��Ϊ0.5mol��L��1��
2SO3�����ƽ��ʱSO3��Ũ��Ϊ0.5mol��L��1��
��1����500��ʱ���÷�Ӧƽ�ⳣ��K��_____
��2����Ӧ�ﵽƽ��ʱ��SO2��ת����Ϊ______
��3���ӿ�ʼ��Ӧ���ﵽƽ��״̬ ��Ӧ����v(O2)��_____
��4���÷�Ӧ�ڵ���ʱ���Է����У���÷�Ӧ������Ӧ��_____(��������������������)��Ӧ
��5����500��ʱ����2L���ܱ������У�����������Ӧ��ijһʱ�̲��������SO2��O2��SO3�����ʵ����ֱ�Ϊ1mol��2mol��2mol���ʱ���淴Ӧ���ʴ�СΪv(��)____v(��)��������������������������
���𰸡�4 50% 0.05 mol��L��1��min��1 ���� =
��������
��һ���¶��£���4molSO2��2molO2����4L���ܱ������У�c(SO3)=0.5mol/L����������ʽ������(1)~(3)��
(4)�÷�Ӧ����S��0���ڵ���ʱ���Է����У���Ҫ��G=��H-T��S��0���ݴ˷����жϣ�
(5)���ȼ���Qc������Qc��K�Ĵ�С��ϵ�����жϡ�
��һ���¶��£���4molSO2��2molO2����4L���ܱ������У�5���Ӻ�Ӧ��2SO2��O2![]() 2SO3�ﵽƽ�⣬c(SO3)=0.5mol/L����ת�������������ʵ���Ϊx����
2SO3�ﵽƽ�⣬c(SO3)=0.5mol/L����ת�������������ʵ���Ϊx����
2SO2 + O2![]() 2SO3
2SO3
��ʼ(mol) 4 2 0
ת��(mol) 2x x 2x
ƽ��(mol) 4-2x 2-x 2x
��c(SO3)=![]() =0.5mol/L����ã�x=1mol����ƽ����c(O2)=
=0.5mol/L����ã�x=1mol����ƽ����c(O2)=![]() =0.25mol/L��c(SO2)=
=0.25mol/L��c(SO2)=![]() =0.5mol/L��
=0.5mol/L��
(1)���¶���ƽ�ⳣ��K=![]() =4L/mol���ʴ�Ϊ��4L/mol(��4)��
=4L/mol���ʴ�Ϊ��4L/mol(��4)��
(2)ƽ��ʱSO2��ת����=![]() ��100%=50%���ʴ�Ϊ��50%��
��100%=50%���ʴ�Ϊ��50%��
(3)�ӿ�ʼ��Ӧ���ﵽƽ��״̬��ʱ��Ϊ5���ӣ�O2�ķ�Ӧ����v(O2)��![]() =0.05 mol/(L��nim)���ʴ�Ϊ��0.05 mol/(L��min)��
=0.05 mol/(L��nim)���ʴ�Ϊ��0.05 mol/(L��min)��
(4)�÷�Ӧ����S��0���ڵ���ʱ���Է����У�����G=��H-T��S��0������H��0���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���ʴ�Ϊ�����ȣ�
(5)�������£���Ӧ2SO2��O2![]() 2SO3��Qc=
2SO3��Qc=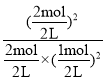 =4=K=4����˷�ӦΪƽ��״̬�����淴Ӧ���ʵ�������Ӧ���ʣ��ʴ�Ϊ��=��
=4=K=4����˷�ӦΪƽ��״̬�����淴Ӧ���ʵ�������Ӧ���ʣ��ʴ�Ϊ��=��


 �߲������Ӧ��һ��ͨϵ�д�
�߲������Ӧ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�òⶨ�к��ȵ�ʵ�鲽�����£�
������Ͳ��ȡ50 mL 0.50 mol��L��1���ᵹ��С�ձ��У���������¶ȣ�
������һ��Ͳ��ȡ50 mL 0.55 mol��L��1 NaOH��Һ������ͬһ�¶ȼƲ�����¶ȣ�
�۽�NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ���û��Һ����¶ȡ��ش��������⣺

��1����ͼ��������δ������������______��__________��
��2��Ϊʲô����NaOH��ҺҪ�Թ���_________________��
��3������NaOH��Һ����ȷ������_______________________��
��4���ֽ�һ������ϡ����������Һ��ϡ����������Һ��ϡ��ˮ�ֱ��1 L 1 mol��L��1��ϡ����ǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�Ϊ��H1����H2����H3������H1����H2����H3�Ĵ�С��ϵΪ______��
��5���������������������Һ���ܶȶ���1 g��cm��3����֪�кͷ�Ӧ��������Һ�ı�����c��4.18 J��g��1������1��Ϊ�˼����к��ȣ�ijѧ��ʵ���¼�������£�
ʵ�� ��� | ��ʼ�¶�t1/ �� | ��ֹ�¶�t2/ �� | |
���� | ����������Һ | �����Һ | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
���ݸ�ѧ����ʵ�����ݼ��㣬��ʵ���õ��к�����H��______(�������һλС��)��
��6��____(������������������)��Ba(OH)2��Һ�������������������Һ�����ᣬ������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ��1 mol/L��HClO2�ͣ�1 mol/L��HMnO4��������Һ����ʼʱ�������ΪVo���ֱ�������Һ�м�ˮ����ϡ�ͣ�ϡ�ͺ���Һ���ΪV������������ͼ��ʾ������˵����ȷ���� ( )

A. ϡ��ǰ�ֱ���1mol��L-1��NaOH��Һ�кͣ����ĵ�NaOH��Һ�����HMnO4��HClO2
B. ��ϡ����pH��Ϊ3ʱ����Һ��c(ClO2-)��c(MnO4-��
C. ��0��pH��5ʱ��HMnO4��Һ���㣬pH= ![]()
D. �����£�Ũ�Ⱦ�Ϊ0.1mol��L-1��NaClO2��NaMnO4��Һ��pH: NaMnO4��NaClO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ÿ��ȡ20 g��ˮ���ϸ��չ��ˡ���������ȴ�������������ʵ�鲽��淶����������ʵ�����Σ�ƽ���ù�̬��a g���ú�ˮ�к��Ȼ��Ƶ�����������(����)
A.����5a%
B.��5a%
C.����5a%
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����������һ�ܱ������г���һ����CO2���壬�������������ۣ�������Ӧ��Fe(s)��CO2(g)![]() FeO(s)��CO(g)����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
FeO(s)��CO(g)����֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
T/�� | 1200 | 1100 | 1000 | 900 | 800 |
K | 0.36 | 0.49 | 1.0 | 1.23 | 1.89 |
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��______��
��2���÷�ӦΪ______(��������������������)��Ӧ��
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������____��
A��������ѹǿ���� B�����������c(CO)����
C����������ƽ����Է����������� D��c(CO2)��c(CO)
��4�����д�ʩ�У��ܹ��ı�ƽ��ʱc(CO)/c(CO2)�ı�ֵ����_____(�����)��
A���¶� B�����۵���(����)
C��ѹǿ D��CO����
��5����900���£��÷�Ӧ�ﵽƽ��ʱ��CO2�����ʵ���Ũ��Ϊ2mol��L-1�����ʱc(CO)��____ mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A. ʵ���ҿ������ű���ʳ��ˮ�ķ����ռ�����
B. ��ͭ�ۺ�п�ۻ�Ϻ����ϡ�����У�������������ʱȲ���ͭ�ۿ�
C. ��ѹ�����ڹ�ҵ�Ϻϳɰ�
D. ����ˮƿʱ��ƿ���������������ĭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£������й�������ȷ����
A. ��0.1 mol��L1 Na2CO3��Һ��ͨ������CO2�����c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. �����£�pH=6��NaHSO3��Һ�У�c(![]() )c(H2SO3)=9.9��107 mol��L1
)c(H2SO3)=9.9��107 mol��L1
C. �����ʵ���Ũ�ȡ��������Na2CO3��NaHCO3��ϣ�![]() <
<![]()
D. 0.1 mol��L1 Na2C2O4��Һ��0.1 mol��L1 HCl��Һ�������ϣ�H2C2O4Ϊ��Ԫ���ᣩ��2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ����ú�ˮ�Ʊ�����þ��������ͼ��ʾ�����ͼ�ش��������⣺
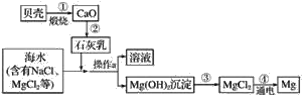
��1��������Ҫ�ɷֵĻ�ѧʽ��__��
��2���ڢڲ�������ʯ�Һ�ˮ��Ӧ��ȡʯ����(��Ҫ�ɷ�����������)��д����ȡʯ����Ļ�ѧ����ʽ��__��������Ӧ������__��
��3���ڢ۲��ǽ���������������þ�����ᷴӦ�����Ȼ�þ��д���÷�Ӧ�Ļ�ѧ����ʽ��__���÷�Ӧ����������__��
��4���ڢܲ�����ˮMgCl2������״̬�£�ͨ�������Mg��Cl2���÷�Ӧ�Ļ�ѧ����ʽ��___����Ӧ����������__��
��5��Ҫʹ��ˮ��MgCl2��ȫת��Ϊ����Mg(OH)2������ʯ�������Ӧ������ȷ����ˮ�е�MgCl2��ȫ��ת��ΪMg(OH)2�ķ�����ȡ�ϲ���Һ�����������м�������������Һ���۲쵽__��
��6����ˮ�б��������Ȼ�þ��������Ӻ�ˮ����ȡMgCl2ʱ��Ҫ������MgCl2��Mg(OH)2��MgCl2����ת��ԭ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000molL-1NaOH��Һ�ζ�20mL0.1000molL-1H3PO4��Һ����Һ��pH������NaOH��Һ�������ϵ��ͼ��ʾ������˵������ȷ���ǣ� )

A.H3PO4�ĵ���ƽ�ⳣ��Ka1ԼΪ10-2
B.��V(NaOH��Һ)=40mLʱ��c(PO![]() )+c(OH-)=c(H+)+c(H2PO
)+c(OH-)=c(H+)+c(H2PO![]() )+2c(H3PO4)
)+2c(H3PO4)
C.��pH=7ʱ��c(Na+)=c(H2PO![]() )+2c(HPO
)+2c(HPO![]() )+3c(PO
)+3c(PO![]() )
)
D.��V(NaOH��Һ)=20mLʱ��c(Na+)>c(H2PO![]() )>c(H3PO4)>c(HPO
)>c(H3PO4)>c(HPO![]() )
)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com