
【题目】铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )
A.铊是易导电的银白色金属
B.能生成+3价离子化合物
C.Tl(OH)3是两性氢氧化物
D.Tl3+的氧化能力比Al3+弱
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将一定量的铁粉加入100mL稀硫酸中,为中和过量硫酸,且使Fe2+完全转化为Fe(OH)2,共消耗掉2mol·L-1NaOH溶液150mL。原硫酸溶液的浓度是
A. 0.5mol·L-1 B. 1mol·L-1 C. 1.5mol·L-1 D. 2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是放热反应的是( )
A.Ba(OH)2·8H2O与NH4Cl的反应B.铝与稀盐酸的反应
C.灼热的碳与二氧化碳的反应D.氢氧化钠与盐酸的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.下列表述中正确的是( )
A. X位于元素周期表中第二周期第IA族
B. X的单质和Y的单质相比,熔点较高的是X
C. Z的氧化物的水化物一定是强酸
D. W、X可形成X2W、X2W2离子化合物,且阴阳离子个数比均为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某主族元素R的最高正化合价与最低负化合价的代数和为4,由此可以判断( )
A.R一定是第四周期元素
B.R一定是ⅣA族元素
C.R的气态氢化物比同周期其他元素气态氢化物稳定
D.R气态氢化物化学式为H2R
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为: ![]() ,下列关于该电池工作时的说法正确的是
,下列关于该电池工作时的说法正确的是![]()

A. 该装置工作时,Ag电极上有气体生成
B. 甲池中负极反应为![]()
C. 甲池和乙池中的溶液的pH均减小
D. 当甲池中消耗![]()
![]() 时,乙池中理论上最多产生
时,乙池中理论上最多产生![]() 固体
固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝与过量的稀盐酸反应,为了加快反应速率,同时几乎不影响生成的氢气总量,不可以采取的措施是( )
A.加热,升高溶液温度
B.加入适量的水
C.加入少量CuSO4溶液
D.加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用高锰酸钾分解制氧气的反应,测定室温下的气体摩尔体积,实验装置如下。
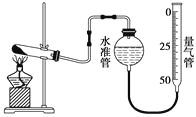
部分实验步骤:
①装好实验装置。
② 。
③把适量的高锰酸钾粉末放入干燥的试管中,准确称量试管和高锰酸钾粉末的质量为m g。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热。
⑥测量收集到的气体体积。
⑦准确称量试管和残留物的质量为n g。
⑧测量实验室的温度。
回答下列问题。
(1)实验步骤的第②步是 ________________________________________________。
(2)测量收集到的气体体积,应注意的事项有:
①_____________________________________________________________________;
②_____________________________________________________________________;
③视线与凹液面最低处相平。
(3)如果实验中得到的氧气体积是p L,水蒸气的影响忽略不计,则室温下气体摩尔体积的计算式为__________(含m、n、p)。
(4)假定其他操作均正确,未恢复至室温就读数会导致实验结果___________________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com