
����Ŀ��ij��ѧ�о���ѧϰС�������ƺ���NH4+��Cl-��K+��SO42-��ֲ������Һ450mL����Ҫ�������Һ��c(Cl-)=c(K+)=c(SO42-)=0.4mol��L1��ʵ�����ṩ��ҩƷ�У�NH4Cl��KCl��(NH4)2SO4��K2SO4������ˮ���ṩ��ʵ�������У���ҩ�ע�������ƽ���ձ��ܽ�ͷ�ιܢ���Ͳ����ش��������⣺
��1����ֲ������Һ�У�NH4+�����ʵ���Ũ��Ϊ____��
��2�����о�С�����Ƹ�ֲ������Һʱ�������õ��IJ���������____��_____��
��3�������Ƹ�����Һ��������������ȷ�������д��������ʹ��������Һ��Ũ��ƫ�͵���____��
a.����Һת��������ƿ��δϴ���ձ��Ͳ�����
b.���ձ��ڵ���Һ������ƿ��ת��ʱ������ƿ�л���������ˮ
c.���ձ��ڵ���Һ������ƿ��ת��ʱ�����������ʹ������Һ��������ƿ
d.�ý�ͷ�ι�������ƿ�м�ˮʱ����������ƿ�̶���
e.ҡ�Ⱥ���Һ���������ƿ�̶���
���𰸡�0.8mol/L 500mL����ƿ ������ ac
��������
��1��Ҫ�������Һ��c��Cl-��=c��K+��=c��SO42-��=0.4molL-1�����ݵ���غ������Һ��笠�����Ũ�ȣ�
��2���������Ʋ���ѡ����Ҫ������
��3���������������ʵ�������Һ�����Ӱ�죬����C=![]() ������������
������������
(1)������Һ��c��Cl-��=c��K+��=c��SO42-��=0.4molL-1��������Һ�е���غ���ɿ�֪��c(Cl)+2c(SO42-)=c(K+)+c(NH4+)������0.4mol/L+2��0.4mol/L=0.4mol/L+c(NH4+)����ã�c(NH4+)=0.8mol/L��
�ʴ�Ϊ��0.8mol/L��
(2)����450mL��Һ����Ҫ500mL����ƿ��������Һһ�㲽�裺���㡢����(��ȡ)���ܽ�(ϡ��)����ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵ��õ���������������ƽ(��Ͳ)��ҩ�ס��ձ�����������500mL����ƿ����ͷ�ιܣ���ȱ�ٵIJ���������500mL����ƿ����������
�ʴ�Ϊ��500mL����ƿ����������
(3)a.����Һת��������ƿ��δϴ���ձ��Ͳ��������������ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ���aѡ��
b.���ձ��ڵ���Һ������ƿ��ת��ʱ������ƿ�л���������ˮ�������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ����Ӱ�죬��b��ѡ��
c.���ձ��ڵ���Һ������ƿ��ת��ʱ�����������ʹ������Һ��������ƿ�����²���������ģ����ʵ������ƫС����ҺŨ��ƫ�ͣ���cѡ��
d.�ý�ͷ�ι�������ƿ�м�ˮʱ����������ƿ�̶��ߣ�������Һ���ƫС����ҺŨ��ƫ�ߣ���d��ѡ��
e.ҡ�Ⱥ���Һ���������ƿ�̶��ߣ�����������������ҺŨ��ȷ����e��ѡ��
��ѡ��ac��


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������;��˵��������ȷ����( )
A.ClO2����ǿ�����ԣ�����������ˮ��ɱ������
B.���ʰ����̬���ʡ���̬���ʺ�����
C.��ⷨұ����ʱ���������ʯ�ɽ��������������¶ȣ������ܺ�
D.������ͭ����ָ��ijЩϸ�������£����ÿ����е�������������ͭ��ת��Ϊͭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() ��25��ʱ��
��25��ʱ��![]() ��
��![]() �����¶�����
�����¶�����![]() ��Һ�ζ�
��Һ�ζ�![]() ��Һ�ĵζ�������ͼ��ʾ������˵������ȷ����( )
��Һ�ĵζ�������ͼ��ʾ������˵������ȷ����( )
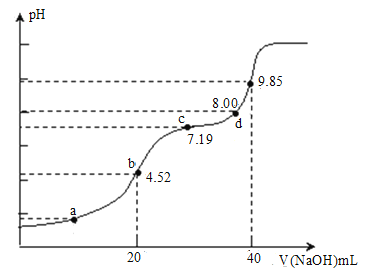
A.��a����Һc(![]() )=c(H2SO3)����a���Ӧ��
)=c(H2SO3)����a���Ӧ��![]()
B.��ѡ��bΪ��Ӧ�յ㣬��ѡ�����Ϊָʾ��
C.c���Ӧ����Һ2c(Na+)=3c(![]() )
)
D.d���Ӧ����Һc(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ܱ������з������·�Ӧ��2X(g)+Y(g) ![]() 2Z(g) ��H<0,��ͼ�DZ�ʾ�÷�Ӧ���ʣ�v)��ʱ�䣨t)�仯�Ĺ�ϵͼ��t1��t2��t5ʱ������������иı䣨����û�иı�����ʵ���������������˵������ȷ���ǣ� ��
2Z(g) ��H<0,��ͼ�DZ�ʾ�÷�Ӧ���ʣ�v)��ʱ�䣨t)�仯�Ĺ�ϵͼ��t1��t2��t5ʱ������������иı䣨����û�иı�����ʵ���������������˵������ȷ���ǣ� ��

A. t3ʱ�������¶� B. t5ʱ������ѹǿ
C. t6ʱ�̺�Ӧ���ת������� D. t4ʱ�÷�Ӧ��ƽ�ⳣ��С��t6ʱ��Ӧ��ƽ�ⳣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ����״��������������Janus���л���ṹ��ʽ����ѧ�ҽ��齫�÷��ӽ�����Janusene��������˵����ȷ����
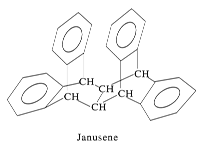
A.Janusene�ķ���ʽΪC30H20
B.Janusene���ڱ���ͬϵ��
C.Janusene�����ϵ�һ�ȴ�����8��
D.Janusene�ȿɷ���������Ӧ���ֿɷ�����ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ�й������Ĵ������ĸ���������ǵ�һ�����й����ֵ�ȫ�»�ѧ�ṹ��ҩƷ��Ҳ��Ŀǰ�ڹ����ϻ�ù㷺�Ͽɵ��й�ԭ��ҩƷ�������ѱ�����Ƿǹ���ָ��Ϊű������һ����ҩ������ű����һ�ߴ�Ⱦ�Լ�������ʷ�Ͼ�����̱����塣����Ҫ�ɷ��������أ���һ���������з���õ��ľ������ͻ�ѧ�ṹ�Ŀ�űҩ�����ṹ��ͼ��ʾ���йظû������������ȷ����( )
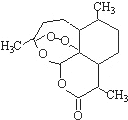
A.����ʽΪ��C16H22O5
B.�û�������һ�������²�����NaOH��Һ��Ӧ
C.�û������к��й�������һ����������������
D.��������ά����һ����ˮ���Ե�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25�桢101kPa�����£�C��s����H2��g����CH3COOH��l����ȼ���ȷֱ�Ϊ393.5kJ/mol��285.8kJ/mol��870.3kJ/mol����2C(s)+2H2(g)+O2(g)=CH3COOH(l)�ķ�Ӧ��Ϊ
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��������٤������������˵����ȷ���ǣ� ��
A.��״���£�560mL�������������Ļ�������ַ�Ӧ�ۼ���ĿΪ0.05NA
B.��״���£�2.24LCl2ͨ��NaOH��Һ�з�Ӧת�Ƶĵ�����Ϊ0.2NA
C.���³�ѹ�£�1.5molHCHO��C2H2O3�Ļ������ȫ���ȼ�գ����ĵ�O2������ĿΪ1.5NA
D.0.1mol/L��NH4Cl��Һ��ͨ���������������ԣ���ʱ��Һ��NH4+��ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᣨH2C2O4����һ�ֶ�Ԫ���ᡣ����ʱ������ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
A.0.1 mol��L1 NaHC2O4��Һ��c(Na��)��c(C2O![]() )��c(HC2O
)��c(HC2O![]() )
)
B.0.1 mol��L-1 Na2C2O4��Һ��c(OH��) = c(H��) + 2c(H2C2O4) + c(HC2O![]() )
)
C.0.1 mol��L1 H2C2O4��Һ��0.2 mol��L1 + c(OH��) = c(H��) + 2c(H2C2O4) + c(HC2O![]() )
)
D.��Na2C2O4��Һ�еμ�H2C2O4��Һ�����ԣ�c(Na��) = 2c(C2O![]() )
)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com