
【题目】向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图一所示.图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知t3~t4阶段使用了催化剂;图一中t0~t1阶段c(B)未画出.
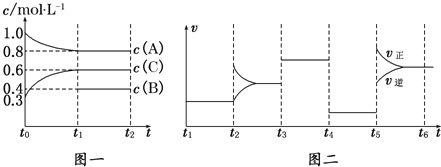
(1)若t1=15min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=______________.
(2)t4~t5阶段改变的条件为______________,B的起始物质的量为______________.
(3)判断图一中可逆反应达到平衡状态的依据是(填序号)______________.
①2v正(A)=3v逆(C)
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④A、B、C的浓度都不再发生变化
(4)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:______________.
(5)容器乙与容器甲的体积相同且保持不变,且乙容器的温度恒定为甲容器t4~t5时的温度,若要使C的平衡浓度为1.2mol/L,则在乙容器中加入1.2molA、0.6molB的同时还需要加入___________molC。
【答案】(1)0.02 mol/(L·min);
(2)减小压强;1.0 mol;(3)④;
(4)2A(g)+B(g)![]() 3C(g)△H=+200a kJ/mol;
3C(g)△H=+200a kJ/mol;
(5)5.4mol。
【解析】
试题分析:(1)15min内,以C浓度变化表示的反应速率为v(C)=(0.6mol/L0.3mol/L)÷15min=0.02 mol/(Lmin);
(2)t3~t4和t4~t5这两段平衡是不移动的,则只能是压强和催化剂影响的,因此应该推断该反应为等体积变化的反应,t3~t4的平衡比原平衡的速率要快,而t4~t5的速率又变慢,则前者应是加催化剂,因为条件只能用一次,t4~t5段为减小压强;反应过程中,反应物的浓度降低,生成物的浓度增大,结合图一可知,A为反应物,C为生成物,A的变化为0.2mol/L,C的变化量为0.3mol/L.又由于该反应为等体积变化的反应,所以B为反应物,根据化学反应的速率之比等于化学方程式前的计量系数比,该反应的方程式为2A(g)+B(g)![]() 3C(g),所以,△c(B)=1/2△n(A)=1/2×0.2mol/L=0.1mol/L,起始2molA所对应的浓度为1mol/L,则体积应是2mol÷1mol/L=2L,故B的起始物质的量为n(B)=(0.1mol/L+0.4mol/L)×2L=1mol;
3C(g),所以,△c(B)=1/2△n(A)=1/2×0.2mol/L=0.1mol/L,起始2molA所对应的浓度为1mol/L,则体积应是2mol÷1mol/L=2L,故B的起始物质的量为n(B)=(0.1mol/L+0.4mol/L)×2L=1mol;
(3)根据方程式计算,若①3v正(A)=2v逆(C),反应达到平衡,现在①2v正(A)=3v逆(C),所以反应未达到平衡状态,错误;②由于反应混合物都是气体,气体的质量不变,容器的容积也不变,所以在任何时刻混合气体的密度不变,故不能据此判断反应是否处于平衡状态,错误;③由于气体的物质的量不变,气体的质量不变,等于在任何情况下混合气体的平均相对分子质量不变,故不能据此判断反应是否处于平衡状态,错误;④若A、B、C的浓度都不再发生变化,则用任何一物质表示的正反应、逆反应速率都相等,反应处于平衡状态,正确;
(4)A的物质的量变化0.01mol,而此过程中容器与外界的热交换总量为a kJ,则反应2molA时,交换热量200akJ,而由图象可知,t5~t6阶段应为升高温度,正反应速率大于逆反应速率,平衡向正反应方向移动,则根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,所以该反应的正反应为吸热反应,所以热化学方程式为2A(g)+B(g)![]() 3C(g)△H=+200a kJ/mol;
3C(g)△H=+200a kJ/mol;
(5)反应的方程式为2A(g)+B(g)![]() 3C(g),根据方程式计算,若平衡时c(C)= 1.2mol/L,是甲的2倍,由于容器的容积不变,所以开始时气体的物质的量是甲的2倍。对于甲,若反应从正反应方向开始,其起始时等效开始状态是n(A)= 2mol +2/3×0.6mol=2.4mol,那么乙若从正反应方向开始,等效开始时n(A)=4.8mol,现在实际加入的A的物质的量是1.2molA,则1.2mol+2/3n(C)=4.8mol,解得n(C)=5.4mol。
3C(g),根据方程式计算,若平衡时c(C)= 1.2mol/L,是甲的2倍,由于容器的容积不变,所以开始时气体的物质的量是甲的2倍。对于甲,若反应从正反应方向开始,其起始时等效开始状态是n(A)= 2mol +2/3×0.6mol=2.4mol,那么乙若从正反应方向开始,等效开始时n(A)=4.8mol,现在实际加入的A的物质的量是1.2molA,则1.2mol+2/3n(C)=4.8mol,解得n(C)=5.4mol。


科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )
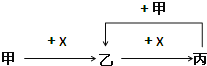
A.甲为C,X为O2 B.甲为SO2,X为NaOH溶液
C.甲为Fe,X为Cl2 D.甲为AlCl3,X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2CrO42-(黄)+2H+ =Cr2O72-(橙)+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,下列有关叙述正确的是( )

A.CrO42-生成Cr2O72-的反应为非氧化还原反应,不能通过电解方法获得
B.电源左侧是正极
C.右侧电极的电极反应为:2H2O+2e-=H2+2OH-
D.Na+从右侧通过膜进入左侧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,密闭容器中发生反应aX(g)![]() bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是( )
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是( )
A.可逆反应的化学方程式的化学计量数:a>b+c
B.压缩容器的容积时,v(正)增大,v(逆)减小
C.达到新平衡时,物质X的转化率减小
D.达到新平衡时,混合物中Z的质量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2可用作漂白剂和呼吸面具中的供氧剂。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞溶液变红是因为__________,红色褪去的可能原因是__________________。
②加入MnO2反应的化学方程式为__________________________。
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。
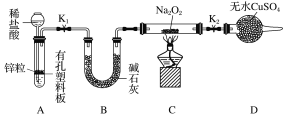
步骤1:按上图组装仪器(图中夹持仪器省略),检查气密性,装入药品。
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象。
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色。
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①添加稀盐酸的仪器名称是____________;B装置的作用是________。
②必须检验氢气纯度的原因是_____________________。
③设置装置D的目的是___________________________。
④你得到的结论是____________(若能反应请用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冰晶石(Na3 AlF6)难溶于水,广泛应用于铝的冶炼。工业上用萤石(CaF2)为原料生产Na3 AIF6:

回答下列问题:
(1)Na3AIF6为助溶剂,冶炼铝的化学方程式为 。
(2)写出煅烧时总反应的化学方程式为________。
(3)煅烧后的固体在浸取前进行粉碎的目的是____,为达到相同目的,常温浸取时还可采取的措施是____。
(4)写出向NaF溶液中加入硫酸铝溶液发生反应的离子方程式:____。NaF溶液呈碱性,用离子方程式表示其原因: ,因此在按化学计量加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,否则可能产生副产物 。
(5)97.5kg含CaF280%萤石(杂质不含氟元素)理论上可生产Na3 AIF6 kg(设生产过程中的每一步含氟物质均完全转化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关组成生物体化学元素的论述,正确的是 ( )
A. 组成生物体和组成无机自然界的化学元素中,碳元素的含量最多
B. 人、动物与植物所含的化学元素的种类差异很大
C. 组成生物体的化学元素在无机自然界都可以找到
D. 不同生物体内各种化学元素的含量比例基本相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(g)+nB(g)![]() pC(g)在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表所示:
pC(g)在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表所示:
压强/Pa | 2×105 | 5×105 | 1×106 |
c(A)/(mol·L-1) | 0.08 | 0.20 | 0.44 |
分析表中数据,回答:
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡 (填“向左”“向右”或“不”)移动,理由是 。
(2)当压强从5×105 Pa增加到1×106 Pa时,该反应的化学平衡 移动,判断的依据是 ,可能的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.放热反应在任何条件都能自发进行
B.应用盖斯定律,可计算某些难以直接测量的反应焓变
C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
D.电解精炼铜时,外电路中转移电子数为2NA个时,阳极铜质量减少64g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com