


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
| A、三氯化铝溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
| B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ |
| C、K37ClO3与浓盐酸(HCl)在加热时生成氯气:K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O |
| D、将0.1mol/L盐酸数滴缓缓滴入0.1mol/L25mLNa2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O |
| B、在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O |
| C、碳酸钠溶液中通入少量SO2:2CO32-+SO2+H2O=2HCO3-+SO32- |
| D、氧化铁溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O |
查看答案和解析>>
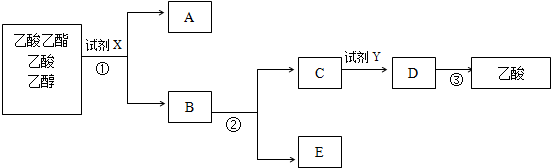
科目:高中化学 来源: 题型:
查看答案和解析>>
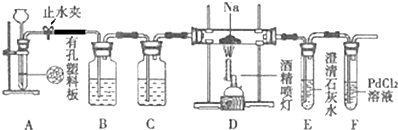
科目:高中化学 来源: 题型:
| y-x |
| 2 |
查看答案和解析>>
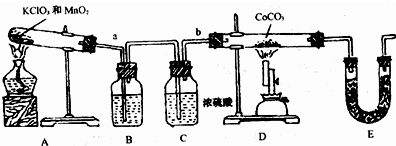
科目:高中化学 来源: 题型:
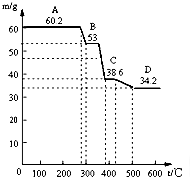 为研究水滑石的组成、结构和性质,某校研究性学习小组取得了二种牌号的水滑石样品拟进行探究,请你参与探究并回答相关问题.
为研究水滑石的组成、结构和性质,某校研究性学习小组取得了二种牌号的水滑石样品拟进行探究,请你参与探究并回答相关问题.查看答案和解析>>
科目:高中化学 来源: 题型:
 2Li0.85NiO2下列说法不正确的是( )
2Li0.85NiO2下列说法不正确的是( )| A、放电时,负极的电极反应式:Li-e-=Li+ |
| B、充电时,Li0.85NiO2既发生氧化反应又发生还原反应 |
| C、该电池不能用水溶液作为电解质 |
| D、放电过程中Li+向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 光合作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com