
【题目】亚硝酰氣(ClNO)常用作催化剂和合成洗涤剂,其沸点为-5.5℃,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,进行如下实验(夹持装置略去)。请回答:

Ⅰ.Cl2的制备
(1)Cl2的发生装置可以选择上图中的____________(填大写字母),反应的离子方程式为__________.
(2)欲收集一瓶干燥的氯气,选择上图中的装置,其连接顺序为:a![]() _____(按气流方向,用小写字母表示)。
_____(按气流方向,用小写字母表示)。
Ⅱ.亚硝酰氯(ClNO)的制备。实验室可用下图装置制备亚硝酰氯(ClNO);
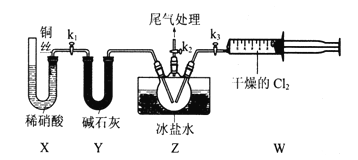
(3)实验室也可用B装置制备NO,与之相比X装置的优点为_______.
(4)在检查完装置气密性,并装入药品后,打开k2,然后再打开________(填“k1”"或“k3”),通入一段时间气体,其目的为_________。接下来,两种气体在Z中反应,当有一定量液体生成时,停止实验。
Ⅲ.亚硝酰氯(ClNO)纯度的测定
取Z中所得液体mg溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4。溶液为指示剂,用c mol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体)
(5)亚硝酰氯(ClNO)与水反应的化学方程式为___________.
(6)亚硝酰氯(ClNO)的质量分数为_________(用代数式表示即可)。
【答案】 A或B MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O或B:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O f→g→c→b→d→e→j→h 排除装置内空气的干扰;可以随开随用,随关随停 K3 排尽三颈烧瓶中的空气,防止NO和ClNO变质 2ClNO+H2O=2HCl+NO↑+NO2↑
Mn2++Cl2↑+2H2O或B:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O f→g→c→b→d→e→j→h 排除装置内空气的干扰;可以随开随用,随关随停 K3 排尽三颈烧瓶中的空气,防止NO和ClNO变质 2ClNO+H2O=2HCl+NO↑+NO2↑ ![]() (或写成
(或写成![]() )
)
【解析】(1)实验室制取氯气可以利用二氧化锰与浓盐酸加热反应生成氯化锰、氯气和水,则发生装置可以选择上图中的A;反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;也可以利用高锰酸钾与浓盐酸反应生成氯化钾、氯化锰、氯气和水,则装置可以选择上图中的B;反应的离子方程式为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;(2)制得的氯气中含有氯化氢及水蒸气,所以需要利用饱和食盐水除去氯化氢后再用浓硫酸进行干燥,然后再根据氯气的密度比空气大的性质,用向上排空气法收集,氯气是大气污染物,要进行尾气处理,可利用碱石灰作吸收剂进行尾气处理,故装置的连接顺序为a
Mn2++Cl2↑+2H2O;也可以利用高锰酸钾与浓盐酸反应生成氯化钾、氯化锰、氯气和水,则装置可以选择上图中的B;反应的离子方程式为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;(2)制得的氯气中含有氯化氢及水蒸气,所以需要利用饱和食盐水除去氯化氢后再用浓硫酸进行干燥,然后再根据氯气的密度比空气大的性质,用向上排空气法收集,氯气是大气污染物,要进行尾气处理,可利用碱石灰作吸收剂进行尾气处理,故装置的连接顺序为a![]() f→g→c→b→d→e→j→h;(3)实验室也可用B装置制备NO,与之相比X装置的优点为排除装置内空气的干扰;可以随开随用,随关随停;(4)在检查完装置气密性,并装入药品后,打开k2,然后再打开k3,通入一段时间气体,其目的为排尽三颈烧瓶中的空气,防止NO和ClNO变质;(5)亚硝酰氯(ClNO)与水反应生成盐酸、一氧化氮和二氧化氮,反应的化学方程式为2ClNO+H2O=2HCl+NO↑+NO2↑;(6)取Z中所得液体mg溶于水, 25.00mL溶液中n(ClNO)=n(Cl-)=n(Ag+)=c mol/L
f→g→c→b→d→e→j→h;(3)实验室也可用B装置制备NO,与之相比X装置的优点为排除装置内空气的干扰;可以随开随用,随关随停;(4)在检查完装置气密性,并装入药品后,打开k2,然后再打开k3,通入一段时间气体,其目的为排尽三颈烧瓶中的空气,防止NO和ClNO变质;(5)亚硝酰氯(ClNO)与水反应生成盐酸、一氧化氮和二氧化氮,反应的化学方程式为2ClNO+H2O=2HCl+NO↑+NO2↑;(6)取Z中所得液体mg溶于水, 25.00mL溶液中n(ClNO)=n(Cl-)=n(Ag+)=c mol/L![]() 22.50mL
22.50mL![]() 10-3L/mL=0.0225cmol,亚硝酰氯(ClNO)的质量分数为
10-3L/mL=0.0225cmol,亚硝酰氯(ClNO)的质量分数为![]() 。
。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
熔点/℃ | 69 | 25 | 193 | 304 | 714 |
在TiCl4中的溶解性 | 互溶 | —— | 微溶 | 难溶 | |
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) 2C(s)+O2(g)=2CO(g)
① 沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的化学方程式:________________
② 氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是_____________________。
③ 氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有_____________
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:
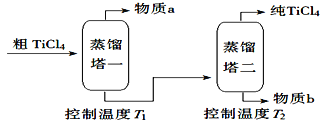
物质a是_________,T2应控制在_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富马酸(反式丁烯二酸)可用于制备聚酯树脂、医药等。实验室以石油的裂解产物之一A为原料制备富马酸及其衍生物的一种工艺路线如下:
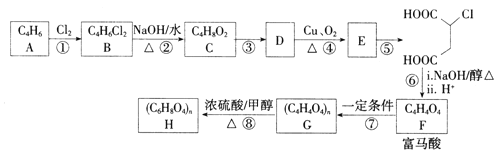
已知:链烃A的核磁共振氢谱中有2组吸收峰。
(1)A的化学名称为________,B的结构简式为__________。
(2)③的反应类型为________.检验E中含氧官能团所用的试剂为___________。
(3)反应④的化学方程式为___________。
(4)反应⑧的化学方程式为______________。
(5)富马酸的同分异构体中,同为二元羧酸的还有__________(包括顺反异构)。
(6)已知: 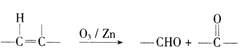 ,参照上述合成路线,以
,参照上述合成路线,以![]() 为原料( 无机试剂任选).设计制备
为原料( 无机试剂任选).设计制备![]() 的合成路线:_____________________。
的合成路线:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于SO2性质的说法中,不正确的是( )
A.能使酸性KMnO4溶液褪色
B.能使品红溶液褪色
C.能与NaOH溶液反应
D.能与水反应生成硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是( )




①除去CO2中HCl ②吸收Cl2 ③检查装置气密性 ④利用排空气法收集CO2
A. ①④ B. ②④ C. ②③ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质,在室温下A为固体,B和C为气体,向D溶液中加入KSCN溶液后,溶液显红色。在适宜的条件下可发生如下关系的化学反应。
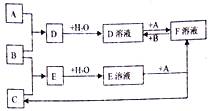
回答以下问题:
(1)写出B的化学式:____________
(2)写出E溶液和+A→F溶液+C的离子反应方程式:___________________。D溶液和+A→F溶液的离子反应方程式:_______________________________。若向F溶液中加入NaOH溶液,观察到的现象为:________________________。
(3)写出除去D溶液中F杂质的离子反应方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时, Ksp (AgCl)= 1.56×10-10, Ksp(Ag2CrO4)= 9.0×10-12,下列说法正确的是
A. AgCl 和 Ag2CrO4 共存的悬浊液中,![]()
B. 向Ag2CrO4悬浊液中加入 NaCl 浓溶液, Ag2CrO4不可能转化为 AgCl
C. 向 AgCl 饱和溶液中加入 NaCl 晶体, 有 AgC1 析出且溶液中 c(Cl-)=c(Ag+)
D. 向同浓度的 Na2CrO4和 NaCl 混合溶液中滴加 AgNO3溶液,AgC1先析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时红磷比白磷稳定,在下列反应中:
4P(白磷,s)+5O2(g)====2P2O5(s);△H=== -a kJ/mol
4P(红磷,s)+5O2(g)====2P2O5(s);△H=== -b kJ/mol
若a、b均大于零,则a和b的关系为
A.a<bB.a=bC.a>bD.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com