
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法错误的是

A. 该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管
B. 取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸
C. 配制200mL4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol·L-1
【答案】B
【解析】
A.98![]() 的硫酸为浓硫酸,具有强腐蚀性,属于危险药品,在实验室中应妥善保管,所以A选项是正确的;B.用浓硫酸配制稀硫酸时,要把浓硫酸沿烧杯壁缓缓加入水中,边加边搅拌。若把水加入浓硫酸中,由于浓硫酸遇水放出大量的热引起液体飞溅,会出现安全事故,且所配硫酸的质量分数不等于
的硫酸为浓硫酸,具有强腐蚀性,属于危险药品,在实验室中应妥善保管,所以A选项是正确的;B.用浓硫酸配制稀硫酸时,要把浓硫酸沿烧杯壁缓缓加入水中,边加边搅拌。若把水加入浓硫酸中,由于浓硫酸遇水放出大量的热引起液体飞溅,会出现安全事故,且所配硫酸的质量分数不等于![]() ,故B错误;C.该浓硫酸的物质的量浓度为c=1000
,故B错误;C.该浓硫酸的物质的量浓度为c=1000![]() /M=1000
/M=1000![]() 1.84g/L
1.84g/L![]() 98
98![]() =18.4mol/L,计算根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则xmL/1000
=18.4mol/L,计算根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则xmL/1000![]() =200ml
=200ml![]() 4.6mol/L,计算得出:x=50,所以应量取的浓硫酸体积是50mL,所以C选项是正确的;D.该硫酸与等质量的水混合,因为硫酸密度大于水的密度,等质量混合时总体积大于硫酸体积的2倍,则所得溶液的物质的量浓度小于9.2mol.L-1 ,所以D选项是正确的;所以答案为B。
4.6mol/L,计算得出:x=50,所以应量取的浓硫酸体积是50mL,所以C选项是正确的;D.该硫酸与等质量的水混合,因为硫酸密度大于水的密度,等质量混合时总体积大于硫酸体积的2倍,则所得溶液的物质的量浓度小于9.2mol.L-1 ,所以D选项是正确的;所以答案为B。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
①0.1mol·L-1 氨水中,c(OH-)=c(NH 4+)
②10mL 0.02mol·L-1 HCl 溶液与 10mL0.02mol·L-1Ba(OH)2 溶液充分混合,若混合后溶液的体积为 20mL,则溶液的 pH=12
③在 0.1mol·L-1 CH COONa 溶液中,c(OH-)=c(CH COOH)+c(H+)
④0.1mol·L-1 某二元弱酸酸式盐 NaHA 溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H A)
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组欲探究Cl2与KI溶液的反应,设计实验装置如图。

已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大,其原因为I2(s)+I-(aq)![]() I3-(aq)
I3-(aq)
完成下列填空:
(1)仪器A使用前必须进行的操作是___________,仪器B的名称是___________。
(2)该实验设计装置存在明显缺陷是___________,改进之后,进行后续实验。
(3)C中的试剂是___________;当E装置中出现___________时,停止加热。
(4)当氯气开始进入D时,D中看到的现象是____________;不断向D中通入氯气,看到溶液颜色逐渐加深,后来出现深褐色沉淀,试运用平衡移动原理分析产生这些现象的原因_____。
(5)持续不断地向D中通入氯气,看到D中液体逐渐澄清,最终呈无色。实验小组猜想,D中无色溶液里的含碘物质可能是HIO3。
①按照实验小组的猜想,用化学方程式解释“D中液体逐渐澄清,最终呈无色”的原因_____。
②为了验证猜想是否正确,实验小组又进行如下实验:
ⅰ.取反应后D中溶液5.00mL(均匀)于锥形瓶中,加入KI(过量)和足量稀硫酸。
ⅱ.向上述锥形瓶中滴加淀粉指示剂,溶液变蓝,用0.6250mol/L的Na2S2O3溶液滴定至蓝色刚好褪去,消耗Na2S2O3溶液VmL。
已知:2HIO3+10KI+5H2SO4=6I2+5K2SO4+6H2O、I2+2S2O32-=2I-+S2O62-,若V=___________时,说明实验小组的猜想正确。
(6)欲检验某溶液中是否含有I-,可使用的试剂为溴水和四氯化碳。合理的实验操作为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.2kJ/mol
2NH3(g) ΔH=-92.2kJ/mol
(1)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_____________。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
(2)L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。

ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由:______。
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:

① 电极b上发生的是______反应(填“氧化”或“还原”)
② 写出电极a的电极反应式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟氨(NH2OH)为一元弱碱(25℃时,平衡常数Kb=9.0×10-9),其电离方程式为:NH2OH+H2ONH3OH++OH-。在25℃时,用0.10mol·L-1盐酸滴定20mL0.10mol·L-1NH2OH溶液,滴定过程中由水电离出来的H+浓度的负对数[-1gc水(H+)]与盐酸体积(V)的关系如图所示。(已知:lg3=0.5),下列说法中错误的是

A. a点对应溶液的pH=9.5
B. b点对应的溶液中有:c(NH3OH+)=c(Cl-)
C. c点溶液中存在离子反应:![]()
D. d点溶液中:-lgc水(H+)=13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S,已知甲池中发生的反应:


下列说法正确的是( )
A. 甲池中碳棒上发生的电极反应为AQ+2H+-2e-=H2AQ
B. 乙池溶液中发生的反应为H2S+I3-=3I-+S+2H+
C. 该装置中电能转化为光能
D. H+从甲池移向乙池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.2kJ/mol
2NH3(g) ΔH=-92.2kJ/mol
(1)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_____________。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
(2)L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。

ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由:______。
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
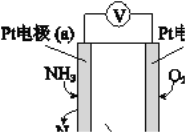
① 电极b上发生的是______反应(填“氧化”或“还原”)
② 写出电极a的电极反应式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。化合物XW3能作制冷剂且其浓溶液可检验Z单质是否泄露,化合物YZ3能促进水的电离,则下列说法错误的是
A. 简单离子半径:r(Z)>r(X)>r(Y)B. Y的最高价氧化物对应的水化物为强碱
C. X2W4分子中既含极性键,又含非极性键D. 化合物XW3的水溶液能抑制水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5,表示,咸水中的主要溶质为NaCl。下列有关说法正确的是

A. a为原电池的负极
B. b电极附近溶液的pH减小
C. a电极反应式为![]()
D. 中间室:Na+移向左室,Cl-移向右室
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com