
【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.2kJ/mol
2NH3(g) ΔH=-92.2kJ/mol
(1)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_____________。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
(2)L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。

ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由:______。
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:

① 电极b上发生的是______反应(填“氧化”或“还原”)
② 写出电极a的电极反应式:_________。
【答案】K= ![]() 逆向 减小 温度 L2﹥L1,其他条件相同时,增大压强有利于平衡向气体体积缩小的方向移动,从而提高H2(g)的平衡转化率 。 还原 2NH3-6e-+6OH- = N2+6H2O
逆向 减小 温度 L2﹥L1,其他条件相同时,增大压强有利于平衡向气体体积缩小的方向移动,从而提高H2(g)的平衡转化率 。 还原 2NH3-6e-+6OH- = N2+6H2O
【解析】
(1)根据平衡常数表达式
(1)① N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
起始浓度(mol/L) 1 3 0
转化浓度(mol/L) 0.4 1.2 0.8
平衡浓度(mol/L) 0.6 1.8 0.8
因为合成氨反应的平衡常数=生成物浓度的幂次方之积比上反应物浓度的幂次方之积,所以N2(g)+3H2(g)![]() 2NH3(g)的平衡常数表达式为K=c2(NH3)/c(N2)c3(H2)=0.82/(1.82×0.6),故答案为:K=0.82/(1.82×0.6)。
2NH3(g)的平衡常数表达式为K=c2(NH3)/c(N2)c3(H2)=0.82/(1.82×0.6),故答案为:K=0.82/(1.82×0.6)。
②按投料Ⅱ将氨气完全转化到右边,则与投料Ⅰ完全相同,为完全等效平衡,所以按投料Ⅱ进行反应,起始时反应进行的方向为逆向,故答案为:逆向。
③由题可知,合成氨为放热反应,所以升高温度平衡向逆反应方向移动,所以反应的化学平衡常数变小,故答案为:减小。
(2)i.由图可知,X越大,氢气转化率越低,升高温度平衡向逆反应方向移动,则氢气转化率减小,则X表示温度,故答案为:温度。
ii.由N2(g)+3H2(g)2NH3(g)△H<0,温度高,氢气转化率小,压强大,平衡正向移动,氢气转化率大,图中等温度时L2对应的氢气转化率大,则压强L1<L2,故答案为:L1<L2;其他条件相同时,增大压强有利于平衡向气体体积缩小的方向移动,从而提高H2(g)的平衡转化率。
(3)①Pt电子通入氨气生成氮气,说明氨气被氧化,为原电池负极,则b为正极,氧气得电子被还原发生还原反应,故答案为:还原。
②因为a极为负极,负极是氨气发生氧化反应变成氮气,且OH﹣向a极移动参与反应,故电极反应式为2NH3﹣6e﹣+6OH﹣=N2+6H2O,故答案为:2NH3﹣6e﹣+6OH﹣=N2+6H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】用Li和石墨的复合材料以及纳米Fe2O3材料作电极的锂离子电池,在循环充放电过程中可实现对磁性的可逆调控(如图)。下列有关说法一定错误的是
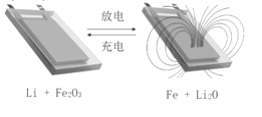
A. 该电池的电解质溶液可以是硫酸溶液
B. 放电时,总反应式是6Li+Fe2O3=3Li2O+2Fe
C. 充电时,阳极的电极反应是2Fe+3Li2O-6e-= Fe2O3+6Li+
D. 充放电过程中,电池可在被磁铁不吸引和吸引之间循环调控
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Ba2+、CO32-、Cl-、SO42-。现取两份200mL溶液分别进行如下实验:
①第一份加足量NaOH溶液,加热,收集到气体1.36g;
②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,以下推测正确的是( )
A.一定存在NH4+、CO32-、SO42-,一定不存在Ba2+、Cl-
B.一定存在NH4+、CO32-、Cl-、SO42-,可能存在K+
C.c(SO42-)=0.2mol/L,c(NH4+)>c(SO42-)
D.若溶液中存在K+、NH4+、CO32-、Cl-、SO42-五种离子,则c(K+)>0.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
以芳香烃A为原料制备某重要医药中间体F的合成路线如下:
![]()
试回答下列问题:
(1)B的化学名称为___________。
(2)F中所含官能团的名称为___________。
(3)由A生成B和由D生成E的反应类型分别是___________、___________。
(4)已知G的分子式为C4H9Br2N,在一定条件下C与G反应生成 ,写出该反应的化学方程式___________。
,写出该反应的化学方程式___________。
(5)写出同时满足下列条件的D的两种同分异构体的结构简式___________、___________。
①含有苯环,且分子中含有4种不同化学环境的氢;
②既能与盐酸反应,又能发生银镜反应。
(6)请以![]() 、(CH3)2SO4、CH3CH2OH为原料,结合本题信息和流程图中的图例,写出制备
、(CH3)2SO4、CH3CH2OH为原料,结合本题信息和流程图中的图例,写出制备![]() 的合成路线流程图(其它无机试剂任选)。
的合成路线流程图(其它无机试剂任选)。
_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是

A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C. 点④所示溶液液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是重要的有机合成中间体,其一种合成路线如下:
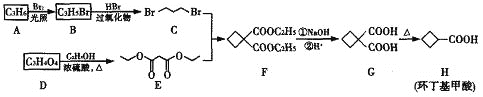
请回答下列问题:
(1)环丁基甲酸的分子式为____________________。
(2)环丁基甲酸由原料A和D经一系列反应制得,A为烯烃,则A的名称为______,D物质的官能团为_______。
(3)写出D→E的化学方程式________________________。
(4)C+E→F的反应类型为_________________________。
(5)化合物W为H的同分异构体,能发生银镜反应且只含酯基一种官能团,则所有符合条件的W的结构简式为_____________。
(6)参照上述合成路线,以 ![]() 和E为原料(无机试剂任选),设计制备
和E为原料(无机试剂任选),设计制备![]() 的合成路线:__________。
的合成路线:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法错误的是

A. 该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管
B. 取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸
C. 配制200mL4.6 mol·L-1的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示:

已知:①菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。
②Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③焙烧过程中主要反应为MnCO3+2NH4Cl ![]() MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。
(1)结合图1、2、3,分析焙烧过程中最佳的焙烧温度、焙烧时间、m(NH4Cl)/m(菱锰矿粉)分别为____________、____________、____________。

(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围__,将Fe3+和Al3+变为沉淀而除去,然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为____。
(4)上述流程中可循环使用的物质是________。
(5)现用滴定法测定浸出液中Mn2+的含量。实验步骤:称取1.000 g试样,向其中加入稍过量的磷酸和硝酸,加热使反应2Mn2++NO3-+4PO43-+2H+![]() 2[Mn(PO4)2]3-+NO2-+H2O充分进行并除去多余的硝酸;加入稍过量的硫酸铵,发生反应NO2-+NH4+===N2↑+2H2O以除去NO2-;加入稀硫酸酸化,用2.00 mol·L-110.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3-+Fe2+===Mn2++Fe3++2PO43-;用0.10 mol·L-110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
2[Mn(PO4)2]3-+NO2-+H2O充分进行并除去多余的硝酸;加入稍过量的硫酸铵,发生反应NO2-+NH4+===N2↑+2H2O以除去NO2-;加入稀硫酸酸化,用2.00 mol·L-110.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3-+Fe2+===Mn2++Fe3++2PO43-;用0.10 mol·L-110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应(还原产物是Cr3+)的离子方程式为___________。
②试样中锰的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应3A(g)+2B(g) ![]() zC(g)+2D(g),在2 L 的密闭容器中把4 mol A 和 2 mol B 混合,2 min 后反应达到平衡时生成 1.6 mol C,又测得反应速率v(D)=0.2 mol·(L·min) -1 。则下列说法不正确的是
zC(g)+2D(g),在2 L 的密闭容器中把4 mol A 和 2 mol B 混合,2 min 后反应达到平衡时生成 1.6 mol C,又测得反应速率v(D)=0.2 mol·(L·min) -1 。则下列说法不正确的是
A. z=4 B. B 的转化率是40%
C. A 的平衡浓度是1.4 mol·L-1 D. 平衡时气体压强是原来压强的0.9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com