
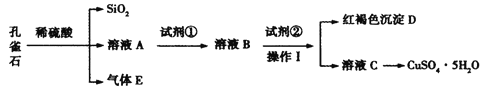
����Ŀ����ȸʯ��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ����ij�����Կ�ȸʯΪ��Ҫԭ���Ʊ�CuSO4��5H2O����Ҫ�������£�
��֪�������£�ͨ��������Һ������Զ�ʹ Fe3+��Fe2+��Cu2+���ɳ����� pH �ֱ����£�
���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
Fe��OH��3 | 2.2 | 3.2 |
Fe��OH��2 | 7.6 | 9.6 |
Cu��OH��2 | 4.7 | 6.4 |
��ش��������⣺
��1��Ϊ����߿�ȸʯ���ʱ�����ʣ����ʵ�����Ũ����Ũ���⣬�����Բ�ȡ�Ĵ�ʩ��:___(дһ��)��
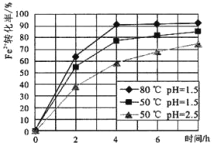
��2���Լ�����˫��ˮ���� Fe2+������ Fe3+��Ŀ����___��������ͼ�й����ݣ�����Ϊ��ҵ����������ʱӦ��ȡ��������___��
��3���Լ���ΪCuO����Ŀ���ǵ�����Һ�� pH ������___��Χ���������������___��
��4����Һ C �õ�CuSO4��5H2O����Ҫ������___��___�����ˡ�ϴ�ӡ����
���𰸡��ʵ���߷�Ӧ�¶�(����衢����ʯ��ĥ�ɷ�ĩ�����������Ȱ�) ����pHʱ, Fe3+��Cu2+��ʼ����֮ǰ���ܳ�����ȫ���Զ������ʿ��ȥ �¶ȿ�����80C��pH������1.5,����ʱ��Ϊ4h���� 3.2��pH<4.7 ���� ����Ũ�� ��ȴ�ᾧ
��������
��ȸʯ��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ�������ȸʯ�м�������ϡ���ᣬ�����ķ�Ӧ��Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2����Fe+ H2SO4=FeSO4+H2�������ϡ�����Ӧ����ҺAֻ��Cu2+��Fe2+���ֽ������ӣ�Ȼ����˵õ��������к���Si���������ҺA�к��к������κ������μ�����ͭ������ҺA�м����Լ���˫��ˮ�õ���ҺB��˫��ˮ��һ������������Fe2+ת��ΪFe3+������ҺB�м����Լ���CuO����������õ���ҺC�ͺ��ɫ����D���������Ϊ���ˣ�DΪFe(OH)3���Լ��������Լ�����ҺCΪ����ͭ��Һ���ݴ˴��⡣
��1��Ϊ����߿�ȸʯ���ʱ�����ʣ����Բ�ȡ�Ĵ�ʩ��: �ʵ���߷�Ӧ�¶�(����衢����ʯ��ĥ�ɷ�ĩ�����������Ȱ�)��
��ˣ�������ȷ���ǣ��ʵ���߷�Ӧ�¶�(����衢����ʯ��ĥ�ɷ�ĩ�����������Ȱ�)��
��2���Լ�����˫��ˮ���� Fe2+������ Fe3+��Ŀ���ǵ���pHʱ, Fe3+��Cu2+��ʼ����֮ǰ���ܳ�����ȫ���Զ������ʳ�ȥ��
����ͼ���֪����80��pH����1.5ʱת������ߣ�����Ӧ�ÿ��Ƶ�����������Һ�¶ȿ�����80�棬pH������1.5������ʱ��Ϊ4Сʱ���ҡ�
��ˣ�������ȷ���ǣ��¶ȿ�����80C��pH������1.5,����ʱ��Ϊ4h���ң�
��3������ҺB�м�CuO������Һ��pHʹFe3+��ȫ��������Cu2+�����������ݱ������ݣ�Ӧ������Һ�� pH ������3.2��pH<4.7��Χ������ҺB�м���CuO����������õ���ҺC�ͺ��ɫ����D���������Ϊ���ˣ�
��ˣ�������ȷ���ǣ����ˣ�
��4����ҺCΪ����ͭ��Һ��������ͭ��Һ�õ�CuSO4��5H2O����Ҫ����������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��ˣ�������ȷ���ǣ�����Ũ������ȴ�ᾧ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ����![]() �ζ�
�ζ�![]() ijһԪ��HX,�ζ�������pH�仯������ͼ��ʾ��
ijһԪ��HX,�ζ�������pH�仯������ͼ��ʾ��

����˵����ȷ����
A. HX��Һ�����Ե�ԭ����![]()
B. ��a��![]()
C. ��b��![]() ��
��![]() ǡ����ȫ��Ӧ
ǡ����ȫ��Ӧ
D. ��c��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������˵����ȷ���ǣ� ��
A.1 mol��������2NA����ԭ��B.14 g�����к�6.02��1023��������
C.���³�ѹ�£�32gO3���е�ԭ����Ϊ2NAD.18 gˮ�������ĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na2CO3��NaHCO3�������Һ����μ���ϡ���ᣬ�����������������������ı仯��ϵ��ͼ��ʾ���������������ڶ�Ӧ����Һ��һ���ܴ����������
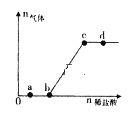
A. a���Ӧ����Һ�У�Na+��OH-��SO42-��NO3-
B. b���Ӧ����Һ�У�Al3+��Fe3+��MnO4-��Cl-
C. c���Ӧ����Һ�У�Na+��Ca2+��NO3-��Cl-
D. d���Ӧ����Һ�У�F-��NO3-��Fe2+��Ag+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ڳİ�ֽ�IJ���Ƭ�������������KMnO4����������Χ�ֱ�μ�һ�κ��з�̪�ij���ʯ��ˮ��FeCl2��Һ��Ȼ����KMnO4�����ϵμ�������Ũ���ᣬѸ�ٸǺñ�������ʾ��ʵ���������õ�������������������ԭ����ȡ��2KMnO4��16HCl��Ũ��=2KCl��2MnCl2��5Cl2����8H2O���˷�Ӧ�ڳ����¼��ܽ��С�
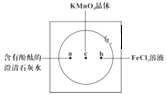
��1��Ũ�����ڷ�Ӧ�б��ֳ�����������______ ����д��ţ����������뻹ԭ�����ʵ���֮��Ϊ______ ����������Ϊ______ ��
��ֻ�л�ԭ�� ����ԭ�Ժ�����
��ֻ�������� �������Ժ�����
��2������0.1 mol Cl2����ת�Ƶ��ӵ����ʵ���Ϊ ______ mol��
��3��a����Ӧ�Ļ�ѧ����ʽ��___________________________����ҵ���ô�ԭ����ȡƯ�ۡ�
��4��b�����ӷ���ʽ��________________________��
��5��������ر���Һ���������ζ��������ʵĺ������ø�����ط���Ӳⶨʯ��ʯ��CaCO3�ĺ����ķ���Ϊ:��ȡ����0.1250g����ϡ�����ܽ�����(NH4)2C2O4��CaC2O4����������������ϴ�Ӻ�����ϡ�����С��ζ����ɵ�H2C2O4��ȥŨ��Ϊ0.016mo/LKMnO4��Һ25.00mL��
��д��CaC2O4�����ܽ�����ӷ���ʽ:___________________
����ƽ��������и�����صζ����ᷴӦ�����ӷ���ʽ: ____MnO4-+___H2C2O4+____=___Mn2++___CO2��+____
��ʯ��ʯ��CaCO3�İٷֺ���:_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ﵽʵ��Ŀ�ģ��Լ��������������ȷ���ǣ� ��
ѡ�� | ʵ��Ŀ�� | �Լ������������ |
A | �ⶨ�к��� | ѡ��Ũ������NaOH��Һ��Ϊ�Լ� |
B | �Ƚ�Cl��S�ķǽ����� | ��������� |
C | �Ʊ������������� | ���Ȼ���������Һ�����ˮ�У����ȵ����ɫ |
D | ��ⷨ��ȡ���� | ������������ⱥ��ʳ��ˮ |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����ͬ�¶��£���������͢��зֱ��������ʵ�����HI��������Ӧ2HI(g) ![]() H2��g��+I2(g)�����й��ڷ�Ӧ��ʼʱ������͢��л���ӵ�˵������ȷ����( )
H2��g��+I2(g)�����й��ڷ�Ӧ��ʼʱ������͢��л���ӵ�˵������ȷ����( )
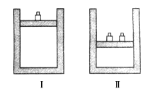
A. ��͢��л��������ͬ
B. ��͢��л���Ӱٷ�����ͬ
C. ��͢��е�λ����ڻ���������
D. ���л�ѧ��Ӧ���ʱȢ��е�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о��������ḻ�� CO2 ������Ϊ��̼Դ�������ǰӦ����㷺��̼Դ��ʯ�ͺ���Ȼ�����ݽ�Σ����ͬʱ�ֿɻ����� CO2�ۻ�������������ЧӦ��ʵ�� CO2������ѭ����
(1)Ŀǰ��ҵ����һ�ַ�������CO2����ϳɵ�̼ϩ�������Ժϳ���ϩ(C2H4)Ϊ�����ù��̷���������:
��һ����CO2��g��+H2��g��![]() CO��g��+H2O��g����H=+41.3kJ/mol
CO��g��+H2O��g����H=+41.3kJ/mol
�ڶ�����2CO��g��+4H2��g��![]() C2H4��g��+2H2O��g����H=-210.5kJ/mol
C2H4��g��+2H2O��g����H=-210.5kJ/mol
��CO2����ϳ���ϩ���Ȼ�ѧ����ʽΪ___��
��һ�������µ��ܱ������У�������Ӧ�ﵽƽ���Ҫ�ӿ췴Ӧ���ʲ���� CO2 ��ת���ʣ����Բ�ȡ�Ĵ�ʩ��___(����ĸ)��
A.��Сѹǿ B.���� H2Ũ�� C.������ʵĴ��� D.�����ˮ����
(2)��һ�ַ����ǽ� CO2 �� H2 �� 230��������������ɼ״�������ˮ�������ڲ�ͬ�����²��ƽ��ʱ�״������ʵ������¶ȡ�ѹǿ�ı仯��ͼ��ʾ������ 10L �����ܱ�������Ͷ��1molCO2 �� 2.75molH2��������Ӧ: CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g����
CH3OH��g��+H2O��g����
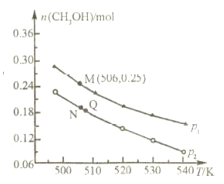
�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����___(����ĸ)��
A.c(H2):c(CH3OH)=3:1
B.����������������������ٸı�
C.������������ܶȲ��ٸı�
D.������ѹǿ���ٸı�
��������Ӧ�ġ�H___0(�>����<��)��ͼ��ѹǿ p1 ___p2(�>����<��)��
�۾��ⶨ֪ Q ��ʱ������ѹǿ�Ƿ�Ӧǰѹǿ�� 9/10���� Q �� CO2��ת����Ϊ___��
��M ��ʱ���÷�Ӧ��ƽ�ⳣ�� K=___ (������������λС��)��
(3)����ʯ������ CO2 ���������ܵ���� CaCO3�����ܶȻ����� Ksp=2.8��10-9������һ���ʵ���Ũ��Ϊ2��10-4mol/L ������Һ�������������� CaCl2��Һ��ϣ������ɳ������� CaCl2��Һ����СŨ��Ϊ___mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���ڱ������������Һ���ζ�NaOH��Һ�����в�����
������Һ�м���1��2��ָʾ��
��ȡ20.00 mL����Һ������ƿ��
����NaOH��Һ�ζ����յ�(�յ�ʱ��Һ��pHԼΪ9.1)
���ظ����ϲ���
������ƽ��ȷ��ȡһ�������ڱ���������ع������250 mL����Һ(���pHԼΪ4.2)
����ʵ�����ݼ���NaOH�����ʵ���Ũ��
(1)���ϸ����У���ȷ��(�����)����˳����________����������ʹ�õ���������ƿ�⣬����Ҫʹ�õ�������________��ѡ��ָʾ����________��
(2)�ζ�������¼NaOH���ն������ظ��ζ����Σ����ݼ�¼���±���

ijͬѧ�ڴ������ݹ����м���õ�ƽ������NaOH��Һ�����ΪV(NaOH)��(19.98+20.00+20.80+20.02)/4mL��20.20mL�����ļ��������������__________��
(3)��������ڹ۲�ζ��ܵ���ʼ����ʱ��Ҫʹ�ζ��ܵļ��첿�ֳ�����Һ������ζ����ڲ������ݣ��������ݵIJ���__________���ζ�ǰ������ˮϴ����ʽ�ζ��ܣ�Ȼ���NaOH��Һ���еζ����˲�����ʵ����________(�ƫ����ƫС������Ӱ�족)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com