
【题目】在一定条件下,对于反应mA(g)+nB(g) ![]() cC(g)+dD(g),C物质的含量(c%)与温度、压强的关系如图所示,下列判断正确的是
cC(g)+dD(g),C物质的含量(c%)与温度、压强的关系如图所示,下列判断正确的是

A.ΔH<0 ΔS>0 B.ΔH>0 ΔS<0
C.H>0 ΔS>0 D.H<0 ΔS<0
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示。下列有关说法正确的是
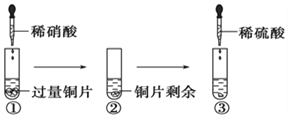
A.①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO2
B.③中反应的化学方程式:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
C.③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
D.由上述实验可知:Cu在常温下既可与稀硝酸反应,也可与稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中含有NA个氯化氢分子的是
A. 将lmol H2和1molCl2光照或点燃后的产物
B. 6.02×1023个HCl气体分子
C. 室温下,将1molHCl气体通入100mL水中所得溶液
D. 室温下,73gHCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中生成物总能量高于反应物总能量的是
A.氢氧化钠溶液与稀硫酸混合 B.异丁醇燃烧
C.氢氧化钡晶体与氯化铵晶体混合搅拌 D.氧化钙溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ/mol表示。请认真观察下图,然后回答问题。

(1)图中反应___________(填“需要”或“不需要”)环境先提供能量,该反应的△H=_________(用含E1、E2的代数式表示)。
(2)对于同一反应,图中虚线(II)与实线(I)相比,活化能________,因此反应速率________,你认为改变的条件是__________。
(3)已知常温下拆开1molH-H键,1molN-H键,lmolN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向容积固定为2L的密闭容器中充入9.6mol NO和4.8molO2,发生如下反应:
①2NO(g)+O2(g)![]() 2NO2(g) △H<0
2NO2(g) △H<0
②2NO2(g)![]() N2O4(g) △H<0
N2O4(g) △H<0
测得反应达到平衡时NO2浓度为1.2 mol/L,N2O4的浓度为0.8 mol/L。则反应①的化学平衡常数为( )
A. 0.24 B.0.36 C.1.44 D.l.96
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、(1)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式:____________________;:如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式为:______________________
(2)有一包白色粉末,其中可能含有NaCI、Ba(NO3)2、CuSO4、Na2CO3,现做以下实验:
① 将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
② 向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③ 取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中一定含有的物质是_____________,可能含有的物质是__________(以上物质均写化学式),写出第①步中反应的化学方程式为__________________第②步反应中离子方程式为____________________
II、根据反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,回答下列问题:
(1)还原产物是__________
(2)氧化剂与还原剂的物质的量之比是____________
(3)用双线桥标上电子转移的方向和数目_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俄罗斯用“质子﹣M”号运载火箭成功将“光线”号卫星送入预定轨道。发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂,已知:
(1)H2(g)=H2(l)△H1=﹣0.92kJmol﹣1
(2)O2(g)=O2(l)△H2=﹣6.84kJmol﹣1
(3)如图:下列说法正确的是( )
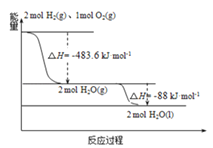
A. 2mol H2(g)与1mol O2(g)所具有的总能量比2molH2O(g)所具有的总能量低
B. 氢气的燃烧热为△H=﹣241.8 kJmol﹣1
C. 火箭液氢燃烧的热化学方程式2H2(l)+O2(l)═2H2O(g)△H=﹣474.92kJmol﹣1
D. H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com