
【题目】下列物质中,能导电的电解质是( )
A. 铝丝 B. 熔融的MgCl2 C. NaCl溶液 D. 酒精
科目:高中化学 来源: 题型:
【题目】通过图像分析影响化学平衡移动的因素,某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g) 2SO3(g) ΔH<0的正、逆反应速率的影响如图所示:

①加催化剂对反应速率影响的图像是___(填字母,下同),平衡____移动。
②升高温度对反应速率影响的图像是___,平衡向____方向(填“正反应”或“逆反应”,下同)移动。
③增大反应容器体积对反应速率影响的图像是___,平衡向____方向移动。
④增大O2的浓度对反应速率影响的图像是___,平衡向____方向移动。
⑤上述①到④中的外界条件,使得单位体积内活化分子百分数增大的是___(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。其中X、Y、Z都为气体,反应在t1min时到达平衡,如图所示,下列说法正确的是( )

A. 该反应的化学方程式是2X=3Y+Z
B. 已知1molX完全反应要吸收46kJ的热量,则至t1min时,该反应吸收的热量为36.8kJ·mol-1
C. 在此t1min时间内,用Y表示反应的平均速率v(Y)为0.6mol/(L·min)
D. 在相同状态下,反应前的压强是反应后的0.75倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)
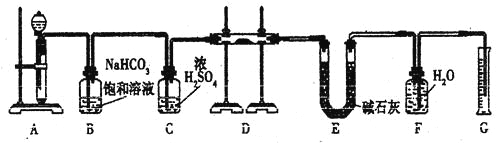
回答下列问题:
(1)装置A中液体试剂选用 ,理由是 。
(2)装置B的作用是 。
装置C的作用是 。
装置E中碱石灰的作用是 。
(3)装置D中发生反应的化学方程式是 。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体为b L(标况)。反应的离子方程式为_______________,样品中铝的物质的量为_____________(用含b的代数式表示)。
(2)若取a g样品,在高温下能恰好完全反应,该反应的化学方程式为________________,样品中氧化铁与铝的质量比为_________________(用含a 、b的代数式表示)。
(3)待(2)中反应产物冷却后,往其中加入足量的盐酸,测得生成的气体体积为c L(标况),则该气体与(1)中所得的气体的体积比c∶b=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法正确的是( )

A. 0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+c(CO32—)+c(HCO3—)
B. 当加入10mL盐酸时,所得混合溶液pH>7
C. 当pH=8时,c(Na+)=c(CO32—)+c(HCO3—)+c(H2CO3)
D. 在M点:c(CO32—)=c(HCO3—)>c(Na+)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3 L的密闭容器中反应CO(g)+ 2H2(g)![]() CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
(1)反应的平衡常数表达式K=_____________;根据下图,升高温度,K值将__________(填“增大”、“减小”或“不变”)。

(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是______(用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是______ (填字母)。
a.v生成(CH3OH)= v消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是(填字母)______________。
a.c(H2)减少 b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加 d.重新平衡时c(H2)/ c(CH3OH)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼是无色、有强还原性的液体,实验室制备水合肼的原理为:CO(NH2)2+2NaOH+NaClO==Na2CO3+N2H4·H2O+NaCl 据此,某学生设计了下列实验。
(制备NaClO溶液)

实验装置如图甲所示(部分夹持装置已省略)已知:3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3
(1)请写出肼的电子式_________________。
(2)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有________________。
(3)装置I中发生的化学反应方程式是 ____________________________;Ⅱ中用冰水浴控制温度在30℃以下,其主要目的是______________________________。
(制取水合肼)
实验装置如图乙所示。
(4)仪器B的名称为_________;反应过程中,如果分液漏斗中溶液的滴速过快,部分N2H4·H2O参与A中反应并产生大量氮气,请写出该反应的化学反应方程式__________。
(5)充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品。若在蒸馏刚刚开始的时候忘记添加沸石,应该采取的操作是_____________________。
(测定肼的含量)
称取馏分0.2500g,加水配成20.00mL溶液,在一定条件下,以淀粉溶液做指示剂,用0.1500 mol·L-1的I2溶液滴定。
已知:N2H4·H2O+2I2==N2↑+4HI+H2O
①滴定终点时的现象为______________________________。
②实验测得消耗I2溶液的平均值为20.00 mL,馏分中N2H4.H2O的质量分数为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com