
����Ŀ��ijͬѧ������һƿ��84����Һ������װ˵�����£�

����������Ϣ�����֪ʶ�жϣ����з�������ȷ����
A.�á�84����Һ�������ʵ���Ũ��ԼΪ4.0mol��L-1
B.һƿ�á�84����Һ�������տ�����44.8L��CO2(��״��)����ȫ����
C.ȡ100mL�á�84����Һ��ϡ��100��������������ϡ�ͺ����Һ��c(Na��)ԼΪ0.04mol��L-1
D.���ĸá�84����Һ�����䷽������NaClO��������480mL��25% NaClO������Һ����Ҫ������NaClO��������Ϊ149g
���𰸡�B
��������
A.����Һ�����ʵ���Ũ��c=![]() mol/L=4.0mol/L��A��ȷ��
mol/L=4.0mol/L��A��ȷ��
B.һƿ����84����Һ���к���NaClO�����ʵ���Ϊn(NaClO)=4.0mol/L��1L=4.0mol����������H2CO3>HClO���ᷢ����Ӧ��NaClO+CO2+H2O=NaHCO3+2HClO�����ݷ���ʽ��֪4.0mol NaClO��Ӧ������4mol CO2�����ڱ�״���µ����V=4mol��22.4L/mol=89.6L��B����
C.����84����Һ����Ũ��Ϊ4.0mol/L������ϡ��100����Na+Ũ����ԭ���İٷ�֮һ����ϡ�ͺ����Һ��c(Na��)ԼΪ0.04 mol/L��C��ȷ��
D.û��480mL������ƿ����ʹ��500mL������ƿ��������500mL 25% NaClO������Һ,�����ʵ���Ũ��Ϊ4.0mol/L��n(NaClO)=4.0mol/L��0.5L=2.0mol��m(NaClO)=2.0mol��74.5g/mol=149g��D��ȷ��
�ʺ���ѡ����B��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ɡ��ܽ��ת���������Ʊ����ᴿ�Լ����е������й㷺Ӧ�á���֪25��ʱ��Ksp(BaSO4)��1��10��10��Ksp(BaCO3)��1��10��9��
��1����Ũ�Ⱦ�Ϊ0.1 mol��L��1��BaCl2��Һ��Na2SO4��Һ�������ϣ���ֽ������ˣ���Һ��c(Ba2��)��_____mol��L��1��
��2��ҽѧ�Ͻ�������ϵͳ��X������ʱ����ʹ��BaSO4���ڷ���Ӱ����θ�����Ժ�ǿ( pHԼΪ1)�� �����ô���BaSO4��Ȼ�ǰ�ȫ�ģ�BaSO4���������ԭ����_______________________��(�ó����ܽ�ƽ��ԭ������)����һ���������BaCO3��Ӧ�����ô���0.5mol��L��1Na2SO4��Һ������ϴθ���������ϴθ������Na2SO4��ҺŨ�ȵı仯��������θҺ�е�Ba2��Ũ�Ƚ�Ϊ________mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ�Ӧ����ʽ��ȷ����(����)
A.����������Һ��̼��������Һ��ϣ�HSO4-+HCO3-=H2O+CO2��+SO42-
B.�ռ���Һ�������Һ��ϣ�OH-+H+ =H2O
C.���������Ȼ�����Һ�����Ȼ�������Fe3++Fe=2Fe2+
D.���ˮ�еμ�FeCl3��Һ�Ʊ�Fe(OH)3���壺Fe3+ +3H2O![]() Fe(OH)3(����)+3H+
Fe(OH)3(����)+3H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����(����)
A. 0.1 mol/L NaHCO3��Һ��0.1 mol/L NaOH��Һ�������ϣ�������Һ�У�c(Na��)>c(CO![]() )>c(HCO
)>c(HCO![]() )>c(OH��)
)>c(OH��)
B. 20 mL 0.1 mol/L CH3COONa��Һ��10 mL 0.1 mol/L HCl��Һ��Ϻ���Һ�����ԣ�������Һ�У�c(CH3COO��)>c(Cl��)>c(CH3COOH)>c(H��)
C. �����£�pH��2��������pH��12�İ�ˮ�������ϣ�������Һ�У�c(Cl��)��c(H��)>c(NH![]() )��c(OH��)
)��c(OH��)
D. 0.1 mol/L CH3COOH��Һ��0.1 mol/L NaOH��Һ�������ϣ�������Һ�У� c(OH��)>c(H��)��c(CH3COOH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ���ˮ�ܿ�����Ҫ�ɷ�ΪCo2O3����������Fe2O3�� Al2O3��MgO��CaO�������� �Ʊ��ܵ���������Ʊ���������������
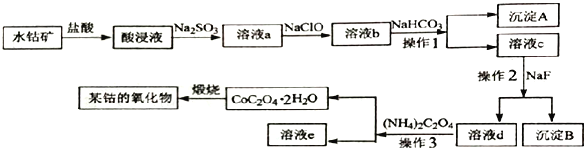
�ش�����������
��1���ڼ�����������������ʱ�����������������ʵķ�����______________����дһ������
��2��������������Na2SO3���ܵĴ�����ʽΪCo2+��д������Co2+��Ӧ�����ӷ���ʽ_______________________________��
��3����Һa�м���NaClO������Ϊ_______________________________��
��4������A �ijɷ�Ϊ__________________������2��������___________________��
��5����֪: Ksp (CaF2)=5.3��10-9��Ksp(MgF2)=5.2��10-12��������Һc �м���NaF��Һ����Mg2+ǡ�ó�����ȫ����Һ��c(Mg2+)=1.0��10-5moI/L����ʱ��Һ��c(Ca2+)������_________mol��L-1��
��6���ڿ���������CoC2O4 �����ܵ�ij���������CO2����ó�����պ��������Ϊ12.05 g��CO2�����Ϊ6.72 L����״��������˷�Ӧ�Ļ�ѧ����ʽΪ_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 0.1 mol H2�к��еķ�����Ϊ6.02��1022
B. 24 g Mg���Mg2��ʱʧȥ�ĵ�����Ϊ6.02��1023
C. 1 L 1 mol��L��1 CaCl2��Һ�к��е�Cl����Ϊ6.02��1023
D. ���³�ѹ�£�11.2 L O2�к��е�ԭ����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�����(S2C12)�����л�������Ʒ��ɱ�������Ⱦ�ϡ��ϳ��������е��Ȼ������м��塣S2Cl2��һ���ж����ж����ζ��dz��ɫҺ�壬��300��������ȫ�ֽ⣬��������ˮ�ֽ⣬���ܽ���ǣ�����������ͨ�����ڵ���Ƕ��ã�������Cl2�ὫS2Cl2��һ�������õ�SCl2�������Ƕ�S2Cl2���Ʊ����о�����ش��������⣺
��.S2Cl2���Ʊ�
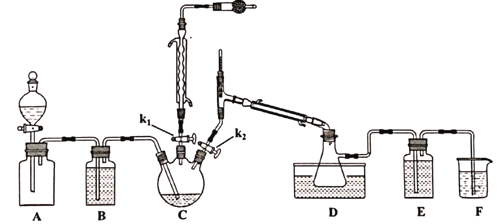
��֪�������ʵ��۷е����£�
���� | S | S2Cl2 | SCl2 |
�е�/�� | 445 | 138 | 59 |
�۵�/�� | 113 | ��76 | ��122 |
�Ʊ�������Ϊ��
��Aװ�ü���ƿ�г���Cl2����Aװ���еķ�Һ©������k1��k2��һ��ʱ���ر�k2��
�ڽ�ͨ����ˮ����C������135~140�档
��һ��ʱ���ر�k1��ͬʱ��k2�������D���ռ���dz��ɫҺ�塣
(1)ʵ������ȡ�����ķ�Ӧ����ʽ_________________________________��
(2)Aװ�÷�Һ©����ʢװ��Һ����___________��
A.CCl4 B.����NaHCO3��Һ C����NaCl��Һ
(3)�μӹ���Ҫ������ԭ����____________________________________________��
(4)Dװ����ˮԡ�¶�Ӧ����Ϊ___________��ԭ����_______________________________��
��.S2Cl2���ȵIJⶨ
��֪��S2Cl2��ˮ�ֽ�Ļ�ѧ����ʽ��2S2Cl2+2H2O=3S��+SO2��+4HCl��ȡag���л�ɫҺ������ƿ����ˮ����Ӧ��ȫ(�������ʾ�����ˮ��Ӧ)��������Һ�м��������C0 mol/L��AgNO3��ҺV0mL��������ƿ�м����������������ɵij������ǡ���������Fe��NO3)3��ָʾ������C1 mol/L NaSCN��Һ�ζ����յ㣬���� NaSCN��ҺV1mL(�ζ����̷�����Ӧ��Ag++SCN-= AgSCN��)
(5)�ζ��յ������Ϊ_________________________________��
(6)S2Cl2�Ĵ���Ϊ___________(д������ʽ)�����ζ�������δ���������������ô���___________��(�ƫ����ƫС��������Ӱ�족)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ؽ���Ԫ�ظ��Ķ��Խϴ�����ˮ�辭������������ŷš�
��.ij��ҵ��ˮ����Ҫ����Cr3����ͬʱ������������Fe3����Al3����Ca2����Mg2���ȣ������Խ�ǿ��Ϊ�������ã�ͨ�������������̴�����
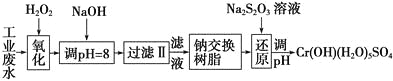
ע�����������ӳ�����������������ʽ��ȫ����ʱ��Һ��pH���±���
�������� | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9�ܽ�) |
��1�����������пɴ���H2O2������Լ���________(�����)��
A��Na2O2B��HNO3C��FeCl3D��KMnO4
��2������NaOH��Һ������ҺpH��8ʱ����ȥ��������________����֪�����ӽ�����֬��ԭ����Mn����nNaR�D��MRn��nNa�����˲�������������ȥ������������__________��
A��Fe3��B��Al3��C��Ca2��D��Mg2��
��3����ԭ�����У�ÿ����0.8 mol Cr2O![]() ת��4.8 mol e�����÷�Ӧ���ӷ���ʽΪ________________��
ת��4.8 mol e�����÷�Ӧ���ӷ���ʽΪ________________��
��.���������£����۸���Ҫ��Cr2O![]() ��ʽ���ڣ���ҵ�ϳ��õ�ⷨ������Cr2O
��ʽ���ڣ���ҵ�ϳ��õ�ⷨ������Cr2O![]() �ķ�ˮ��
�ķ�ˮ��
�÷���Fe���缫��⺬Cr2O![]() �����Է�ˮ�����ŵ����У�������������ҺpH���ߣ�����Cr(OH)3��Һ��
�����Է�ˮ�����ŵ����У�������������ҺpH���ߣ�����Cr(OH)3��Һ��
��1�����ʱ�ܷ���Cu�缫������Fe�缫��________(������������������)��������______________��
��2�����ʱ����������Һ��Cr2O![]() ת��ΪCr3�������ӷ���ʽΪ___________________��
ת��ΪCr3�������ӷ���ʽΪ___________________��
��3�������£�Cr(OH)3���ܶȻ�Ksp��1��10��32����Һ��pHӦΪ____ʱ����ʹc(Cr3��)����10��5mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ�������ж���ȷ����
A. �����£�5.6 g Fe������ˮ������Ӧ��ת�Ƶĵ�����Ϊ0.3NA
B. ��״���£�22.4 L NO��11.2 L O2��ַ�Ӧ������ķ�����ΪNA
C. 60g�����������Ҵ�����������Ӧ����ַ�Ӧ����ѵ�C��O����ĿΪNA
D. ����0.2 mol NH4Al(SO4)2����Һ�еμ�NaOH ��Һ������ǡ����ȫ�ܽ⣬������OH������ĿΪNA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com