
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
【答案】排除体系中的N2A和DDCxHyOzNm+(![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O+
H2O+![]() N2吸收未反应的O2,保证最终收集的气体是N2量筒内液面与广口瓶中的液面持平视线与凹液面最低处相切ABD
N2吸收未反应的O2,保证最终收集的气体是N2量筒内液面与广口瓶中的液面持平视线与凹液面最低处相切ABD
【解析】
在本实验中,通过测定氨基酸和氧气反应生成产物中二氧化碳、水和氮气的相关数据进行分析。实验的关键是能准确测定相关数据,用浓硫酸吸收水,碱石灰吸收二氧化碳,而且二者的位置不能颠倒,否则碱石灰能吸收水和二氧化碳,最后氮气的体积测定是主要多余的氧气的影响,所以利用加热铜的方式将氧气除去。首先观察装置图,可以看出A中是氨基酸的燃烧,B中吸收生成的水,在C中吸收生成的二氧化碳,D的设计是除掉多余的氧气,E、F的设计目的是通过量气的方式测量氮气的体积,在这个基础上,根据本实验的目的是测定某种氨基酸的分子组成,需要测量的是二氧化碳和水和氮气的量。实验的关键是氮气的量的测定,所以在测量氮气前,将过量的氧气除尽。
(1)装置中的空气含有氮气,影响生成氮气的体积的测定,所以通入一段时间氧气的目的是排除体系中的N2;
(2)氨基酸和氧气反应,以及铜和氧气反应都需要加热,应先点燃D处的酒精灯,消耗未反应的氧气,保证最终收集的气体只有氮气,所以应先点燃D处酒精灯。
(3)氨基酸燃烧生成二氧化碳和水和氮气,方程式为: CxHyOzNm+(![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O+
H2O+![]() N2;
N2;
(4)加热铜可以吸收未反应的O2,保证最终收集的气体是N2 ;
(5)读数时必须保证压强相同,所以注意事项为量筒内液面与广口瓶中的液面持平而且视线与凹液面最低处相切;
(6) 根据该实验原理分析,要测定二氧化碳和水和氮气的数据,再结合氨基酸的相对分子质量确定其分子式。故选ABD。


科目:高中化学 来源: 题型:
【题目】化介物H是一种有机光电材料中间体。实验室由芳香化合物A制务H的一种合成路线如下:
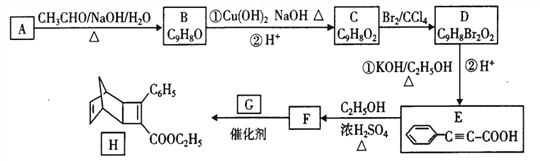
已知:①![]()
②![]()
回答下列问题:
(1)E中的官能团名称为____________和_______________。
(2)C→D的反应类型为___________,B→C的化学反应方程式为_________________。
(3)G的结构简式为_______________。
(4)写出同时满足下列条件的F的一种同分异构体的结构简式______________。
①遇FeCl3溶液显紫色; ②能发生银镜反应; ③分子中有5种不同化学环境的氢且个数比为1:1:2:2:4。
(5)写出用甲醛和乙烯为原料制备化合物C(CH2ONO2)的合成路线(其他无机试剂任选,合成路线流程图示例见本题题干)。_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
A. 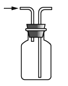 收集 NOB.
收集 NOB.  制备 NH3
制备 NH3
C.  制备 Fe(OH)2D.
制备 Fe(OH)2D. 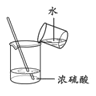 稀释浓 H2SO4
稀释浓 H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用时,反应条件(温度、反应物用量、浓度等)改变,不会引起产物改变的是 ( )
A. NaOH和CO2B. Fe粉在Cl2中燃烧
C. Na和O2D. Cu和HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。
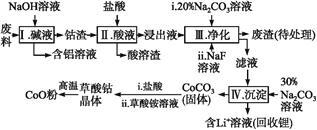
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表。
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是__________。
(2)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:______。
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过______;废渣中的主要成分除了LiF外,还有______。
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是______。
(5)在空气中加热5.49 g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~920 | 2.25 |
①加热到210 ℃时,固体质量减轻的原因是__________。
②经测定,加热到210~290 ℃过程中的生成物只有CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中,发生以下反应:2A(g)+ B(g) ![]() 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
A. 1.6 mol B. 2.8 mol
C. 2.4 mol D. 1.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com