
【题目】下列说法正确的是( )
A.在粗硅的制取中发生2C+SiO2![]() 2CO↑+Si,硅被还原,所以碳的还原性大于硅的还原性
2CO↑+Si,硅被还原,所以碳的还原性大于硅的还原性
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D.由Na2CO3+SiO2![]() CO2↑+Na2SiO3可知硅酸的酸性大于碳酸
CO2↑+Na2SiO3可知硅酸的酸性大于碳酸
【答案】C
【解析】
试题分析:A.在粗硅的提取中发生反应2C+SiO2![]() 2CO+Si,由于反应是在高温条件下进行,因此尽管是硅被还原,也不能说碳的还原性大于硅的还原性,A错误;B.硅酸钠属于盐,由有粘性,会把试剂瓶与玻璃塞粘在一起,因此不能保存在磨口玻璃塞试剂瓶中,B错误;C.SiO2是酸性氧化物,难溶于水,因此若用SiO2制取硅酸,应先使二氧化硅与碱氢氧化钠溶液反应产生Na2SiO3,然后利用酸性H2CO3大于H2SiO3的性质,然后再通入CO2,就可以反应产生H2SiO3,C正确;D.复分解反应的规律是强酸制取弱酸,由Na2CO3+SiO2
2CO+Si,由于反应是在高温条件下进行,因此尽管是硅被还原,也不能说碳的还原性大于硅的还原性,A错误;B.硅酸钠属于盐,由有粘性,会把试剂瓶与玻璃塞粘在一起,因此不能保存在磨口玻璃塞试剂瓶中,B错误;C.SiO2是酸性氧化物,难溶于水,因此若用SiO2制取硅酸,应先使二氧化硅与碱氢氧化钠溶液反应产生Na2SiO3,然后利用酸性H2CO3大于H2SiO3的性质,然后再通入CO2,就可以反应产生H2SiO3,C正确;D.复分解反应的规律是强酸制取弱酸,由Na2CO3+SiO2 ![]() CO2+Na2SiO3,是由于在高温下用高沸点的酸制取低沸点的栓,与酸性强弱无关,D错误。答案选C。
CO2+Na2SiO3,是由于在高温下用高沸点的酸制取低沸点的栓,与酸性强弱无关,D错误。答案选C。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1L lmol·L—1FeBr2溶液与l molCl2气反应时转移的电子数目为3NA
B. 7g分子式为CnH2n的链烃中含有的C—H键的数目为NA
C. 常温时,1.0L pH=13的Ba(OH)2溶液中含有OH—的数目为0.2NA
D. 0.5mol·L—1硫酸钠溶液中含有溶质离子总数为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO![]() 、⑥SO
、⑥SO![]() 中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 | 操作 | 现象 |
(1) | 用pH试纸检验 | 溶液的pH大于7 |
(2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
(3) | 向(2)所得的水溶液中加入Ba(NO3)2溶液和稀硝酸 | 有白色沉淀产生 |
(4) | 过滤,向滤液中加入AgNO3溶液和稀硝酸 | 有白色沉淀产生 |
下列结论正确的是( )
A. 不能确定的离子是① B. 不能确定的离子是③⑤
C. 肯定含有的离子是①④⑤ D. 肯定没有的离子是②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3kJ/mol、2800 kJ/mol。则下列热化学方程式正确的是
A.C(s)+![]() O2(g)=CO(g);△H= - 393.5 kJ/mol
O2(g)=CO(g);△H= - 393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(l);△H=+571.6 kJ/mol
C.CH4(g)+CO2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol
D.![]() C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400 kJ/mol
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学应用如图所示装置研究气体的性质.现有某气体,其主要成分是氯气,还含有少量空气和水蒸气,请回答:
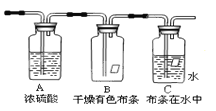
(1)实验室用二氧化锰和浓盐酸制取氯气____________(写化学方程式),该实验研究的主要目的是 。浓硫酸的作用是 。
(2)B、C中能观察到的实验现象是
B中 ;
C中 .
(3)氯水里面含有较多成分,氯水呈黄绿色,起作用的是 ,将紫色石蕊溶液滴入氯水中,氯水显红色,过一会儿,红色消失,起作用的成分是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是一种常用的消毒剂,我国从2 000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有__________性。
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:
2KClO3+SO2=2ClO2+__________。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,是放热反应,当1 mol Cl2参与反应时 释放145 kJ的热量,写出这个反应的热化学方程式:________________。
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检 测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O![]() +I2=S4O
+I2=S4O![]() +2I-)
+2I-)
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示:

请回答:
①操作Ⅰ中反应的离子方程式是___________________。
②确定操作Ⅱ完全反应的现象是___________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是___________________。
④若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mol·L-1的Na2S2O3溶液10mL,则水样中ClO2的浓度是________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.反应SiO2 (s) + 3C(s)=SiC(s)+2CO(g)室温下不能进行,则该反应的△H<0
B.铅蓄电池放电过程中,正极质量增加,负极质量减小
C.25 ℃下,在NH3·H2O稀溶液中,加水,  的值不变
的值不变
D.在NaHS溶液中,滴入少量CuC12溶液产生黑色沉淀,HS-水解程度增大,pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3在工业生产中有着重要的用途。下列关于NH3的性质叙述不正确的是
A. 密度比空气小 B. 极易溶于水
C. 可由N2和H2作为原料进行工业生产 D. 任何条件下,不能与氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“嫦娥飞天,玉兔登月”,实现了中华民族“九天揽月”的伟大梦想。制造登月车太阳能电池板的半导体材料是
A.硅 B.二氧化硅 C.铝合金 D.铁合金
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com