
【题目】“嫦娥飞天,玉兔登月”,实现了中华民族“九天揽月”的伟大梦想。制造登月车太阳能电池板的半导体材料是
A.硅 B.二氧化硅 C.铝合金 D.铁合金
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在粗硅的制取中发生2C+SiO2![]() 2CO↑+Si,硅被还原,所以碳的还原性大于硅的还原性
2CO↑+Si,硅被还原,所以碳的还原性大于硅的还原性
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D.由Na2CO3+SiO2![]() CO2↑+Na2SiO3可知硅酸的酸性大于碳酸
CO2↑+Na2SiO3可知硅酸的酸性大于碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,在生产中有着重要的应用。工业上用甲烷氧化法合成甲醇的反应有:
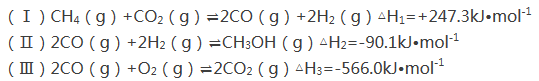
(1)用CH4和O2直接制备甲醇蒸气的热化学方程式为 。
(2)某温度下,向容积为4 L的容器通人6 mol CO2和6mol CH4,发生反应(i),平衡体系中各组分的体积分数均为![]() ,则此温度下该反应的平衡常数K= ,CH4的转化率为 。该温度下反应达平衡后,将反应容器的容积增大至10L,平衡向___________(填“正反应”或“逆反应”)方向移动。
,则此温度下该反应的平衡常数K= ,CH4的转化率为 。该温度下反应达平衡后,将反应容器的容积增大至10L,平衡向___________(填“正反应”或“逆反应”)方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述不正确的是( )
A.甲烷和乙烯都可以与氯气反应,反应类型不同
B.蔗糖、油脂、蛋白质都可以水解
C.乙烯和氯乙烯都可以通过聚合反应得到高分子材料
D.乙醇和乙酸都存在碳氧双键,二者可以发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 L水中含有的水分子数为NA
B.常温常压下,46 g NO2和N2O4的混合气体中含有的氧原子数为2NA
C.1mol/L的Ba(NO3)2溶液中含NO3-离子数为2NA
D.分子数为NA的CO和N2的混合气体的体积约为22.4 L,质量为28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。
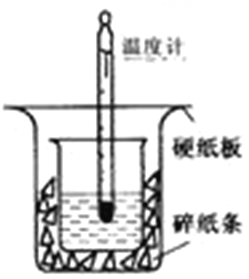
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_______。装置中还存在的2个错误是 。
(2)在实验过程中,该同学需要测定并记录的实验数据有 (填序号)。
A盐酸的浓度 B盐酸的温度
C氢氧化钠溶液的浓度 D氢氧化钠溶液的温度
E水的比热容 F反应后混合溶液的终止温度
(3)使用补全仪器后的装置进行实验,取50ml0.50mol·L-1盐酸与50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃。已知中和后生成的溶液的 比热容为4.18J/(g·℃),溶液的密度均为1g/cm3。通过计算可得中和热△H= 。
(4)实验中改用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述正确的实验操作相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会 ;(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于DNA与RNA的叙述,正确的是( )
A. 在细胞内存在的主要部位相同 B. 构成的五碳糖不同
C. 核苷酸之间的连接方式不同 D. 构成的碱基相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4 mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65 kJ的热量。
(1)写出肼和过氧化氢的结构式:肼____________过氧化氢____________。
(2)写出反应的热化学方程式:__________________________。
(3)已知H2O(l)===H2O(g) ΔH=+44 kJ·mol-1,则16 g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是________kJ。
(4)上述反应用于火箭推进剂,除释放大量热和快速产生大量气体个很突出的优点是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸240ml。
(1)在盛放浓硫酸的试剂瓶的标签上应印有下列警示标志中的____________。

(2)选用的主要仪器有:__________
①烧杯,②玻璃棒,③量筒,④胶头滴管,⑤____________。
(3)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至凹液面恰好与刻度线相切
D.稀释浓H2SO4
E.将冷却后的稀释液转入容量瓶
F.将蒸馏水注入容量瓶,直到液面距刻度线1-2cm处
G.用少量蒸馏水洗涤烧杯和玻璃棒2-3次,并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀,其操作正确的顺序依次为____________________________。
(4)简要回答下列问题:
①所需浓硫酸的体积为____________mL,如果实验室有10mL、20mL、50mL的量筒应选用____________mL的量筒最好
②下列操作使所配溶液浓度偏高的是__________
A.用水洗涤量取浓硫酸的量筒,并将洗涤液转入容量瓶中
B.用量筒来量取浓硫酸,读数时,俯视量筒
C.搅拌过程中有液体溅出
D.在转入容量瓶前烧杯中液体未冷却至室温
E.定容时,俯视刻度线
F.容量瓶用蒸馏水洗净后未经干燥马上用来配制溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com