
【题目】[化学—选修5:有机化学基础]对乙酰氨基酚,俗称扑热息痛(Paracetamol),具有很强的解热镇痛作用,工业上通过下列方法合成(图中B1和B2、C1和C2分别互为同分异构体,无机产物略去):
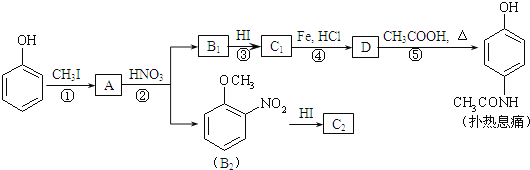
已知:![]() ,请按要求填空:
,请按要求填空:
(1)写出A分子中官能团名称:_________;C1的结构简式为:___________________。
(2)写出由D生成扑热息痛的化学方程式:_______________________。
(3)学出反应③和④的反应类型:③______________,④__________。
(4)工业上设计反应①、②、③,而不是只通过反应②得到C1、C2,其目的是:___________。
(5)扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(1)是对位二取代苯;(II)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(III)两个氧原子与同一原子相连。其中2种的结构简式是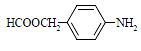 和
和![]() ,写出另3种同分异构体的结构简式____________、____________、____________。
,写出另3种同分异构体的结构简式____________、____________、____________。
【答案】(1)醚键(2分);![]() (2分)
(2分)
(2)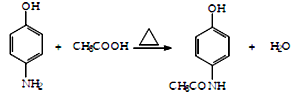 (2分)
(2分)
(3)取代反应,还原反应(各2分)
(4)保护酚羟基不被硝酸氧化(2分)
(5)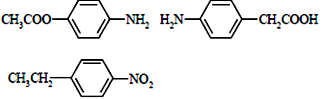 (3分)
(3分)
【解析】
试题分析:苯酚和CH3I发生取代反应生成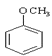 ,A与硝酸发生硝化反应生成
,A与硝酸发生硝化反应生成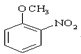 或
或![]() ,所以B1为
,所以B1为![]() ,与HI发生取代反应,则C1为
,与HI发生取代反应,则C1为![]() ,C2为
,C2为 ,C1发生还原反应得D为
,C1发生还原反应得D为![]() ,D与乙酸发生取代反应得扑热息痛,则
,D与乙酸发生取代反应得扑热息痛,则
(1)根据A的结构简式可知A分子中官能团名称为醚键;C1的结构简式为![]() 。
。
(2)由D生成扑热息痛的化学方程式为![]() +CH3COOH
+CH3COOH![]()
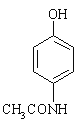 +H2O。
+H2O。
(3)根据以上分析可知反应③和④的反应类型分别是取代反应,还原反应。
(4)C1、C2含有酚羟基,易被硝酸氧化,应先生成醚基,防止被氧化,其目的是保护酚羟基不被硝酸氧化;
(5)含N基团可为氨基或硝基,当为氨基时,含碳基团可为羧基或酯基,当为硝基时,对位应为乙基,可能的结构还有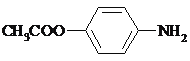 、
、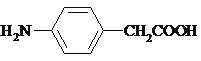 、
、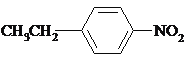 。
。


科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与应用不相对应的是
A.Na2O2能分别与H2O、CO2反应产生氧气,可用作供氧剂
B.硅胶多孔、吸水能力强,常用作袋装食品的干燥剂
C.K2FeO4具有强还原性且被氧化生成Fe3+,可用于水的消毒和净水
D.液氨气化时能吸收大量的热,使周围温度急剧降低,因此可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp (25℃)如下:
AgCl | AgI | Ag2S | |
Ksp(单位省略) | 1.8×10-10 | 1.5×10-16 | 6.3×10-50 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀容易转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示.下列说法不正确的是( )

A.图中五点Kw间的关系:B>C>A=D=E
B.若0.1 mol/L 的NaHA 溶液水溶液中c(H+)与c(OH-)关系如图D 点所示,则 溶液中有:c(HA-)>c(OH-)>c(A2- )>c(H2A)
C.E 点对应的水溶液中,可能有NH 4+、Ba 2+、Cl-、I-大量同时存在
D.向NaHSO4溶液中滴入Ba(OH)2溶液,当c(H+)与c(OH-)关系如图A 点所示,则溶液中反应: 2H++SO4 2-+Ba2++2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制作印刷电路板。下列说法正确的是
A. 该反应为置换反应 B. 用KSCN溶液可检验废液中的Fe2+
C. 可用置换法回收废液中的铜 D. Fe3+能溶解Cu说明Cu比Fe金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定温度下的2 L固定容积的密闭容器中,通入2 mol CO2和3 mol H2,发生的反应为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-akJ·mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-akJ·mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
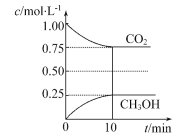
①能说明该反应已达平衡状态的是_____________(填编号)。
A.单位时间内每消耗1.2 mol H2,同时生成0.4 mol H2O
B.CO2的体积分数在混合气体中保持不变
C.混合气体的平均相对分子质量不随时间的变化而变化
D.该体系中H2O与CH3OH的物质的量浓度之比为1∶1,且保持不变
②若要使K=1,则改变的条件可以是_____________(填选项)。
A增大压强 B减小压强 C升高温度 D降低温度 E加入催化剂
(2)有一种用CO2生产甲醇燃料的方法。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(l) ΔH=-akJ·mol-1;
CH3OH(g)+H2O(l) ΔH=-akJ·mol-1;
CH3OH(g)=CH3OH(l) ΔH=-bkJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH=-ckJ·mol-1;
则表示CH3OH(l)燃烧热的热化学方程式为 。
(3)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)![]() 3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。
3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。
物质 | A | B | C | D |
起始投料/mol | 2 | 1 | 3 | 0 |
该反应的平衡常数表达式为K=__________。升高温度,平衡常数将__________(填“增大”“减小”或“不变”)。
p>(4)为研究不同条件对反应2NO(g)+Cl2(g)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com