
【题目】常温下,改变0.1mol·L-1的富马酸(H2A)溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)[ δ(X)= ![]() ]随pH的变化如图所示。下列叙述正确的是( )
]随pH的变化如图所示。下列叙述正确的是( )

A.pH=3.05时,c(H2A)=c(HA-)=c(OH-)B.pH=4.0时, c(HA-)>C(H2A)>c(A2-)
C.常温下,反应HA-+OH-![]() A2-+H2O的pK=9.51D.常温下,图中x点处:1g
A2-+H2O的pK=9.51D.常温下,图中x点处:1g![]() =0.72
=0.72
【答案】D
【解析】
A.H2A的第一步电离平衡常数![]() , 当c(HA-)=c(H2A)时,K1=c(H+),由于pK1=3.05,因此可得当c(HA-)=c(H2A)时,c(H+)=10-3.05 , 此时溶液的pH=3.05,因此当溶液的pH=3.05时,c(H2A)=c(HA-)>c(OH-),故A错误;
, 当c(HA-)=c(H2A)时,K1=c(H+),由于pK1=3.05,因此可得当c(HA-)=c(H2A)时,c(H+)=10-3.05 , 此时溶液的pH=3.05,因此当溶液的pH=3.05时,c(H2A)=c(HA-)>c(OH-),故A错误;
B.由图可知,当溶液的pH=4.0时,溶液中离子浓度关系为:c(HA-)>c(A2-)>c(H2A),故B错误;
C.该反应的平衡常数![]() , 又水的离子积Kw=c(H+)×c(OH-),H2A的第二步电离平衡常数
, 又水的离子积Kw=c(H+)×c(OH-),H2A的第二步电离平衡常数![]() , 因此该反应的平衡常数
, 因此该反应的平衡常数![]() , 又pK2=4.49,因此K2=10-4.49, 常温下,Kw=10-14, 因此该反应的平衡常数
, 又pK2=4.49,因此K2=10-4.49, 常温下,Kw=10-14, 因此该反应的平衡常数![]() , 因此pK=-lgK=-lg109.51=-9.51,故C错误;
, 因此pK=-lgK=-lg109.51=-9.51,故C错误;
D.pK1=3.05,则K1=10-3.05, pK2=4.49,因此K2=10-4.49;由于X点时溶液中c(H2A)=c(A2-),因此![]() , 因此X点时溶液中
, 因此X点时溶液中![]() , 因此X点溶液中
, 因此X点溶液中![]() , 故D正确;
, 故D正确;
故答案为:D,


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】某学习小组利用如图实验装置制备Cu(NH3)xSO4·H2O。并测量x值。
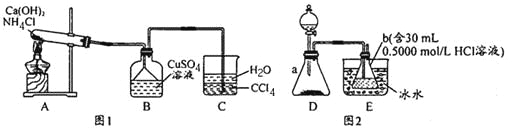
(Cu(NH3)xSO4·H2O制备)见图1
(1)A中发生的化学反应方程式为________________________________。
(2)C中CCl4的作用是______________。
(3)B中先产生蓝色沉淀,随后沉淀溶解变成深蓝色溶液,此溶液中含有Cu(NH3)xSO4,若要从溶液中析出Cu(NH3)xSO4·H2O晶体,可加入试剂___________________________。
(x值的测量)见图2
步骤一:检查装置气密性,称取0.4690g晶体[M=(178+17x)g/mol]于锥形瓶a中
步骤二:通过分液漏斗向锥形瓶a中滴加l0%NaOH溶液至无气体产生为止
步骤三:用0.5000mol/L的NaOH标准溶液液滴定b中剩余HCI,消耗标准溶液液16.00mL
(4)步骤二的反应可理解为Cu(NH3)xSO4与NaOH在溶液中反应,其离子方程式为_________________。
(x值的计算与论证)
(5)计算:x=__________。
该学习小组针对上述实验步骤,提出测量值(x)比理论值偏小的原因如下:
假设1:步骤一中用于称量的天平砝码腐蚀缺损;
假设2:步骤二中_____________________________________________________(任写两点);
假设3 :步骤三中测定结束读数时,体积读数偏小。该假设_______(填“成立”或“不成立”)。
(6)针对假设l,你对实验的处理意见是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:①乙醇蒸气通过红色粉末(CrO3),红色粉末变成绿色粉末(Cr2O3),生成乙醛。②乙醛能还原酸性高锰酸钾溶液。某小组设计如下装置制备少量乙醛。下列说法错误的是( )
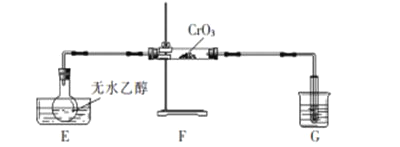
A.水槽E中装热水,烧杯G中装冷水
B.检验乙醛的方法是向反应后的溶液中滴加酸性高锰酸钾溶液
C.E中增加一支温度计,有利于提高乙醇的利用率
D.常采用蒸馏操作分离、纯化粗产品中的乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取少量溴乙烷的装置如图所示,将生成物导入盛有冰水混合物的试管a中,实验结束发现试管a中的物质分为三层.对该实验的分析错误的是( )
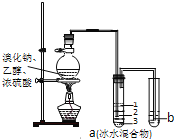
A. 烧瓶中除发生取代反应可能发生消去反应、氧化还原反应等
B. 产物在a中第一层
C. a中有产物和水还含HBr、CH3CH2OH等
D. b中盛放的酸性KMnO4溶液会褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学配置450毫升 1mol/L的硫酸溶液
(1)应该选择________的容量瓶 A 250毫升 B 500毫升 C 1000毫升
(2)需要量取98%,ρ=1.84g/cm3浓硫酸__________毫升
(3)将所取浓硫酸逐滴加入盛有水的烧杯中,边加边搅拌
(4)将该溶液注入容量瓶
(5)在容量瓶中加水至___________处,改用__________加水至_______与刻度线相切
(6)塞好瓶塞,反复摇匀
(7)摇匀后发现,溶液体积缩小,继续加水至刻度线
(8)该同学的操作是否有不当之处,请指出(不必全部填满)
a__________________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
b____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
c_______________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
d____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从葡萄籽中提取的原花青素结构如右图所示,具有生物活性,如抗氧化和自由基清除能力等,可防止机体内脂质氧化和自由基的产生而引发的肿瘤等多种疾病。有关原花青素的下列说法不正确的是( )

A. 该物质既可看做醇类,也可看做酚类
B. 1 mol该物质可与4 mol Br2反应
C. 1 mol该物质可与7 mol NaOH反应
D. 1 mol该物质可与7 mol Na反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中,始终无明显现象的是( )
A.NO2通入FeSO4溶液中
B.SO2通入已酸化的Ba(NO3)2溶液中
C.NH3通入AlCl3溶液中
D.CO2通入CaCl2溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型药物H(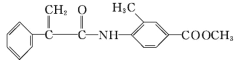 )是一种可用于治疗肿瘤的药物,其合成路线如图所示:
)是一种可用于治疗肿瘤的药物,其合成路线如图所示:
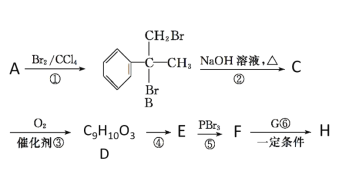
已知:①E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色;
②RCOOH![]()
![]() (R为烃基);
(R为烃基);
③![]()
![]()
![]() 。
。
请回答下列问题:
(1)A的结构简式为________;D的官能团的名称为____________。
(2)①的反应类型是________。
(3)写出B→C的化学方程式: ______________________________________。
(4)E有多种同分异构体,同时满足下列条件的E的同分异构体的结构简式_______。
ⅰ.能发生银镜反应
ⅱ.能发生水解反应
ⅲ.分子中含的环只有苯环,且苯环上只有一个取代基。
(5)参照合成H的上述路线,设计一条由乙醛和NH2CH(CH3)2为起始原料制备医药中间体CH3CONHCH(CH3)2的合成路线。
________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,体积不变的密闭容器中发生反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),经2min后达到平衡。NH3的浓度减少了0.6mol·L-1,下列说法正确的是( )
4NO(g)+6H2O(g),经2min后达到平衡。NH3的浓度减少了0.6mol·L-1,下列说法正确的是( )
A.平衡时:5V正(O2)=4V逆(NO)
B.2min末的反应速率,用NO表示是0.3 mol·L-1·min-1
C.由混合气体的密度不再改变可判定达到平衡
D.由混合气体的压强不再改变可判定达到平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com