
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
|
| A. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32﹣、NO3﹣ |
|
| B. | 甲基橙呈黄色的溶液:I﹣、Ba2+、AlO2﹣、Cl﹣ |
|
| C. | c(H+)=1.0×10﹣13mol/L溶液中C6H5O﹣、K+、SO42﹣、Br﹣ |
|
| D. | 1.0 mol•L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣ |
| 离子共存问题. | |
| 专题: | 离子反应专题. |
| 分析: | A、铝是两性元素和强酸、强碱反应生成氢气; B、甲基橙呈黄色溶液P溶液PH>4.4,溶液可能是酸、中性、碱; C、氢离子浓度c(H+)=1.0×10﹣13mol/L,说明溶液呈碱性; D、硝酸根在酸溶液中具有氧化性能氧化亚铁离子. |
| 解答: | 解:A、与铝反应产生大量氢气的溶液可能是酸溶液或碱溶液:Na+、K+、CO32﹣、NO3﹣,酸溶液中碳酸根离子不能大量存在,故A不符合; B、甲基橙呈黄色溶液P溶液PH>4.4,溶液可能是酸、中性、碱;在酸溶液中AlO2﹣不能大量存在,故B不符合; C、c(H+)=1.0×10﹣13mol/L溶液,依据离子积常数计算可知溶液呈碱性,C6H5O﹣、K+、SO42﹣、Br﹣,离子可以大量存在,故C符合; D、1.0 mol•L﹣1的KNO3溶液存在硝酸根离子,H+、Fe2+、Cl﹣、SO42﹣在酸溶液中的Fe2+离子被氧化,不能存在,故D不符合; 故选C. |
| 点评: | 本题考查了离子共存的分析判断,离子性质和环境的判断是解题依据,关键注意硝酸根离子在酸溶液中的氧化性判断,题目难度中等. |


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
有某种含有少量FeCl2杂质的FeCl3样品。现要测定其中铁元素的质量分数,实验采用下列步骤进行:
①准确称量mg样品(在2—3g范围内):
②向样品中加入10mL 6 moL·L-1的盐酸,再加入蒸馏水,配制成250mL溶液:
③量取25mL操作②中配得的溶液,加入3mL氯水,加热使其反应完全;
④趁热迅速加入10%氨水至过量,充分搅拌,使沉淀完全:
⑤过滤,将沉淀洗涤后,移至坩埚,灼烧、冷却、称重,并重复操作至恒重。
试回答下列问题:
(1)溶解样品时,要加入盐酸,原因是 ;
(2)加入氯水后,反应的离子方程式为 ;
(3)加入过量氨水生成沉淀的离子方程式为 ;
(4)若不用氯水,可用下列试剂中的 代替(填序号)。
A.H2O2 B.碘水 C.NaClO
(5)步骤⑤中检验沉淀是否洗净的方法是 。
(6)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为 (请把结果约到最简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家研制出多种新型杀虫剂代替DDT,化合物M是其中的一种。下列关于M的说法错误的是
A.M的分子式为C15H22O3
B.与FeCl3溶液发生反应后溶液不显紫色
C.M可以发生银镜反应
| |
D.1molM最多与1molH2完全加成
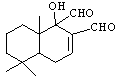 化合物M
化合物M
查看答案和解析>>
科目:高中化学 来源: 题型:
某课题组以苯为主要原料,采用以下路线合成利胆药—柳胺酚。
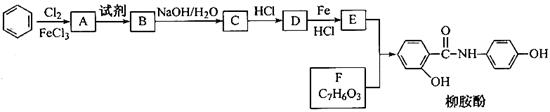 |
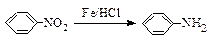 已知:。 请回答下列问题:
已知:。 请回答下列问题:
(1)对于柳胺酚,下列说法正确的是 。
A.1 mol柳胺酚最多可以和2 molNaOH反应 B.不发生硝化反应
C.可发生水解反应 D.可与溴发生取代反应
(2)写出A→B反应所需的试剂 。
(3)写出B→C的化学方程式 。
(4)写出化合物F的结构简式 。
(5)写出同时符合下列条件的F的同分异构体,其结构简式为
(写出3种)。
①属酚类化合物,且苯环上有三种不同化学环境的氢原子;②能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的工业原料.工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
|
| A. | 若管道漏气遇氨就会产生白烟 | B. | 该反应利用了Cl2的强氧化性 |
|
| C. | 该反应属于复分解反应 | D. | 生成1mol N2有6mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G各物质间的关系如图,其中B、D为气态单质.
请回答下列问题:
(1)物质C和E的名称分别为 浓盐酸 、 四氧化三铁 ;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为 2H2O2═2H2O+O2↑ ;若只能在加热情况下进行,则反应物A应为 KClO3 ;
(3)反应②的化学方程式为 4HCl(浓)+MnO2 MnCl2+2H2O+Cl2↑ ;
MnCl2+2H2O+Cl2↑ ;
(4)新配制的F溶液应加入 铁粉 以防止其转化为G.检验G溶液中阳离子的常用试剂是 KSCN溶液 ,实验现象为 溶液变成红色 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列烷烃:①正己烷 ②丙烷 ③正戊烷 ④正丁烷 ⑤癸烷中,沸点由高到低的顺序正确的是( )
A.①②③④⑤ B.⑤①③④② C.⑤③④①② D.③④⑤②①
查看答案和解析>>
科目:高中化学 来源: 题型:
关于溶液中微粒的浓度,下列说法正确的是
A.0.1mol·L-1的(NH4)2SO4溶液中:c(SO42-) > c(NH4+) > c(H+) > c(OH-)
B.等浓度等体积的NaHSO3溶液与NaClO溶液混合后:
c(Na+) + c(H+) = c(HSO3-) + c(ClO-) + 2c(SO32-) + c(OH-)
C.等浓度等体积的NaHCO3溶液与NaCl溶液混合后:
1/2 c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
D.标况下,将2.24LSO2气体通入到100ml 1mol·L-1的NaOH溶液中,完全反应
后溶液呈酸性,则该溶液中:c(Na+) > c(HSO3-) > c(SO32-) >c(H+) > c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com