
������Һ������Ũ�ȣ�����˵����ȷ����
A��0.1mol��L-1��(NH4)2SO4��Һ�У�c(SO42-) > c(NH4+) > c(H+) > c(OH-)
B����Ũ�ȵ������NaHSO3��Һ��NaClO��Һ��Ϻ�
c(Na+) + c(H+) = c(HSO3-) + c(ClO-) + 2c(SO32-) + c(OH-)
C����Ũ�ȵ������NaHCO3��Һ��NaCl��Һ��Ϻ�
1/2 c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
D������£���2.24LSO2����ͨ�뵽100ml 1mol��L-1��NaOH��Һ�У���ȫ��Ӧ
����Һ�����ԣ������Һ�У�c(Na+) > c(HSO3-) > c(SO32-) >c(H+) > c(OH-)

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ���������ǣ�������
| �� | A�� | ������Ӧ����������������Һ��Na+��K+��CO32����NO3�� |
| �� | B�� | ���ȳʻ�ɫ����Һ��I����Ba2+��AlO2����Cl�� |
| �� | C�� | c��H+��=1.0��10��13mol/L��Һ��C6H5O����K+��SO42����Br�� |
| �� | D�� | 1.0 mol•L��1��KNO3��Һ��H+��Fe2+��Cl����SO42�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڻ�ѧ���ϣ�Χ��Ũ����Ļ�ѧ���ʽ���������ʵ��̽���������������Ƿ����ձ��У����뼸��ˮ��������ȡ�Ȼ���������Ũ���ᣬѸ�ٽ��裬�ų��������ȣ�ͬʱ�۲쵽������ڣ�������ͣ����ų��д̼�����ζ�����塣��ش�
(1)��ں�,��ɫ���ʻ������Ũ�������ò����������壬���ֺ�ɫ������Ũ�������õĻ�ѧ����ʽΪ__________________________________________________________________
(2)��������Ũ���ᷴӦ��ʵ������˵��Ũ�������_____________������ţ���
A������ B����ˮ�� C����ˮ�� D��ǿ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ö��Ե缫���һ����������ͭ��Һ�����һ��ʱ�������Һ����0.1mol��ʽ̼��ͭ���壨�����ᾧˮ����ǡ��ʹ��Һ�ָ������ǰ��Ũ�Ⱥ�pH�������й���������ȷ���ǣ�������
| �� | A�� | �����̲���������������ڱ�״���£�Ϊ5.6L |
| �� | B�� | ������ת�Ƶĵ�����Ϊ3.612��1023�� |
| �� | C�� | ������ֻ������2CuSO4+2H2O |
| �� | D�� | ����ļ�ʽ̼��ͭ�ķ�Ӧ�ǣ�Cu2��OH��2CO3+2H2SO4�T2CuSO4+CO2��+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
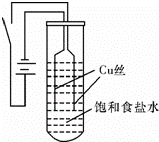
ijУ��ѧ�о���ѧϰС����ͭΪ�缫��ⱥ��ʳ��ˮ��̽���������£�
��ʵ�����ͼװ�ã���Դ��ͨ�����ظ���������ͭ˿���д������ݲ�������������������ͭ˿�ɴֱ�ϸ����ʼ30s�ڣ������������ְ�ɫ���ǣ�Ȼ��ʼ���ֳȻ�ɫ���ǣ���ʱ�ⶨ��Һ��pHԼΪ10�����ų������������ӣ��Ȼ�ɫ���������ۼ����Թܵײ�������Һʼ��δ������ɫ��
��ʵ���ʵ������Թܵײ��ijȻ�ɫ����ȡ������װ����֧С�Թ��У������ܿ�ת��Ϊש��ɫ�������IJ������������£�
| ��� | ���� | ���� |
| �� | ����ϡ���� | ש��ɫ�����ܽ⣬����ɫ���ݲ��������յõ���ɫ��Һ |
| �� | ����ϡ���� | ש��ɫ����ת��Ϊ�Ϻ�ɫ�������Һ����ɫ |
��֪����ͭ�Ļ�������ɫ���£�
| ���� | ��ɫ | ���� | ��ɫ |
| �Ȼ�ͭ | �������ɫ��Ũ��Һ����ɫ��ϡ��Һ����ɫ | ��������ͭ�����ȶ��� | �Ȼ�ɫ |
| ��ʽ�Ȼ�ͭ | ��ɫ | ������ͭ | ��ɫ |
| ������ͭ | ש��ɫ | �Ȼ���ͭ | ��ɫ |
��ش��������⣺
��1��ͭ�ij������ϼ�Ϊ��+1������+2�����ۼ����Թܵײ��ijȻ�ɫ�����Ļ�ѧʽΪ��Cu2O����
��2�������ĵ缫��ӦʽΪ��2Cu+2Cl����2e��=2CuCl������
��3��д��ʵ����Т١��ڵ����ӷ���ʽ���١�3Cu2O+2H++2NO3��=6Cu2++2NO��+7H2O�����ڡ�Cu2O+2H+=Cu+Cu2++H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Al�������г����Ľ�������ҵ���Ʊ���������ԭ�Ͽɴ���������Ҫ�ɷ���
Al2O3��MgO��Fe2O3�ȣ�����ȡ�����������£���ش��������⣺
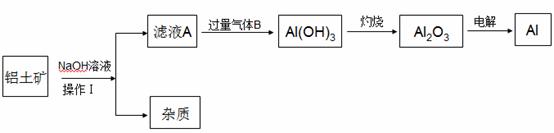
��1���������� ������B�Ļ�ѧʽ��
��2������ҺA����Al(OH)3�����ӷ���ʽ��
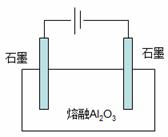 ��3����ҵ�ϲ�����ͼװ�õ������Al2O3�Ʊ����������õ�
��3����ҵ�ϲ�����ͼװ�õ������Al2O3�Ʊ����������õ�
��������ĵ缫��ӦΪ �������һ
��ʱ���������ʯī��ʧ��54g�������ɵ�CO��CO2�����ʵ�
��֮��Ϊ2:1�����������ɵIJ�������Ϊ g��
��4����Ԫ�����ں�ˮ����Ҫ��Be(OH)+��ʽ���ڣ�
����������Ԫ�����ƣ���Be(OH)+��ǿ����Һ��Ӧ�����ӷ���ʽΪ�� ���о�����26Al����˥��Ϊ26Mg�����ԱȽ�������Ԫ�ؽ�����ǿ���ķ����� ��
a���Ƚ�������Ԫ�صĵ��ʵ�Ӳ�Ⱥ��۵�
b�����Ȼ������Ȼ�þ����Һ�зֱ�μӹ���������������Һ
c������ĥ����þ������Ƭ�ֱ����ˮ���ã��������̪��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£����ռ���Һ�м���һ�����Ĺ������ƣ���ַ�Ӧ��ָ���ԭ�¶ȣ�������Һ����˵����ȷ���ǣ�������
| �� | A�� | �о���������Na+ ��Ŀ���� | B�� | �������ݳ���Na+ ��Ŀ���� |
| �� | C�� | Na+��Ŀ���䣬���ʵ������������� | D�� | Na+��Ŀ���٣��������ݳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������У�����һ�����ʵ�������������ֲ�ͬ��
A��MgO��Na2O��CO2��CuO B��HCl��H2O��H2SO4��HNO3 C��NaOH��Na2CO3��KOH��Cu��OH��2
��1���������������ǣ��ѧʽ����A�飺��CO2����B�飺��H2O����C�飺��Na2CO3����
��2�����������ʿ�����һ�������ʣ�д����ˮ��Һ�����ɸ������ʵ����ӷ���ʽ����CO2+H2O+CO32��=2HCO3������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ճ������г����ˡ��ӵ�ʳ�Ρ������������͡�����������Ҷ�������������ࡱ�����ʣ�����ĵ⡢������������Ӧ����Ϊ��������
| �� | A�� | Ԫ�� | B�� | ���� | C�� | ������ | D�� | ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com