
在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
(1)变黑后,黑色物质会继续与浓硫酸作用产生两种气体,这种黑色物质与浓硫酸作用的化学方程式为__________________________________________________________________
(2)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有_____________(填序号)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
有某种含有少量FeCl2杂质的FeCl3样品。现要测定其中铁元素的质量分数,实验采用下列步骤进行:
①准确称量mg样品(在2—3g范围内):
②向样品中加入10mL 6 moL·L-1的盐酸,再加入蒸馏水,配制成250mL溶液:
③量取25mL操作②中配得的溶液,加入3mL氯水,加热使其反应完全;
④趁热迅速加入10%氨水至过量,充分搅拌,使沉淀完全:
⑤过滤,将沉淀洗涤后,移至坩埚,灼烧、冷却、称重,并重复操作至恒重。
试回答下列问题:
(1)溶解样品时,要加入盐酸,原因是 ;
(2)加入氯水后,反应的离子方程式为 ;
(3)加入过量氨水生成沉淀的离子方程式为 ;
(4)若不用氯水,可用下列试剂中的 代替(填序号)。
A.H2O2 B.碘水 C.NaClO
(5)步骤⑤中检验沉淀是否洗净的方法是 。
(6)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为 (请把结果约到最简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G各物质间的关系如图,其中B、D为气态单质.
请回答下列问题:
(1)物质C和E的名称分别为 浓盐酸 、 四氧化三铁 ;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为 2H2O2═2H2O+O2↑ ;若只能在加热情况下进行,则反应物A应为 KClO3 ;
(3)反应②的化学方程式为 4HCl(浓)+MnO2 MnCl2+2H2O+Cl2↑ ;
MnCl2+2H2O+Cl2↑ ;
(4)新配制的F溶液应加入 铁粉 以防止其转化为G.检验G溶液中阳离子的常用试剂是 KSCN溶液 ,实验现象为 溶液变成红色 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列烷烃:①正己烷 ②丙烷 ③正戊烷 ④正丁烷 ⑤癸烷中,沸点由高到低的顺序正确的是( )
A.①②③④⑤ B.⑤①③④② C.⑤③④①② D.③④⑤②①
查看答案和解析>>
科目:高中化学 来源: 题型:
下列哪种说法可以证明反应.N2+3H2 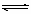 2NH3已达到平衡状态 ( )
2NH3已达到平衡状态 ( )
A.1个N≡N键断裂的同时,有3个H—H键形成
B.1个N≡N键断裂的同时,有3个H—H键断裂
C.1个N≡N键断裂的同时,有2个N—H键断裂
D.1个N≡N键断裂的同时,有6个N—H键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
向溶有10.1g KNO3的水溶液中撒入17.28g 铜粉,微热,铜粉不溶解,慢慢滴入2mol·L-1的稀硫酸,
铜粉开始溶解,溶液显蓝色,并有少量气泡出现。该实验中反应的离子方程式:
3 Cu + 8H+ + 2NO3- == 3 Cu 2+ + 2NO ↑ + 4H2O
(1)当滴入 mL硫酸后铜粉不再溶解;此时烧杯底应该残留 g铜粉;
(2)为使杯底的铜粉全部溶解,在加入足量硫酸的前提下,还应该再加入至少 g KNO3固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国斯坦福大学研究人员发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl.下列有关“水”电池在海水中放电时的说法正确的是( )
|
| A. | 负极反应式:Ag+Cl﹣+e﹣═AgCl |
|
| B. | 电池的正极用二氧化锰纳米棒为材料,可大大提高发电效率 |
|
| C. | Na+不断向“水”电池的负极移动 |
|
| D. | 每转移2 mol电子,正极就有5 mol MnO2被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于溶液中微粒的浓度,下列说法正确的是
A.0.1mol·L-1的(NH4)2SO4溶液中:c(SO42-) > c(NH4+) > c(H+) > c(OH-)
B.等浓度等体积的NaHSO3溶液与NaClO溶液混合后:
c(Na+) + c(H+) = c(HSO3-) + c(ClO-) + 2c(SO32-) + c(OH-)
C.等浓度等体积的NaHCO3溶液与NaCl溶液混合后:
1/2 c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
D.标况下,将2.24LSO2气体通入到100ml 1mol·L-1的NaOH溶液中,完全反应
后溶液呈酸性,则该溶液中:c(Na+) > c(HSO3-) > c(SO32-) >c(H+) > c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中Cl-的物质的量浓度与50mL 1mol?L-1 AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A.150mL 1mol?L-1的NaCl溶液 |
| B.50mL 1mol?L-1的CaCl2溶液 |
| C.150mL 3mol?L-1的KCl溶液 |
| D.150mL 3mol?L-1的MgCl2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com