
【题目】下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑥ | ⑧ | ⑩ | |||||
三 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
四 | ② | ④ |
(1)在这10种元素中,化学性质最不活泼的元素是________ (写序号),得电子能力最强的原子是________ (用元素符号表示);元素⑦的最高价氧化物对应的水化物是________________ (写化学式)。
(2)元素④的离子结构示意图为________________。
(3span>)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示) ________________。
(4)请写出:
(i)③的单质置换出⑥的单质的化学方程式: ________________________。
(ii)①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式为____________________。
(iii)②和⑨两种元素最高价氧化物对应的水化物相互反应的离子方程式为____________________。
【答案】⑩ F H3PO4 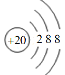 Cl>F>Na+ 2Mg+CO2
Cl>F>Na+ 2Mg+CO2![]() 2MgO+C Al(OH)3+NaOH=NaAlO2+2H2O H++OH=H2O
2MgO+C Al(OH)3+NaOH=NaAlO2+2H2O H++OH=H2O
【解析】
由元素在周期表中位置,可知①为Na、②为K、③为Mg、④为Ca、⑤为Al、⑥为C、⑦为P、⑧为F、⑨为Cl、⑩为Ne。
(1)用在这10种元素中,化学性质最不活泼的元素是⑩,氟的非金属性最强,所以得电子能力最强的原子是F;元素⑦为P,其最高价氧化物对应的水化物是H3PO4,故答案为:⑩;F;H3PO4;
(2)元素④是钙元素,失去两个电子形成钙离子,离子结构示意图为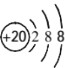 ,故答案为:
,故答案为: ;
;
(3)电子层数越多,半径越大;电子层数相同,核电荷数越小,半径越大,所以①、⑧、⑨三种元素单核离子半径由大到小的顺序是Cl->F->Na+,故答案为:Cl->F->Na+;
(4)(i)③的单质为Mg,⑥的单质为C,镁置换出碳的化学方程式为2Mg+CO2![]() 2MgO+C,故答案为:2Mg+CO2
2MgO+C,故答案为:2Mg+CO2![]() 2MgO+C;
2MgO+C;
(ii)①和⑤两种元素最高价氧化物对应的水化物分别为氢氧化钠和氢氧化铝,相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+
2H2O,故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;
(iii)②和⑨两种元素最高价氧化物对应的水化物分别为KOH和HCl,相互反应的离子方程式为H++OH-=H2O,故答案为:H++OH-=
H2O。


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】
绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(1)基态Al原子中,电子填充的最高能级是_______,基态Cr原子的价电子排布式是_____。
(2)用“>”或“<”填空:
第一电离能 | 键能 | 沸点 | 离子半径 |
Be_____B | C—C_____Si—Si | H2S_____H2O | Al3+_____O2- |
(3)BeCl2分子的空间构型是______,它的二聚体Be2Cl4结构如右图所示,其中Be原子的杂化方式是_____。
![]()

(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式______。
(5)Be的氧化物的立方晶胞结构如右图所示,已知氧化铍晶体的密度为ρg·cm-3,则晶胞连长为___cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a mol Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排出气体为两种气体时,a︰b不可能为
A. 3︰4 B. 3︰2 C. 2︰3 D. 4︰5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为相关物质间的转化关系,其中甲、丙为生活中常见的金属单质,乙、丁为非金属单质且丁为气态,E为白色沉淀,D为浅绿色溶液。请回答:

(1)组成甲的元素在元素周期表中的位置为____________,请列举乙单质的一种用途__________,用电子式表示丁的形成过程________________________
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是________________(化学式)
(3)反应①的离子方程式为____________________________
(4)将B的稀溶液加水稀释,在图中画出溶液的pH随加水体积的变化趋势曲线。__________

(5)将等物质的量的A和NaOH混合溶于水,该溶液中离子的物质的量浓度由大到小的顺序为:________________________
(6)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为________________________________________,小辉同学欲设计实验,验证D溶液中的阳离子尚未完全被氧化,请你将实验过程补充完整:取反应液少许于试管中,滴加______________________,则证明D中的阳离子未完全被氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强,食品添加亚硝酸钠必须严格控制用量。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液PH
用PH试纸分别测定0.1mol·L-1两种盐溶液的PH,测得NaNO2溶液呈碱性。NaNO2溶液呈碱性的原因是 ________________________(用离子方程式解释)。NaNO2溶液中c(HNO2)=_____________(用溶液中其它离子的浓度关系式表示)
(2)沉淀法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液。两只试管均产生白色沉淀。分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。
该温度下Ksp(AgNO2)=2×10-8(mol·L-1)2; Ksp(AgCl)=1.8×10-10(mol·L-1)2
则反应AgNO2(s) +Cl-(aq)![]() AgCl(s)+ NO2-(aq)的化学平衡常数K=__________
AgCl(s)+ NO2-(aq)的化学平衡常数K=__________
(3)氧化法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴酸性KMnO4溶液。使酸性KMnO4溶液褪色的是NaNO2溶液。该反应的离子方程式为____________。
㈡NaNO2性质探究
该兴趣小组同学用下图装置探究亚硝酸钠与硫酸反应及气体产物成分。
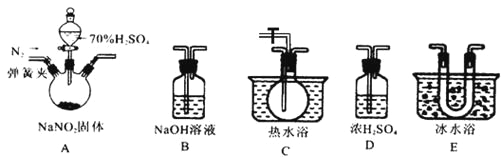
已知: 气体液化的温度:NO221℃ 、 NO –152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→______→ ______→_______→_______;组装好仪器后,接下来进行的操作是________________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①如何确认A中产生气体是否含有NO _________。(写出实验操作、现象和结论)
②装置E的作用是_______________________。
③若向D中通入过量O2,则装置B中发生反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华优秀传统文化涉及到很多的化学知识。下列有关说法不正确的是![]()
![]()
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.“火树银花合,星桥铁索开”,其中的“火树银花”涉及到焰色反应
C.![]() 天工开物
天工开物![]() 中记载:“以硝石、硫磺为主。草木灰为辅。
中记载:“以硝石、硫磺为主。草木灰为辅。![]() 魂散惊而魄齑粉”文中提到的是火药
魂散惊而魄齑粉”文中提到的是火药
D.![]() 天工开物
天工开物![]() 中有如下描述:“世间丝、麻、裘、褐皆具素质
中有如下描述:“世间丝、麻、裘、褐皆具素质![]() ”文中的“裘”主要成分是蛋白质
”文中的“裘”主要成分是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人曾建议用AG表示溶液的酸度(acidity),AG的定义为AG=lg![]() ,下列表述正确的是
,下列表述正确的是
A. 25 ℃时,若溶液呈中性,则pH=7,AG=1
B. 25 ℃时,若溶液呈酸性,则pH<7,AG<0
C. 25 ℃时,若溶液呈碱性,则pH>7,AG>0
D. 25 ℃时,溶液的pH与AG的换算公式为AG=2(7-pH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,古代文献中记载了很多化学研究成果。下列常见古诗文对应化学知识正确的是![]()
选项 | 古诗文 | 化学知识 |
A |
| 冰能量低于水,冰变为水属于吸热反应 |
B |
| “强水”是指氢氟酸 |
C |
| 剂钢为铁的合金,其硬度比纯铁的大,熔点比纯铁的高 |
D |
| 鉴别硝石和朴硝利用了焰色反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3
C.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
D.加入催化剂有利于氨的合成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com