
【题目】把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol/L硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图所示的坐标曲线来表示,请回答下列问题:
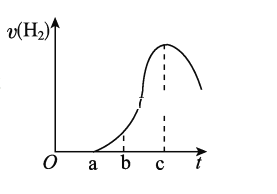
(1)曲线由O→a段不产生氢气的原因是___________________________,有关的化学方程式为___________________________________________。
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_____________________。
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________。
【答案】铝片表面有Al2O3,硫酸首先与Al2O3反应 Al2O3+3H2SO4=Al2(SO4)3+3H2O 反应放出的热量使溶液的温度升高,加快反应速率 c点以后,硫酸的浓度逐渐变小,该因素变为影响反应速率的主要因素,使反应速率减小
【解析】
由图可知,开始不生成氢气,为氧化铝与硫酸的反应,然后Al与硫酸反应生成氢气,开始温度较低,由于反应放热,则温度升高,反应速率加快,后来,氢离子浓度减小,则反应速率减小,据此分析解答。
(1)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,氧化铝首先与稀硫酸反应生成硫酸铝和水,不产生H2,方程式为Al2O3+3H2SO4=Al2(SO4)3+3H2O,故答案为:铝片表面有Al2O3,硫酸首先与Al2O3反应;Al2O3+3H2SO4=Al2(SO4)3+3H2O;
(2)金属和酸的反应是放热反应,使溶液的温度升高,温度升高,化学反应速率加快,故答案为:反应放出的热量使溶液的温度升高,加快反应速率;
(3)随着反应的进行,溶液中的氢离子浓度逐渐降低,此时氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小;故答案为:c点以后,硫酸的浓度逐渐变小,该因素变为影响反应速率的主要因素,使反应速率减小。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】下列化学方程式书写错误的是( )
A.NaHCO3水解的离子方程式:HCO3-+ H2O![]() CO32-+H3O+
CO32-+H3O+
B.NH4Cl水解的化学方程式:NH4Cl+H2O![]() NH3·H2O+HCl
NH3·H2O+HCl
C.Al(OH)3的两性电离方程式:H++AlO2-+H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH
Al3++3OH
D.NaHSO3的电离方程式:NaHSO3=Na++HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中正确的是( )
![]()
A.Y的价层电子排布式是![]()
B.四种元素所形成的最简单氢化物中,沸点最高的是可能Y的氢化物
C.Y、Z之间可形成离子型化合物
D.X、Z、W的最高价氧化物所对应的水化物不可能均是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入lmolCO2和3mo1H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入lmolCO2和3mo1H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是

A. 升高温度平衡常数K增大
B. 反应达到平衡状态时,CO2的平衡转化率为75%
C. 3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D. 从反应开始到平衡,H2的平均反应速率v(H2)=0.075 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界______。
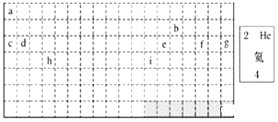
(2)表中所列元素,属于短周期元素的有______(用元素符号回答),属于主族元素的有______(用元素符号回答)。
(3)g元素位于第______周期第______族;i元素位于第______周期第______族。
(4)元素f是第______周期第______族元素,请按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量_________。
(5)写出b元素的基态原子的电子排布式______,写出h元素的符号______,该原子的价层电子排布图______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。
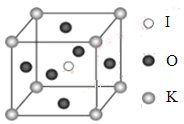
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2A2(g)+B2(g)![]() 2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
(1)a___(填“>”“=”或“<”)b。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将___(填“增大”“减小”或“不变”)。
(3)若在原来的容器中只加入2 mol C,500 ℃时充分反应达到平衡后,吸收热量c kJ,C的浓度___(填“>”“=”或“<”)w mol·L-1。
(4)能说明该反应已经达到平衡状态的是___。
a.v(C)=2v(B2) b.容器内压强保持不变c.v逆(A2)=2v正(B2)d.容器内气体的密度保持不变
(5)使该反应的反应速率增大,且平衡向正反应方向移动的操作是___。
a.及时分离出C气体b.适当升高温度c.增大B2的浓度 d.选择高效的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A.0.1molC4H4(键线式:![]() )含共价键数目为0.4NA
)含共价键数目为0.4NA
B.30g冰醋酸和乳酸(C3H6O3)的混合物中含氢原子的数目为2NA
C.常温下,0.5mol/L的氨水溶液中氢氧根数目小于0.5NA
D.6.4g铜粉与3.2g硫粉混合隔绝空气加热充分反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基钠(NaNH2)常用作有机合成的促进剂,是合成维生素 A 的原料。某学习小组用如下装置,以NH3和Na为原料加热至 350-360 ℃制备氨基钠,并检验其生成的产物和测定产品的纯度。
已知:NaNH2极易水解且易被空气氧化。回答下列问题 :
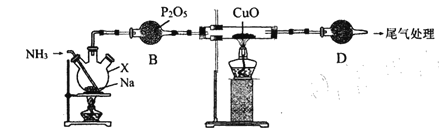
A C
(1)仅从试剂性质角度分析,下列各组试剂不宜用于实验室制备NH3的是________(填字母序号)。
A.浓氨水、CaO B. NH4Cl固体、Ca(OH)2固体
C.浓氨水 D.NH4NO3固体 、NaOH固体
(2)仪器D名称为___________,其中盛放的试剂为 ___________。
(3)装置A中发生反应的化学方程式为 __________,能证明装置A中已发生反应的实验依据是__________________________ 。
(4) 装置B的作用是______________ 。
(5) 制备时,通入的氨气过量,待钠充分反应后,取 mg 产品, 按如图装置进行实验(产品所含杂质仅为 Na2O )。
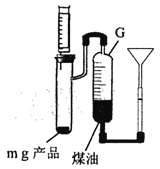
用注射器向试管中缓慢加入H2O至恰好完全反应立即停止,G中液面从刻度V1变 为 V2(已知V2>Vi,单位 mL,忽略固体体积,读取刻度时保持两使液面相平,实验过程处于标准状况下),则产品纯度为________:若读取V1时,G中液面低于漏斗侧液面,则所测得的纯度比实际产品纯度_________(填“偏高”、“ 偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com