
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中正确的是( )
![]()
A.Y的价层电子排布式是![]()
B.四种元素所形成的最简单氢化物中,沸点最高的是可能Y的氢化物
C.Y、Z之间可形成离子型化合物
D.X、Z、W的最高价氧化物所对应的水化物不可能均是强酸
【答案】B
【解析】
A.题中信息无法确定Y位置,则Y的价层电子排布式不一定为ns2np5,故A错误;
B.根据X、Y、Z、W在周期表中的相对位置可知,Y可能为C、N、O,当Y为N时,形成的最简单氢化物为氨气,分子间能够形成氢键,沸点最高,当Y为O时,X为N,Z为S,W为Cl,水常温下为液体,水的沸点最高,故B正确;
C.根据X、Y、Z、W在周期表中的相对位置可知,Y可能为C、N、O,Y、Z同主族,且为短周期元素,二者形成的化合物只含有共价键,不可能形成离子化合物,故C错误;
D.当X、Z、W分别为N、S、Cl时,对应最高价含氧酸分别为硝酸、硫酸和高氯酸,都是强酸,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】向一体积为2L的恒容密闭容器里充入1 mol N2和4 molH2,在一定温度下发生反应: N2(g)+3H2(g)![]() 2NH3(g);△H<0。10秒后达到平衡,c(NH3)为0.4mol/L。下列说法正确的是
2NH3(g);△H<0。10秒后达到平衡,c(NH3)为0.4mol/L。下列说法正确的是
A. 该反应达平衡时H2的转化率为40%
B. 降低温度能使混合气体的密度增大
C. 向该容器中充入N2,平衡正向移动
D. 研发高效催化剂可大大提高N2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列判断中正确的是

A. 用装置①模拟研究时未见a上有气泡产生,说明铁棒没有被腐蚀
B. ②中桥墩与外加电源正极连接能确保桥墩不被腐蚀
C. ③中采用了牺牲阳极的阴极保护法保护桥墩
D. ①②③中海水均是实现化学能转化为电能的电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子核外p能级、d能级等原子轨道上电子排布为“全空”“半满”“全满”的时候一般更加稳定,称为洪特规则的特例。下列事实不能作为这个规则的证据的是( )
A.硼元素的第一电离能小于铍元素的第一电离能
B.磷元素的第一电离能大于硫元素的第一电离能
C.基态铜原子的核外电子排布式为![]() 而不是
而不是![]()
D.某种激发态碳原子的核外电子排布式为![]() 而不是
而不是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将饱和FeCl3溶液滴入沸水时,液体变为红褐色,得到的是Fe(OH)3胶体。用此分散系进行实验:
(1)将其装入U形管内,用石墨做电极,接通直流电源,通电一段时间后发现阴极附近颜色___,这表明_____(根据微粒电性作答),这种现象称为______。
(2)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察(填写“有”或“无”)____丁达尔现象,这个实验可以用来区别____;再向烧杯中加入用稀硝酸化的硝酸银溶液,可观察到的现象为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮硫的氧化物是造成大气污染的主要物质。研究它们的反应机理,对于消除环境污染有重要意义。
(1)2NO(g)+O2(g)=2NO2(g)△H的反应机理和各基元反应(基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应)的活化能为:
2NO(g)![]() N2O2(g)E1=82kJ·mol-1v=k1c2(NO)
N2O2(g)E1=82kJ·mol-1v=k1c2(NO)
N2O2(g)![]() 2NO(g)E-1=205kJ·mol-1v=k-1c(N2O2)
2NO(g)E-1=205kJ·mol-1v=k-1c(N2O2)
N2O2(g)+O2(g)![]() 2NO2(g)E2=82kJ·mol-1v=k2c(N2O2)·c(O2)
2NO2(g)E2=82kJ·mol-1v=k2c(N2O2)·c(O2)
2NO2(g)![]() N2O2(g)+O2(g)E-2=72kJ·mol-1v=k-2c2(NO2)
N2O2(g)+O2(g)E-2=72kJ·mol-1v=k-2c2(NO2)
①2NO(g)+O2(g)![]() 2NO2(g)△H=______kJmol-1,平衡常数K与上述反应速率常数k1、k-1、k2、k-2的关系式为K=_______;
2NO2(g)△H=______kJmol-1,平衡常数K与上述反应速率常数k1、k-1、k2、k-2的关系式为K=_______;
②某温度下反应2NO(g)+O2(g)![]() 2NO2(g)的速率常数k=8.8×10-2L2mol-2s-1,当反应物浓度都是0.05molL-1时,反应的速率是__________________molL-1s-1;若此时缩小容器的体积,使气体压强增大为原来的2倍,则反应速率增大为之前的______倍。
2NO2(g)的速率常数k=8.8×10-2L2mol-2s-1,当反应物浓度都是0.05molL-1时,反应的速率是__________________molL-1s-1;若此时缩小容器的体积,使气体压强增大为原来的2倍,则反应速率增大为之前的______倍。
(2)2SO2(g)+O2(g)![]() 2SO3(g)反应过程中能量变化如图1所示。在V2O5存在时,该反应的机理为:V2O5+SO2
2SO3(g)反应过程中能量变化如图1所示。在V2O5存在时,该反应的机理为:V2O5+SO2![]() 2VO2+SO3(快)4VO2+O2
2VO2+SO3(快)4VO2+O2![]() 2V2O5(慢)
2V2O5(慢)
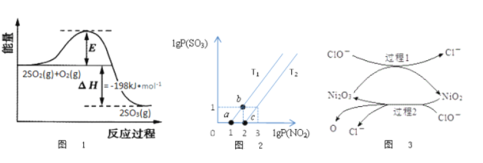
下列说法正确的是___________
A.反应速率主要取决于V2O5的质量
B.VO2是该反应的催化剂
C.逆反应的活化能大于198kJ/mol
D.增大SO2的浓度可显著提高反应速率
(3)某研究小组研究T1℃、T2℃时,氮硫的氧化物的转化:NO2(g)+SO2(g)![]() NO(g)+SO3(g)中lgP(NO2)和lgP(SO3)关系如图2所示,实验初始时体系中的P(NO2)和P(SO2)相等、P(NO)和P(SO3)相等。
NO(g)+SO3(g)中lgP(NO2)和lgP(SO3)关系如图2所示,实验初始时体系中的P(NO2)和P(SO2)相等、P(NO)和P(SO3)相等。
①根据题意可知:T1______T2(填“>”“<”或者“=”),理由是___________________。
②由平衡状态a到b,改变的条件是__________________。
(4)工业上可用NaClO碱性溶液或“亚硫酸盐法”吸收SO2。为了提高吸收效率,常用Ni2O3作为催化剂。催化过程如图3所示。
①过程2的离子方程式_______________________________。
②Ca(C1O)2也可用于脱硫,且脱硫效果比NaC1O更好,原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol/L硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图所示的坐标曲线来表示,请回答下列问题:
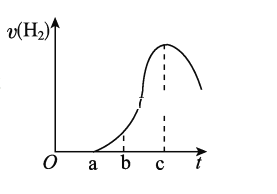
(1)曲线由O→a段不产生氢气的原因是___________________________,有关的化学方程式为___________________________________________。
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_____________________。
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2常用陶瓷材料,可由锆英砂(主要成分为ZrSiO4, 也可表示为ZrO2SiO2还含少量FeCO3、Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取:
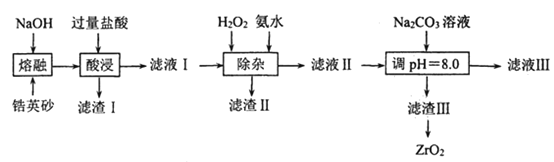
已知:①ZrSiO4能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+;
②常温下,Ksp[Fe(OH)3= 1×10-38,Ksp [(Al(OH)3= 1×10-32;pH=6.2时,ZrO2+开始沉淀.
(1)“熔融”过程中 ,ZrSiO4发生反应的化学方程式为______________________;滤渣 I的化学式为________________________。
(2)“除杂”过程中,加入双氧水的目的是________________:此过程中为使滤液I中的杂质离子沉淀完全而除去(当离子浓度c≤1×10-5 molL-1时即为沉淀完全) ,室温下加氪水调节pH范围为____________________。
(3)为得到纯净的ZrO2滤渣III要用水洗,检验沉淀是否洗涤干净的方法是_______。
(4)滤渣III的成分是Zr(CO3)2 nZr(OH)4。“调 pH=8.0”时,所发生反应的离子方程式为_______________________;滤渣III制备ZrO2的方法是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com