
【题目】氮硫的氧化物是造成大气污染的主要物质。研究它们的反应机理,对于消除环境污染有重要意义。
(1)2NO(g)+O2(g)=2NO2(g)△H的反应机理和各基元反应(基元反应是指在反应中一步直接转化为产物的反应,又称为简单反应)的活化能为:
2NO(g)![]() N2O2(g)E1=82kJ·mol-1v=k1c2(NO)
N2O2(g)E1=82kJ·mol-1v=k1c2(NO)
N2O2(g)![]() 2NO(g)E-1=205kJ·mol-1v=k-1c(N2O2)
2NO(g)E-1=205kJ·mol-1v=k-1c(N2O2)
N2O2(g)+O2(g)![]() 2NO2(g)E2=82kJ·mol-1v=k2c(N2O2)·c(O2)
2NO2(g)E2=82kJ·mol-1v=k2c(N2O2)·c(O2)
2NO2(g)![]() N2O2(g)+O2(g)E-2=72kJ·mol-1v=k-2c2(NO2)
N2O2(g)+O2(g)E-2=72kJ·mol-1v=k-2c2(NO2)
①2NO(g)+O2(g)![]() 2NO2(g)△H=______kJmol-1,平衡常数K与上述反应速率常数k1、k-1、k2、k-2的关系式为K=_______;
2NO2(g)△H=______kJmol-1,平衡常数K与上述反应速率常数k1、k-1、k2、k-2的关系式为K=_______;
②某温度下反应2NO(g)+O2(g)![]() 2NO2(g)的速率常数k=8.8×10-2L2mol-2s-1,当反应物浓度都是0.05molL-1时,反应的速率是__________________molL-1s-1;若此时缩小容器的体积,使气体压强增大为原来的2倍,则反应速率增大为之前的______倍。
2NO2(g)的速率常数k=8.8×10-2L2mol-2s-1,当反应物浓度都是0.05molL-1时,反应的速率是__________________molL-1s-1;若此时缩小容器的体积,使气体压强增大为原来的2倍,则反应速率增大为之前的______倍。
(2)2SO2(g)+O2(g)![]() 2SO3(g)反应过程中能量变化如图1所示。在V2O5存在时,该反应的机理为:V2O5+SO2
2SO3(g)反应过程中能量变化如图1所示。在V2O5存在时,该反应的机理为:V2O5+SO2![]() 2VO2+SO3(快)4VO2+O2
2VO2+SO3(快)4VO2+O2![]() 2V2O5(慢)
2V2O5(慢)
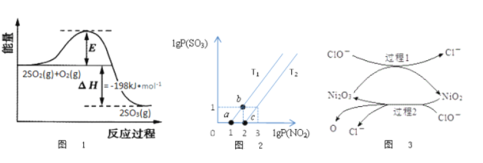
下列说法正确的是___________
A.反应速率主要取决于V2O5的质量
B.VO2是该反应的催化剂
C.逆反应的活化能大于198kJ/mol
D.增大SO2的浓度可显著提高反应速率
(3)某研究小组研究T1℃、T2℃时,氮硫的氧化物的转化:NO2(g)+SO2(g)![]() NO(g)+SO3(g)中lgP(NO2)和lgP(SO3)关系如图2所示,实验初始时体系中的P(NO2)和P(SO2)相等、P(NO)和P(SO3)相等。
NO(g)+SO3(g)中lgP(NO2)和lgP(SO3)关系如图2所示,实验初始时体系中的P(NO2)和P(SO2)相等、P(NO)和P(SO3)相等。
①根据题意可知:T1______T2(填“>”“<”或者“=”),理由是___________________。
②由平衡状态a到b,改变的条件是__________________。
(4)工业上可用NaClO碱性溶液或“亚硫酸盐法”吸收SO2。为了提高吸收效率,常用Ni2O3作为催化剂。催化过程如图3所示。
①过程2的离子方程式_______________________________。
②Ca(C1O)2也可用于脱硫,且脱硫效果比NaC1O更好,原因是________________。
【答案】-113 ![]() 1.1×10-5 8 CD < 该反应为放热反应,温度越高,Kp越小 将容器体积缩小为原来的0.1 2NiO2+ClO-=Ni2O3+Cl-+2O Ca2+和SO42-结合生成微溶的硫酸钙,有利于反应的进行
1.1×10-5 8 CD < 该反应为放热反应,温度越高,Kp越小 将容器体积缩小为原来的0.1 2NiO2+ClO-=Ni2O3+Cl-+2O Ca2+和SO42-结合生成微溶的硫酸钙,有利于反应的进行
【解析】
根据基元反应原理,总反应可分为几步简单反应,可逆反应存在正反两方向的简单反应,寻找规律,速率常数k等于反应物的浓度的反应系数指数幂乘积,据此回答问题。
(1)①根据基元反应含义,第1、3反应为正方向的2个基元反应,第2、4为逆方向的2个基元反应,2NO(g)+O2(g)![]() 2NO2(g)△H=E2+E1-E-1-E-1=-113kJmol-1,平衡常数K=
2NO2(g)△H=E2+E1-E-1-E-1=-113kJmol-1,平衡常数K=![]() ,反应到达平衡时,v正=v逆,所以k1c2(NO)= k-1c(N2O2),k2c(N2O2)·c(O2)= k-2c2(NO2),则有
,反应到达平衡时,v正=v逆,所以k1c2(NO)= k-1c(N2O2),k2c(N2O2)·c(O2)= k-2c2(NO2),则有![]() ;
;
②某温度下反应2NO(g)+O2(g)![]() 2NO2(g)的速率常数k=8.8×10-2L2mol-2s-1,当反应物浓度都是0.05molL-1时,反应的速率为
2NO2(g)的速率常数k=8.8×10-2L2mol-2s-1,当反应物浓度都是0.05molL-1时,反应的速率为![]() molL-1s-1;若此时缩小容器的体积,使气体压强增大为原来的2倍,浓度增大为原来的2倍,则反应速率增大为之前的23=8倍。
molL-1s-1;若此时缩小容器的体积,使气体压强增大为原来的2倍,浓度增大为原来的2倍,则反应速率增大为之前的23=8倍。
(2)A.V2O5的质量不影响反应速率,反应速率取决于慢反应速率,A错误;
B.VO2是该反应的中间态,并非催化剂,催化剂为V2O5,B错误;
C.生成物总能量低,逆反应的活化能大于198kJ/mol,C正确;
D.根据有效碰撞理论,增大SO2的浓度可显著提高反应速率,D正确;
答案为CD。
(3)①根据题意可知:T1<T2,理由是该反应为放热反应,温度越高,Kp越小。
②根据坐标可知,由平衡状态a到b,改变的条件是将容器体积缩小为原来的0.1。
(4)工业上可用NaClO碱性溶液或“亚硫酸盐法”吸收SO2。为了提高吸收效率,常用Ni2O3作为催化剂。
①从箭头指向可知,过程2的离子方程式2NiO2+ClO-=Ni2O3+Cl-+2O。
②Ca(C1O)2也可用于脱硫,且脱硫效果比NaC1O更好,原因是Ca2+和SO42-结合生成微溶的硫酸钙,有利于反应的进行。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:
【题目】如图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述错误的是( )注:氨气在水中溶解度(体积比——V水:V气=
1:700,CO2在水中溶解度1:1。

A.A气体是NH3,B气体是CO2
B.侯氏制碱法的工艺流程应用了物质溶解度的差异
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家设计了如下图装置,反应完毕,电解质溶液的pH保持不变。下列说法正确的是
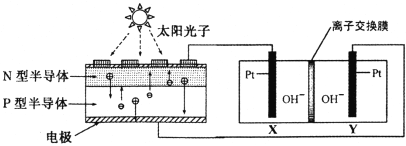
A. 图中N型半导体为正极,P型半导体为负极
B. Y 电极的反应:4OH--4e-=2H2O +O2↑
C. 图中离子交换膜为阳离子交换膜
D. 该装置实现了“太阳能→化学能→电能”的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用如下方法制取Cl2,根据相关信息,回答下列问题:
(1)在该反应中,HCl表现的性质有______、________.
①MnO2 +4HCl(浓)![]() Cl2↑+ MnCl2+ 2H2O
Cl2↑+ MnCl2+ 2H2O
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为________(填化学式),被氧化物质的物质的量为 _____,同时转移电子数为_____(用NA表示)。
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为_________,将此产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______。
(4)②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____。
(5)已知反应4HCl(g)+O2  2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中正确的是( )
![]()
A.Y的价层电子排布式是![]()
B.四种元素所形成的最简单氢化物中,沸点最高的是可能Y的氢化物
C.Y、Z之间可形成离子型化合物
D.X、Z、W的最高价氧化物所对应的水化物不可能均是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】间氯苯甲醛是新型农药、医药等有机合成的中间体,是重要的有机化工产品。实验室制取间氯苯甲醛的过程如下。
Ⅰ.Cl2的制备
舍勒发现氯气的方法至今还用于实验室制备氯气。本实验中利用该方法制备Cl2。
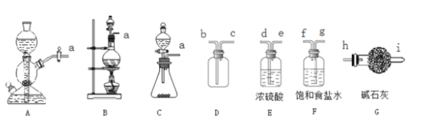
(1)该方法可以选择图中的_____(填字母标号)为Cl2发生装置,反应中氧化剂和还原剂的物质的量之比为_______。
(2)选择图中的装置收集一瓶纯净干燥的Cl2,接口的连接顺序为a→___________(按气流方向,填小写字母标号)
(3)试用平衡移动原理解释用饱和食盐水除去Cl2中混有的HCl的原因:_____________________。
Ⅱ.间氯苯甲醛的制备
反应原理:
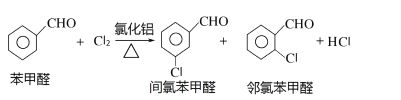
实验装置和流程如图所示:
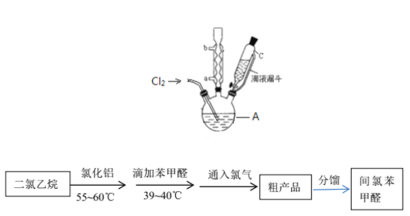
(4)图中仪器A的名称是_____________。
(5)间氯苯甲醛的制备过程中,二氯乙烷的作用是________________________;该实验要求无水操作,理由是____________________________________________;该实验有两次恒温过程,为控制反应温度仪器A处可采用________加热的方法。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入lmolCO2和3mo1H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入lmolCO2和3mo1H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是

A. 升高温度平衡常数K增大
B. 反应达到平衡状态时,CO2的平衡转化率为75%
C. 3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D. 从反应开始到平衡,H2的平均反应速率v(H2)=0.075 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。
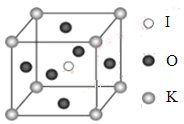
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com