
【题目】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界______。
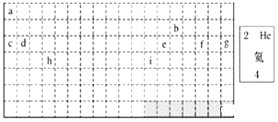
(2)表中所列元素,属于短周期元素的有______(用元素符号回答),属于主族元素的有______(用元素符号回答)。
(3)g元素位于第______周期第______族;i元素位于第______周期第______族。
(4)元素f是第______周期第______族元素,请按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量_________。
(5)写出b元素的基态原子的电子排布式______,写出h元素的符号______,该原子的价层电子排布图______。
【答案】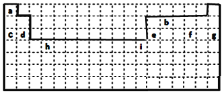 H、C、Na、Mg、Al、S、Ar H、C、Na、Mg、Al、S 三 0 四 ⅡB 三 VIA
H、C、Na、Mg、Al、S、Ar H、C、Na、Mg、Al、S 三 0 四 ⅡB 三 VIA 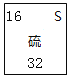 1s22s22p2 Ti
1s22s22p2 Ti ![]()
【解析】
(1)上边界为短周期元素,一周期有2种元素,位于1、18列,二、三周期有8种元素,位于1、2列及13~18列;
(2)第一、二、三周期为短周期;主族元素处于第1列、第2列、第13列~第17列元素;
(3)由元素在周期表中位置可知,g元素位于第三周期0族;i元素位于第四周期ⅡB族;
(4)f为S,处于第三周期第VIA族,名称为硫,原子序数为16,相对原子质量为32;
(5)b为C元素,核外电子数为6,处于第二周期第IVA族;h为Ti,处于第四周期第IVB族,价电子排布式为3d24s2。
(1)上边界为短周期元素,一周期有2种元素,位于1、18列,二、三周期有8种元素,位于1、2列及13~18列,用实线补全元素周期表的边界为: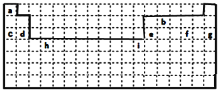 ,故答案为:
,故答案为: ;
;
(2)第一、二、三周期为短周期,由元素在周期表中位置可知,表中H、C、Na、Mg、Al、S、Ar共7种元素为短周期元素;主族元素处于第1列、第2列、第13列~第17列元素,故主族元素有H、C、Na、Mg、Al、S,故答案为:H、C、Na、Mg、Al、S、Ar;H、C、Na、Mg、Al、S;
(3)由元素在周期表中位置可知,g元素位于第三周期0族;i元素位于第四周期ⅡB族,故答案为:三;0;四;ⅡB;
(4)f为S,处于第三周期第VIA族,名称为硫,原子序数为16,相对原子质量为32,硫元素的式样如图为 ,故答案为:三;VIA;
,故答案为:三;VIA; ;
;
(5)b为C元素,核外电子数为6,处于第二周期第IVA族,基态原子的电子排布式为1s22s22p2;h为Ti,处于第四周期第IVB族,价电子排布式为3d24s2,价电子排布图为![]() ,故答案为:1s22s22p2;Ti;
,故答案为:1s22s22p2;Ti;![]() 。
。


科目:高中化学 来源: 题型:
【题目】(1)25 ℃时,0.1 mol·L-1NaOH溶液的pH为________;
(2)25 ℃时,0.1 mol·L-1NH4Cl溶液的pH________7(填“<”、“=”或“>”),其原因是__________________(用离子方程式表示);
(3)将上述两种溶液等体积混合后,离子浓度大小次序正确的是________(填序号)。
A.[Na+]>[Cl-]>[OH-]>[H+] |
B.[Na+]=[Cl-]>[H+]>[OH-] |
C.[Na+]=[Cl-]>[OH-]>[H+] |
D.[Cl-]>[Na+]>[OH-]>[H+] |
(4)25 ℃时,0.1 mol·L-1NaOH溶液中水电离出来的氢氧根的浓度为C1,0.1 mol·L-1NH4Cl溶液中水电离出来的氢离子的浓度为C2,则C1______C2(填“<”、“=”或“>”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将饱和FeCl3溶液滴入沸水时,液体变为红褐色,得到的是Fe(OH)3胶体。用此分散系进行实验:
(1)将其装入U形管内,用石墨做电极,接通直流电源,通电一段时间后发现阴极附近颜色___,这表明_____(根据微粒电性作答),这种现象称为______。
(2)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察(填写“有”或“无”)____丁达尔现象,这个实验可以用来区别____;再向烧杯中加入用稀硝酸化的硝酸银溶液,可观察到的现象为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内的气体是( )
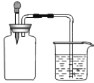
① CO、O2 ② Cl2、CH4 ③ NO2、O2 ④ N2、H2
A.①②B.②C.③④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol/L硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图所示的坐标曲线来表示,请回答下列问题:
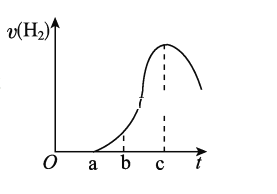
(1)曲线由O→a段不产生氢气的原因是___________________________,有关的化学方程式为___________________________________________。
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_____________________。
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知299 K时,合成氨反应 N2(g ) + 3H2 ( g )![]() 2NH3( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
A. 一定大于92.0 kJB. 一定等于92.0 kJ
C. 一定小于92.0 kJD. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A. Na2CO3 B. Na2O2、Na2CO3
C. NaOH、Na2CO3 D. Na2O2、NaOH、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素A形成气态的A2分子共有3种,其分子量分别为158、160、162,此三种分子的物质的量之比为7:10:7,则下列说法正确的是( )
A.该元素具有三种同位素
B.A的一种同位素的质量数为80
C.三种分子的平均相对分子质量为159
D.A的各种同位素的原子个数百分组成相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com