
����Ŀ��Ī���Σ�(NH4)2Fe(SO4)26H2O��Mr��392����һ����Ҫ�Ļ�ԭ�����ڿ����б�һ����������ȶ���ijѧϰС���������ʵ���Ʊ�������Ī���β��ⶨ�䴿�ȡ�

�ش��������⣺
����ȡĪ����
��1������װ�ã����װ�������ԡ���0.1mol��NH4��2SO4���������ڲ���������______�����������ƣ�����6.0g������м������ƿ�С�
��2���ٴ�Һ©��ƿ�����رջ���K3����K2��K1������55.0mL2mol��L-1ϡ�����ر�K1��Aװ���з�Ӧ�����ӷ���ʽΪ____
�ڴ��������ܽ��K3���ر�K2����ʱ���Կ���������Ϊ_______��ԭ����_______
�۹رջ���K2��K3������100��ˮԡ����B��ˮ�֣�Һ�������Ĥʱ��ֹͣ���ȣ���ȴ�ᾧ��____������ˮ�Ҵ�ϴ�Ӿ��塣�÷�Ӧ�������������������Һ��pH��1��2֮�䣬��Ŀ��Ϊ____
��װ��C������Ϊ ____��װ��C���ڵ�ȱ����____
�ⶨĪ������Ʒ�Ĵ���
��3����ȡ����Ī������Ʒ10.0g������к���ȴ������ˮ���100mL��Һ��ȡ20.00mL��Һ����ϡ���ᣬ��0.1molL-1��KMnO4��Һ�ζ����ﵽ�ζ��յ�ʱ����10.00mlKMnO4��Һ���ζ���Ӧ�����ӷ���ʽΪ____������Ʒ�Ĵ���Ϊ____
���𰸡�������ƿ������ƿ������ƿ��������ƿ�� Fe+2H+![]() H2��+Fe2+ A�е�Һ�屻ѹ��B�� A�в���������ʹA��ѹǿ���� ���� ����Fe2+ˮ�� Һ�����ã���ֹ��������������ƿ����Fe2+ ���ܳ�ȥβ���е�H2�����ܻᵹ������ 5Fe2++MnO4-+8H+
H2��+Fe2+ A�е�Һ�屻ѹ��B�� A�в���������ʹA��ѹǿ���� ���� ����Fe2+ˮ�� Һ�����ã���ֹ��������������ƿ����Fe2+ ���ܳ�ȥβ���е�H2�����ܻᵹ������ 5Fe2++MnO4-+8H+![]() 5Fe3++Mn2++4H2O 98%
5Fe3++Mn2++4H2O 98%
��������
����ȡĪ���Σ���Һ©��ƿ�����رջ���K3 ����K2��K1������55.0mL2mol��L-1ϡ���������Ӧ������������װ���ڵĿ����ϳ������������ܽ��K3���ر�K2��A�е�Һ�屻ѹ��B�У��رջ���K2��K3������100��ˮԡ����B��ˮ�֣�������Ī���Σ���ȴ�ᾧ�����ˣ�����ˮ�Ҵ�ϴ�ӣ���Ī���ξ��壬װ��C������Һ�⣬��ֹ��������������ƿ����Fe2����
�ⶨĪ������Ʒ�Ĵ��ȣ�����5Fe2��+MnO4��+8H���T5Fe3��+Mn2��+4H2O���ӷ���ʽ���㡣
��1����װ�ýṹ��֪��װ��Ϊ������ƿ��
��2�����������ᷴӦ�����������������������ӷ���ʽΪ��Fe+2H���TH2��+Fe2����
�ڴ��������ܽ��K3���ر�K2��A������������ѹǿ����A�е�Һ��ѹ��B�У���ʱ���Կ���������Ϊ��A�е�Һ�屻ѹ��B�У�ԭ���ǣ�A�в���������ʹA��ѹǿ����
�۲���100��ˮԡ����B��ˮ�֣�Һ�������Ĥʱ��ֹͣ���ȣ���ȴ�ᾧ��Ȼ���ù��˵ķ������������Һ�з�����������������������Һ��pH��1��2֮�䣬��Ŀ��Ϊ����Fe2�� ˮ�⣻
��װ��C�ĵ��ܲ���Һ�����£�����Һ�����ã�ǰ�ɷ�ֹ��������������ƿ��Fe2��������װ��C���ڵ�ȱ���ǣ����ܳ�ȥβ���е�H2��Ҳ���ܷ�ֹ������
��3��Fe2�����л�ԭ�ԣ��������ط�Ӧ5Fe2��+MnO4��+8H���T5Fe3��+Mn2��+4H2O��n��KMnO4��=0.01L��0.1mol��L��1=0.001mol����20.00mL��Һ��n��Fe2����=0.005mol��10.0g��Ʒ��n��Fe2����=0.005mol��100mL/20mL=0.025mol����10.0g��Ʒ�У�NH4��2Fe��SO4��2��6H2O�����ʵ���Ϊ0.025mol����Ʒ�ĺ���Ϊ0.025mol��392g��mol��1/10g��100%=98%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij�Ƽ��о�С���״����һ�����͵�Li+�����ϵ������ϵ�������ú���I-��Li+��ˮ��Һ���������ù����л��ۺ���������Һ����LiNO3��Һ���ۺ������ӽ���Ĥ��Ϊ��Ĥ��Һ̬������̬�����ָ�����ԭ��ʾ��ͼ��ͼ������֪��I-+I2=I3-���������й��ж���ȷ����

A. ͼ����ԭ��ع���ԭ��ͼ��ͼ���ǵ�س��ԭ��ͼ
B. �ŵ�ʱ������Һ̬�������Һ����ɫ��dz
C. ���ʱ��Li+��������ͨ���ۺ������ӽ���Ĥ
D. �ŵ�ʱ�������ĵ缫��ӦʽΪ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.5mol��L��1��NaHCO3��Һ�е����̪����Һ��졣�Իش��й����⣺
��1������Һ��HCO3-�ĵ���̶�__________(����ڡ�����С�ڡ����ڡ�)HCO3-��ˮ��̶ȡ���Һ��Na����HCO3-��CO32-��H����OH�����ӵ�Ũ���ɴ�С��˳��Ϊ______________��
��2��ij�¶��´�ˮ�е�c(H+)= 2��10-7mol/L�����ʱ��Һ�е�c(OH-)=_________�����¶Ȳ��䣬����ϡ���ᣬʹc(H+)= 5��10-4mol/L������Һ��c(OH-)=____________����ʱ��Һ����ˮ���������c(H+)= _________ ��
��3�����ʵ���Ũ�Ⱦ�Ϊ0.1 mol/L��������Һ����KNO3����Na2CO3����NaHCO3����HCl ����CH3COOH����NaOH ����Ba(OH)2����NH4Cl�� pH �ɴ�С��˳��Ϊ________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͪ����Ҫ�Ļ���ԭ�ϣ����ɱ���������Ӧ�Ʊ���

ʵ�鲽�����£�

ʵ�鲽�����£�
����1������ͼ��ʾ��������ƿ��Ѹ�ټ���13g��״��ˮAlCl3��16mL(14g��0.18mol)��ˮ�����ڽ����½�4mL(4.3g��0.04mol)�������Ե�Һ©�������μӵ�������ƿ�С��������Ӧ�Ի��ͺ��ڷ�ˮԡ�н��������ֱ��������HCl�����ݳ�Ϊֹ��
����2������Ӧ�������ȴ�����£��ڽ����µ���18mLŨ�����30g������ձ���(��ͨ����н���)�������й��岻����ɲ�������Ũ����ʹ֮��ȫ�ܽ⡣�������ת���Һ©���У��ֳ��л��㣬ˮ���ñ���ȡ����(ÿ��8mL)���ϲ��л��㣬������15mL10%NaOH��Һ��15mLˮϴ�ӣ�������ˮMgSO4���
����3������ˮԡ�������������A��Ȼ����ʯ�����ϼ�����ȥ�����ı����������ÿ��������������ռ�195��202����֣�����Լ4.1g��
(1)����1�н������ʱ������ˮ��_____(����a������b��)�˽�ˮ������©����������_____��
(2)����2��ˮ���ñ���ȡ����(ÿ��8mL)��������ȡһ��(16mL)��Ŀ����_____����15mL10% NaOH��Һϴ�ӵ�Ŀ����_____��
(3)����3����ˮԡ��������յ�����AΪ_____��
(4)����ʵ�鱽��ͪ�IJ���Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ������ˮ�ⷴӦ������Һ�����Ե��� ( )
A. HCO3- + H2O ![]() H3O+ + CO32- B. Fe3+ + 3H2O
H3O+ + CO32- B. Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
C. HS- + H2O ![]() H2S + OH- D. NH4+ + OH-
H2S + OH- D. NH4+ + OH- ![]() NH3��+ H2O
NH3��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���黯�����������������������뵼�弤������̫���ܵ�غ��ټ��ɵ�·��
��1����̬Niԭ�ӵļ۵����Ų�ʽΪ ___����̬Asԭ�ӵ���ռ������ܼ��ĵ���������ͼΪ __ �Ρ�
��2����һ������As ___Se(����>����������) ��ԭ����____��As2O3(��˪)�����������As2O3������������AsCl3��AsCl3��LiAlH4��ԭ����AsH3��
��3����AlH4-������ԭ�ӵ��ӻ���ʽΪ___����ռ乹��Ϊ____��д��һ����AlH4-��Ϊ�ȵ�����ķ��ӵĻ�ѧʽ___��
��AsH3������H��As��H����__109.5�����>������=������)��AsH3�е����NH3����ԭ����____��
��4���л���![]() �����ƻ�˯������ȱ�ٵ�ҩ����л����д��ڵĻ�ѧ��������Ϊ____(����ĸ���)��
�����ƻ�˯������ȱ�ٵ�ҩ����л����д��ڵĻ�ѧ��������Ϊ____(����ĸ���)��
a�����Ӽ� b������ c������ d��̼̼˫��
��5���黯��������ҽѧ����������Ƥ����ճĤ����ĸ�Ⱦ������ȣ��黯��������ͼ��ʾ���þ����ܶ���Ϊ____g��cm-3(��ʽ���ɣ����ػ���)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���״��ǿ�������Դ�����п���Ӧ�õĹ���ǰ�����ش��������⣺
һ���¶��£���һ���ݵ��ܱ������У���CO��H2�ϳɼ״���CO��g��+2H2��g��CH3OH��g��
���������β���˵���÷�Ӧ�Ѵﵽƽ��״̬����________������ţ���
A��ÿ����1mol CO��ͬʱ����2molH2 B��������������ʵ�������
C��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯 D������CH3OH������������CO���������
��CO��ƽ��ת���ʣ��������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��A��B�����ƽ�ⳣ��K��A��________K��B�������������=����������

��2����֪25��ϳɰ���Ӧ�У�1mol N2��ȫת��ΪNH3ʱ�ͷŵ�����Ϊ92.4 kJ���ֽ�1mol N2��3mol H2�������2L�ܱ������У���Ӧ���е�2sĩ���NH3Ϊ0.4mol���ش��������⣺
�� �÷�Ӧ���Ȼ�ѧ����ʽ��________ ��
�� �÷�Ӧ�ﵽƽ��������¶�ƽ����________ �������Ӧ�������淴Ӧ�����ƶ����������ƽ��________������������桱�� ���������ƶ���
�� ǰ2s��v��H2����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���ij�ܱ������н������·�Ӧ��
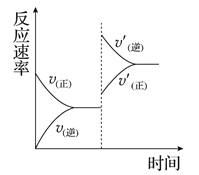
mA(g)��nB(g)![]() pC(g)��qD(g)��������ѹǿ�������¶ȣ����´ﵽƽ�⣬
pC(g)��qD(g)��������ѹǿ�������¶ȣ����´ﵽƽ�⣬
��Ӧ������ʱ��ı仯������ͼ��ʾ����Ը÷�Ӧ��������ȷ����( )
A. ����Ӧ�����ȷ�Ӧ B. �淴Ӧ�Ƿ��ȷ�Ӧ
C. m��n<p��q D. m��n>p��q
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���amolH2S��bmolO2��ϳ��ȼ�պ�����Ӧ�ﶼû��ʣ�࣬�õ����ֲ��S��SO2��H2O�����������жϴ������
A.������SO2�ǣ�b��a/2��mol
B.��Ӧ�����ɵ�ˮ����Ϊ18ag
C.��Ӧ�����������������Ϊ��16a��32b��g
D.3a��2b��a
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com