
����Ŀ��ˮ�����Ҳ�������𣮰������������ƣ�Na2O2����ĩ�ø�����֬�ް�������֬�������Ʋ���Ӧ����������ˮ�ε����й������Ƶ���֬���ϣ�����֬��Ѹ�ٷ���ȼ�գ�С���Դ�����ܸ���Ȥ����������ͬѧ�ǽ�������̽����
��������⡿����������ˮ��Ӧ������ʲô���ʣ�Ϊʲô��֬��ȼ�գ�
�����롿
�ٿ�����һ���������һ���������ɣ�
�ڷ�Ӧ�����п����������仯��
�����ʵ�顿��ͼ��ʾ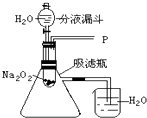
ʵ��һ��̽����Ӧ�����ɵ�������ʲô��
��1������ͼװ���еķ�Һ©���Ļ��������Ƶμ�ˮ���ٶȣ��۲쵽�Թ��������ݲ������ô����ǵ�ľ������P����ľ����ȼ��˵�����ɵ������� �� �����ķ�Ӧ����ʽΪ����������Ϊ����ԭ��Ϊ������0.2mol����������Ҫ��ת�Ƶ���mol��
��2��ʵ���У����۲쵽�����ձ��еĵ��ܿ�������ð��������Ͳ����������ԭ�� ��
��3��ʵ���������̽����Ӧ�����ɵ���һ��������ʲô��
Сǿ������һ��������Na2CO3 �� С����Ϊ�����ܣ�С���������� ��
��4��Ϊ��֤ʵС���Ŀ������������һ��֤��CO32�������ڵ�ʵ�飮
ʵ�鲽�� | ʵ������ | ʵ����� |
��5��С��ȡ��Ӧ�����õ���Һ���Թ��У�������ɫ��̪��Һ�����ַ�̪��Һ���ɫ��˵����Ӧ�����õ���һ�����������ѧʽ����
���𰸡�
��1��O2������������2Na2O2+2H2O=4NaOH+O2����Na2O2��Na2O2��0.4
��2����Ӧ�������������ų���ʹ����ƿ�ڿ�����������
��3�����������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص�����䣬����Ӧ���в���̼Ԫ��
��4��ȡ������Ӧ��������Һ���Թ��У�����ϡ���û�����ݲ�����������CO32��
��5��NaOH
���������⣺ʵ��һ��
��1.������������ȼ�ԣ���ʹ�����ǵ�ľ����ȼ��˵�����ɵ������������������ķ�Ӧ�ǹ������ƺ�ˮ��Ӧ�����������ƺ���������Ӧ�ķ���ʽΪ2Na2O2+2H2O=4NaOH+O2������Ӧ�� ��Ԫ�ػ��ϼ۩�1�۱仯Ϊ��2�ۺ�0�ۣ������������������ͻ�ԭ������ѧ����ʽ��������1mol��������ת��2mol������0.2mol����������Ҫ��ת�Ƶ���0.4mol���Դ��ǣ�O2������������2Na2O2+2H2O=4NaOH+O2����Na2O2��Na2O2��0.4��
��2.���Թ��ڷ����ķ�Ӧ�ų�������ʹ����ƿ�ڵ��¶����ߣ�����ѹǿ�������Իῴ�����ܿ�������ð�������Դ��ǣ���Ӧ�������������ų���ʹ����ƿ�ڿ����������ͣ�ʵ�����
��3.�����������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص�����䣬��Ӧ����û��̼Ԫ�أ������������Ҳ��������̼Ԫ�أ�̼���������������ᷴӦ���ɶ�����̼��������ð������û������ð������˵��û��̼������ӣ����Դ��ǣ����������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص�����䣬����Ӧ���в���̼Ԫ��.
��4.��
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ������Ӧ��������Һ���Թ��У�����ϡ���� | û�����ݲ��� | ������CO32�� |
��5.����̪��Һ���˵����Һ�Լ��ԣ�һ�������������ӣ�����һ���������������Ӻͽ������ӹ��ɵģ���Ӧ���еĽ���Ԫ��ֻ����Ԫ�أ����Ը��������������ƣ����Դ��ǣ�NaOH��


 ������ϵ�д�
������ϵ�д� �żӾ���ϵ�д�
�żӾ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���Ũ����ͬ��CH3COOH��NaOH��Һ��Ϻ���Һ��c��CH3COO����=c��Na+����������������������Һ������������=����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֱ���ŷź�SO2���γ����꣬Σ��������ij��ѧʵ��С��������װ�ý����й�SO2���ʵ�̽�����
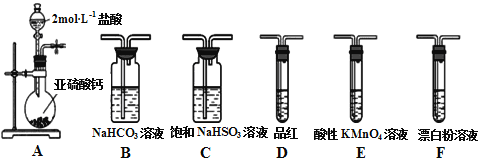
��1��װ��A�з�Ӧ�����ӷ���ʽΪ___________________________________��
��2��ѡ������װ�ú�ҩƷ̽��������������������ǿ������ͬѧ��Ϊ����A��C��F��β������˳������װ�ÿ���֤������ͬѧ��Ϊ�÷�������������������___________________����ȷ������˳���ǣ�A��C��___________��β������������ĸ��˳������װ�á�֤�������������ǿ�ڴ���������Ե�ʵ��������__________________________��
��3������������ͨ������װ�ÿ����Ʊ�Na2S2O3��

��װ��B�������Ǽ���װ��A��SO2������Ч�ʣ�B���Լ���________________��
��д��װ��A�з�����Ӧ�Ļ�ѧ����ʽ___________________________________��
��Na2S2O3��Һ�Ƕ���ʵ���еij����Լ����ⶨ��Ũ�ȵĹ������£�
��һ����ȷ��ȡa g KIO3����ѧʽ����214�����������Һ��
�ڶ������������KI�����H2SO4��Һ���μ�ָʾ����
����������Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��Һ�����ΪV mL����c(Na2S2O3)��____mol��L-1��(��֪��IO3-��5I-+6H+= 3I2��3H2O�� 2S2O32-��I2=S4O62-��2I-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ȩ�ķе�Ϊ20.8�棬����ˮ���ܣ���HgSO4����������75�����ң���Ȳ��ˮ��Ϊ��ȩ����HgSO4����ijЩ�ض����ʳ��ᷢ�������ж���ʧȥ�����ã�H2S��������һ�֣�������Ȳˮ������ֻ�ÿ�״��ʯ��Ũ���ᡢˮ��NaOH��Һ��HgO��ĩ����������ȡ��ȩ��װ����ͼ��ʾ����ش��������⣻ 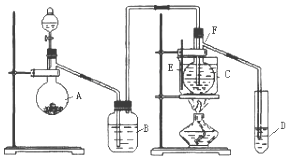
��1��ʵ�鿪ʼʱ������A��ʢ�ŵ�ʯ��B��װNaOH��Һ���������� ��
��2������D��ʢ��ˮ��������������������
��3��������ƿF��Ӧ����HgO��Ũ���ᡢˮ�����Լ����������߷ֱ�ֱ�Ӽ��룬�밴������Ⱥ�˳��д������HgO���ڵĸ��Լ������ƣ����������� ��
��4��װ��ͼ�У�����F�ķ����� �� ��ѡ���¶ȼ�F�����̱�ʾ��ȷ����������ţ��� A��0�桫50��B��0�桫100��C��0�桫200��D�� 0�桫360��
��5��������ȩ���Ƴ��IJ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ��ơ��������ơ�̼���ƺ�̼�������������г��������ʣ���ش��������⣮
��1����������̼���ƺ�̼���������������ᷴӦʱ����CO2������ǰ�����ߣ��������=����
��2��̼�����ƿ�����θ�ᣨ0.2%��0.4%�����ᣩ���࣬��Ӧ�����ӷ���ʽΪ ��
��3����ȥNaHCO3��Һ�е�����Na2CO3 �� �����ǣ� �� ���ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����㻯����M�Ľṹ��ʽΪ 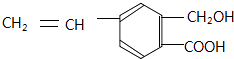 �������л���M��˵����ȷ���ǣ� ��
�������л���M��˵����ȷ���ǣ� ��
A.�л���M�к������ֹ�����
B.1 molNa2CO3���������1 mol���M
C.1 mol M�����������Ʒ�Ӧ����22.4 L����
D.�л���M�ܷ���ȡ���������ͼӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ�������ֵ�������й�˵����ȷ���ǣ� ��
A.78g�������ƾ����У���2NA��������
B.���³�ѹ�£�22.4L��������NA����ԭ��
C.��O2����ķ�Ӧ�У�1 mol O2��������ʱ�õ��ĵ�����һ����4NA
D.������16g O2��O3�Ļ�������к���ԭ����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨ�Ѳ��ֱ��ʵĹ���������Ʒ�Ĵ��ȣ������ͼ��ʾ��ʵ��װ�ã�ͼ��QΪ�������õ�������ҩƷ��Ӧ������ȡһ��������Ʒ�������У�����ͼ��ʾ��װ�ð�װ����������Һ©���Ļ�������ϡ������������У� 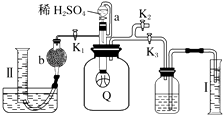
��ش��������⣺
��1��Q�ڷ�����Ӧ���������壬���еķ�Ӧ����Ϊ������ԭ��Ӧ��
��2��Ϊ�ⶨ��Ӧʱ������������������ϡH2SO4ǰ����ر����K1������K2����K3�����������K1������K2����K3������
��3����������Ӧֹͣʱ����K1��K2��K3���رգ�Ȼ���ȴ�K2 �� �ٻ�����K1 �� ��ʱ�ɹ۲쵽�������� ��
��4��b��װ�Ĺ����Լ��� �� �軺����K1��ԭ��Ϊ ��
��5��ʵ�����ʱ����Ͳ������x mLˮ����Ͳ�����ռ���y mL���壬��������ƵĴ��������ú�x��y��ʽ�ӱ�ʾ�����������������ɱ�״������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A������ʯ�͵���Ҫ�л�����ԭ�ϣ��������������һ������ʯ�ͻ�����չˮƽ��E�Ǿ��й���ζ���л��F��һ�ָ߾�����Ƴɶ��ְ�װ���ϡ�
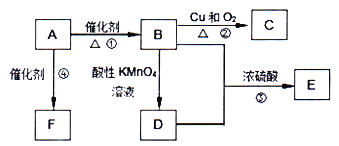
(1)A��D�����еĹ����ŷֱ�����Ϊ_______��_______��
(2)��Ӧ�ٵķ�Ӧ����Ϊ________��
(3)��Ӧ�ڵĻ�ѧ����ʽΪ_________��
(4)��Ӧ�۵Ļ�ѧ����ʽΪ_______���÷�Ӧ�ķ�Ӧ����Ϊ_____��
(5)��Ӧ�ܵĻ�ѧ����ʽΪ_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com