
【题目】某微生物电解池(MEC)制氢工作原理如右图所示。用该电解池电解0.1mol·L-1的CH3COOH溶液,下列说法正确的是
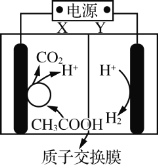
A.Y为电源的正极
B.该电解装置中,阳极的电极反应式为:CH3COOH+2H2O+8e-= 2CO2↑+8H+
C.当2mol H+通过质子交换膜时,则标准状况下产生22.4L H2
D.电解一段时间后,溶液中![]() 的值变小
的值变小
【答案】C
【解析】
用该电解池电解0.1mol·L-1的CH3COOH溶液,氢离子在阴极得到电子发生还原反应生成氢气,电极反应2H++2e-=H2↑,电源Y为负极,正极电极反应是醋酸失电子发生氧化反应生成二氧化碳,电极反应CH3COOH+2H2O-8e-═2CO2↑+8H+,电源X为负极,质子交换膜允许阳离子通过;
A、分析可知Y为电源负极,故A错误;
B、电解池电解0.1mol·L-1的CH3COOH溶液,氢离子在阴极得到电子发生还原反应生成氢气,电极反应2H++2e-=H2↑,正极电极反应是醋酸失电子发生氧化反应生成二氧化碳,电极反应CH3COOH+2H2O-8e-═2CO2↑+8H+,故B错误;
C、当2 molH+通过质子交换膜时,电子转移2mol,则标准状况下产生22.4L H2,故C正确;
D、c(CH3COO-)/c(CH3COOH)=c(CH3COO-)/c(CH3COOH)×c(H+)/c(H+)=Ka/c(H+),电极反应分析阴极电极反应2H++2e-=H2↑,阳极电极反应CH3COOH+2H2O-8e-═2CO2↑+8H+,电子守恒可知氢离子浓度基本不变,比值基本不变,故D错误;
故选:C。


科目:高中化学 来源: 题型:
【题目】A~G是短周期主族元素,原子序数依次增大。它们的部分信息如下表所示:
A | B | C | D | E | F | G | |
原子半径/nm | 0.077 | 0.074 | 0.186 | 0.143 | 0.099 | ||
主要化合价 | -4,+4 | -2 | +3 | -4,+4 | -1,+7 | ||
其它 | 阳离子核外无电子 | 它的化合物数量众多分布极广 | 焰色反应呈黄色 | 无机非金属材料的主角 |
(1)F在元素周期表中的位置是____________;
(2)任写一个BA4的同系物的分子式___________;
(3)请用电子式表示DG的形成过程____________;
(4)元素D与C按原子个数比1∶1形成的化合物所含的化学键有______(填化学键类型);
(5)D与E相比,金属性较强的是_____(用元素符号表示),元素D、E最高价的氧化物对应的水化物反应的离子方程式为___________
(6)工业上冶炼单质E的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
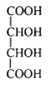
【题目】[物质结构与性质](1)酒石酸钛配合物广泛应用于药物合成。酒石酸(结构如图所示)中羧基氧原子的轨道杂化类型分别是______________
(2)氰酸(HOCN)的结构式是_________,根据等电子体原理,可推测氰酸根离子的空间构型是____。
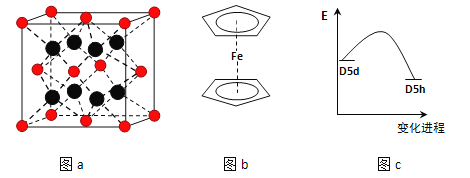
(3)FeBr2为只含有离子键的离子化合物,其晶胞结构如图a,距一个Fe2+离子最近的所有Br-离子为顶点构成的几何体为_____________.
(4)二茂铁是最重要的金属茂基配合物,也是最早被发现的夹心配合物,包含两个环戊二烯基与铁原子成键.二茂铁的结构为一个铁原子处在两个平行的环戊二烯基环的之间,结构如图b所示,已知二茂铁的一氯代物只有一种.
①二茂铁的分子式为__________.
②穆斯堡尔谱学数据显示,二茂铁中心铁原子的氧化态为+2,每个茂环带有一个单位负电荷.因此每个环含有________个π电子.
③二茂铁中两个茂环可以是重叠的(D5h),也可以是错位的(D5d),它们之间的能垒仅有8~20kJ/mol.温度升高时则绕垂直轴相对转动,使得两种结构可以相互转换,转换过程中能量变化如图c.比较稳定的是__________结构(填“重叠”或“错位”).
(5)氧化镍(NiO)是一种纳米材料,比表面积S(m2/g)是评价纳米材料的重要参数之一(纳米粒子按球形计)。基态Ni2+有_________个未成对电子,已知氧化镍的密度为ρg/cm3;其纳米粒子的直径为Dnm列式表示其比表面积 ____________m2/g。
查看答案和解析>>
科目:高中化学 来源: 题型:
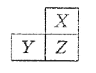
【题目】X、Y、Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
A.原子半径: Y >Z >X
B.元素气态氢化物的热稳定性:X < Z
C.Y和Z的最高价氧化物对应水化物均为强酸
D.X的最高正价为+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌电池是一种极具前景的电化学储能装置。![]() 扣式可充电电池组成示意图如下。
扣式可充电电池组成示意图如下。![]() 可以在
可以在![]() 晶体中可逆地嵌入和脱除,总反应为
晶体中可逆地嵌入和脱除,总反应为![]() 。下列说法错误的是( )
。下列说法错误的是( )
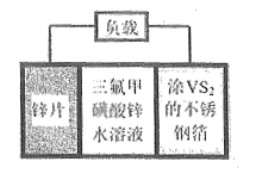
A. 放电时不锈钢箔为正极,发生还原反应
B. 放电时负极的反应为![]()
C. 充电时电池正极上的反应为:![]()
D. 充电时锌片与电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中是同系物的有_______;互为同分异构体的有_______________;互为同素异形体的有________________;互为同位素的有_______________;
互为同一物质的有______________;
(1)液氯 (2)氯气 (3)白磷 (4)红磷 (5)D (6)T (7) ![]() (8)
(8)![]() (9)CH2 = CH-CH3 (10)
(9)CH2 = CH-CH3 (10) ![]() (11)2,2—二甲基丁烷
(11)2,2—二甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 对2HI(g)![]() H2(g)+I2(g)平衡体系增大压强使气体颜色变深
H2(g)+I2(g)平衡体系增大压强使气体颜色变深
B. 向橙色 K2Cr2O7溶液中加入一定浓度的NaOH溶液后,溶液变为黄色
C. 红棕色的NO2,加压后颜色先变深后变浅
D. 溴水中有下列平衡Br2+H2O![]() HBr +HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr +HBrO,当加入AgNO3溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 常温常压下,56g丙烯与环丁烷的混合气体中含有4NA个碳原子
B. 25℃,pH=1的H2SO4溶液中,H+的数目为0.2NA
C. 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
D. 1mol的P4O6中含有6 NA个P-O键(P4O6的结构如图: ![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2A(g)![]() B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够长时间后反应再次达到平衡状态,此时c(A)/c(B=b,下列叙述正确的是( )
B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够长时间后反应再次达到平衡状态,此时c(A)/c(B=b,下列叙述正确的是( )
A. 在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B. 若a=b,则容器中可能使用了催化剂
C. 若其他条件不变,升高温度,则a<b
D. 若保持温度、压强不变,充入惰性气体,则a>b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com