
【题目】I.下列两种溶液中,室温下由水电离生成的H+浓度之比(①∶②)是 。
①pH=1的盐酸 ②0.01 mol·L-1的NaOH溶液
II.已知水在25℃和95℃时,其电离平衡曲线如图所示:
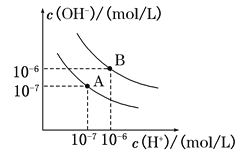
(1)则25℃时水的电离平衡曲线应为 (填“A”或“B”);95℃时水的离子积KW= 。
(2)25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为 。
(3)曲线A对应温度下,pH=2的盐酸溶液和pH=11的氢氧化钠溶液按体积比1:9混合,溶液的pH约为 。
【答案】I. 1:10 ;II.(1)A ;1×10-12(2)10:1(3)4
【解析】
试题分析:I.①酸溶液中水电离产生的氢离子浓度等于溶液中氢氧根浓度,室温下,pH=1的盐酸中氢氧根浓度为1×10-13mol/L,②碱溶液中的氢离子全部来自水的电离,室温下,0.01 mol·L-1的NaOH溶液中氢离子浓度为1×10-12mol/L,由水电离生成的H+浓度之比(①∶②)是1:10。
II.(1)曲线A条件下Kw=c(H+)c(OH-)=10-7×10-7=10-14,曲线B条件下Kw=c(H+)c(OH-)=10-6×10-6=10-12;水的电离时吸热过程,加热促进电离,所以A曲线代表25℃时水的电离平衡曲线;(2)B为95℃水的电离平衡曲线,Kw=c(H+)c(OH-)=10-6×10-6=10-12。
(2)25℃时,所得混合溶液的pH=7,溶液呈中性,酸碱恰好中和,n(OH-)=n(H+),则V[Ba(OH)2]×10-5 mol/L=V(H2SO4)×10-4 mol/L,则Ba(OH)2溶液与H2SO4溶液的体积比为10:1。
(3)pH=2盐酸c(H+)=0.01mol/L,pH=11的氢氧化钠溶液c(OH-)=0.001mol/L,则混合液中c(H+)=(0.01×1-0.001×9)/(1+9)=0.0001mol/L,pH=4。


科目:高中化学 来源: 题型:
【题目】辣椒中含辣椒素,局部应用可助减轻疼痛。辣椒素酯类化合物的结构可以表示为: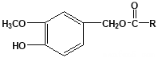 (R为烃基),其中一种辣椒素酯类化合物J的合成路线如下:
(R为烃基),其中一种辣椒素酯类化合物J的合成路线如下:
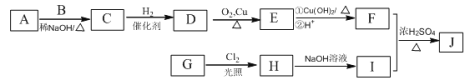
已知:
①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰,峰面积比分别为9:1和3:1;
②化合物J的分子式为C15H22O4;
③
回答下列问题:
(1)G中含有的官能团有 、 。
(2)由C生成D的反应类型为 ,D的化学名称为 。
(3)①的化学方程式为 。
(4)J的结构简式为 。
(5)G的同分异构体中,苯环上的一氯代物只有一种的共有 种(不含立体异构),核磁共振氢谱显示2组峰的是 (写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究碳酸钙与稀盐酸反应过程中的速率变化,在VmL稀盐酸中加入足量的碳酸钙,收集反应放出的CO2(气体体积已换算为标准状况下的数值),实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
CO2体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)0~1 min、1~2 min、2~3 min、3~4 min、4~5 min五个时间段中,_________反应速率最快。
(2)假设溶液体积不变,4~5min时间段以盐酸的浓度变化来表示的该反应速率为____________________________。
(3)为了降低上述化学反应的反应速率,向溶液中加入下列物质,你认为可行的是
_______________(填编号)。
a.蒸馏水 b.浓盐酸 c.NaCl固体 d.NaCl溶液
(4)除了上述方法外,你认为还可以采取哪些措施来降低化学反应速率?(试写两条)_______________________________________________________________________,
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列事实不能用勒夏特列原理解释的是 ( )
A.合成氨工业上增大压强以提高反应物的转化率
B.黄绿色的氯水光照后颜色变浅
C.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
D.在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(平行班做)下表是有机物A、B的有关信息。
A | B |
①能使溴的四氯化碳溶液退色 ②比例模型为: ③能与水在一定条件下反应生成醇 | ①由C、H两种元素组成 ②球棍模型为: |
根据表中信息回答下列问题:
(1)写出A的电子式_____________________。
(2)写出在一定条件下,A生成高分子化合物的化学反应方程式________________________________。
(3)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=_____ 时,这类有机物开始出现同分异构体。
(4)B具有的性质有_____________________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应使之退色 ⑥任何条件下不与氢气反应
(5)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的Cu2O和CuO混合粉末,将其均匀混合后分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入400mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为( )
A. 4.0mol/L B. 3.2mol/L
C. 2.0mol/L D. 1.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,相同体积的四个刚性容器中分别存在以下四个平衡:
①N2(g)+3H2(g)![]() 2NH3(g) K1
2NH3(g) K1
②H2(g)+I2(g)![]() 2HI(g) K2
2HI(g) K2
③2NO2(g)![]() N2O4(g) K3
N2O4(g) K3
④C(s)+H2O(g)![]() CO(g)+H2(g) K4
CO(g)+H2(g) K4
请完成下列各题:
(1)写出反应④的平衡常数的表达式K4=____________;
(2)现有相同温度下的以下平衡:
⑤ 2N2(g)+6H2(g)![]() 4NH3(g) K5
4NH3(g) K5
⑥2HI(g)![]() H2(g)+I2(g) K6
H2(g)+I2(g) K6
则K5=__ ;K6=_ ;(用K1、K2、K3、K4表示)
(3)若平衡③中NO2的体积分数为a,某时刻再加入一定量的N2O4,此时υ(正) υ(逆);再次达到平衡后,NO2的体积分数 a。(填“﹥”、“﹤”或“﹦”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近些年,半导体材料在电子领域发展迅速,科学家一般在分界线出寻找半导体材料,如硅、锗、砷及GaAs等化合物。回答下列问题:
(1)基态As原子的外围电子排布式为________,原子核外有______个未成对电子。
(2)实验测得镓的氯化物的熔沸点显著低于其对应化合价的氯化物,其原因可能是_________。
(3)Ge、Se、As位于周期表第四周期,其第一电离能由大到小的顺序为______。
(4)AsH3分子的立体构型为 ______,其中As的杂化轨道类型为______。
(5)碳和硅属于同主族元素,碳能形成多种氢化物,但硅的氢化物很少且不稳定,试从原子结构角度分析可能的原因__________。
(6)GaAs晶胞结构如图所示,若A的坐标参数为(0,0,0),B为(0,1/2,1/2)、C为(1,0,0)、则D的坐标参数为_______。已知GaAs的晶胞边长为apm,其密度为_____ g·cm-3(列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物Targretin(F)能治疗顽固性皮肤T-细胞淋巴瘤,其合成路饯如下图所示:
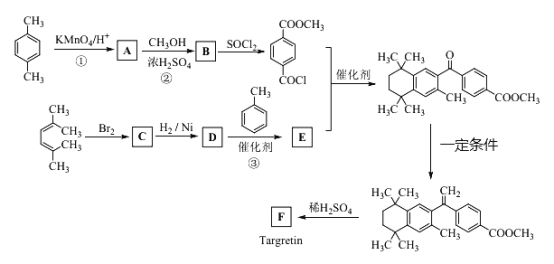
已知:①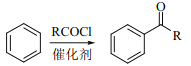
②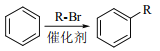
③![]() (R表示烃基或芳基)
(R表示烃基或芳基)
(1)反应①的反应类型是______________________
(2)反应②的化学方程式_________________________________________。
(3)C的结构简式是_____________________________________________。
(4)反应③的化学方程式____________________________________________。
(5)F的分子式C24H28O2,F中含有的官能团____________________________。
(6)写出满足下列条件A的两种同分异构体的结构简式(不考虑-O-O-或![]() 结构)________________________________。
结构)________________________________。
a.苯环上的一氯代物有两种 b.既发生银镜反应又能发生水解反应
(7)已知: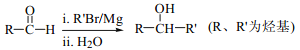 ,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成
,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成![]() ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。_________________________
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com