
【题目】如图是某无机化合物的二聚分子(小球大小只代表种类不同,与原子半径大小无关),该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层电子数都达到8个电子的稳定结构。下列说法不正确的是 ( )

A. 该化合物的化学式是Al2Cl6
B. 该化合物是离子化合物,在熔融状态下能导电
C. 该化合物在固态时所形成的晶体是分子晶体
D. 该化合物中不存在离子键,也不含有非极性共价键
【答案】B
【解析】
将二聚分子变成单分子,得AB3化学式,根据两种元素都处于第三周期,可能是PCl3 或AlCl3,而在PCl3所有原子已达稳定结构,形成二聚分子的话不可能符合,故只可能是AlCl3,为共价化合物,据此分析解答。
A.将二聚分子变成单分子,得AB3化学式,根据两种元素都处于第三周期,可能是PCl3 或AlCl3,而在PCl3所有原子已达稳定结构,形成二聚分子的话不可能符合,故只可能是AlCl3,该化合物的化学式是Al2Cl6,故A正确;
B.Al2Cl6属于共价化合物,不存在离子键,在熔融状态下不能导电,故B错误;
C.Al2Cl6属于共价化合物,固态是构成分子晶体,熔沸点较低,故C正确;
D.Al2Cl6属于共价化合物,不存在离子键,只有极性共价键,不含有非极性共价键,故D正确;
故选B


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X溶液中含有下表所示离子中的某5种,且其离子浓度均为![]() (不考虑水的电离和离子水解)。向X溶液中加入足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列叙述错误的是( )
(不考虑水的电离和离子水解)。向X溶液中加入足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列叙述错误的是( )
阳离子 |
|
阴离子 |
|
A.原溶液中一定含有![]()
B.X溶液中不可能含有![]() 和
和![]()
C.X溶液中含有3种阳离子、2种阴离子
D.生成气体的离子反应方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业综合处理含![]() 废水和含
废水和含![]() 的废气,得无毒气体b,流程如下:
的废气,得无毒气体b,流程如下:
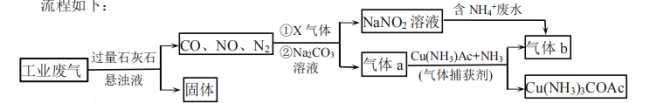
下列说法错误的是( )
A.“固体”中主要含有![]() 、
、![]()
B.X气体、![]() 与
与![]() 溶液的离子反应:
溶液的离子反应:![]()
C.处理含![]() 废水时,离子反应:
废水时,离子反应:![]()
D.捕获剂捕获气体a中![]() 发生了氧化还原反应
发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制银氨溶液操作如图所示,下列说法错误的是( )
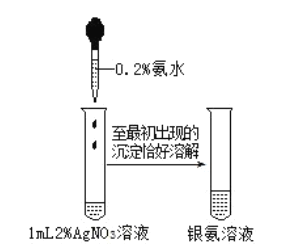
已知:![]() ,
,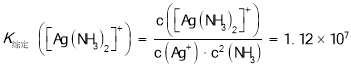
A.制得的银氨溶液可用于还原性糖的检验
B.![]() 中含有
中含有![]() 个
个![]() 键
键
C.银氨溶液不能长期存放,需要现用现配
D.![]() 固体可溶于氨水得到银氨溶液
固体可溶于氨水得到银氨溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等质量的O2和O3所含分子的物质的量之比为____________。
(2)等温等压下,等体积的O2和O3所含分子个数比为________________,
(3)在反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂是________,氧化产物是________,氧化产物与还原产物的物质的量之比为________,被氧化与未被氧化的HCl的质量之比为________,若有73 g HCl被氧化,电子转移的总数为________。
(4)配制100 mL 1 mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分数为98%)的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度为1.5 mol·L-1
B. 把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%
C. 把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol·L-1
D. 把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。如图表示N2O在Pt2O+表面与CO反应转化成无害气体的过程。下列说法正确的是

A.N2O转化成无害气体时的催化剂是Pt2O2+
B.每1mol Pt2O+转化为Pt2O2+得电子数为3NA
C.将生成的CO2通人含大量SiO32-、Na+、Cl-的溶液中,无明显现象
D.1g CO2 、N2O的混合气体中含有电子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com