
【题目】下列有关化学反应的叙述正确的是( )
A.氯化铝溶液和过量氨水生成氢氧化铝
B.镁在二氧化碳中燃烧生成碳酸镁
C.向苯酚溶液中滴入Na2CO3溶液,产生气泡
D.铁与高温水蒸气反应生成氧化铁
科目:高中化学 来源: 题型:
【题目】实验小组探究KI与Cu(NO3)2的反应,进行实验一:
实验一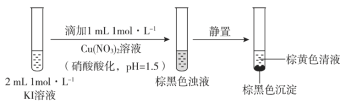
注:本实验忽略Cu2+在此条件下的水解。
(1)取棕黄色清液,加入少量______溶液(试剂a),清液变为______色,说明生成了I2。
(2)探究生成I2的原因。
①甲同学进行如下实验:向2mL1mol·L-1KI溶液中加入1mL______溶液(硝酸酸化,pH=1.5),再加入少量试剂a,观察到与(1)相同的现象。甲同学由此得出结论:实验一中生成I2的原因是酸性条件下,![]() 氧化了I-。
氧化了I-。
②乙同学认为仅由甲的实验还不能得出相应结论。他的理由是该实验没有排除____________氧化I-的可能性。
③若要确证实验一中是![]() 氧化了I-,应在实验一的基础上进行检验______的实验。
氧化了I-,应在实验一的基础上进行检验______的实验。
(3)探究棕黑色沉淀的组成。
①查阅资料得知:CuI为难溶于水的白色固体。于是对棕黑色沉淀的组成提出两种假设:
a.CuI吸附I2b._________吸附I2。为证明上述假设是否成立,取棕黑色沉淀进行实验二:
实验二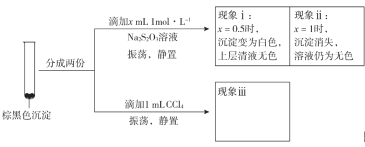
已知:CuI难溶于CCl4;I2+![]() ==2I-+
==2I-+![]() (无色);Cu++S2O32-==
(无色);Cu++S2O32-==![]() (无色)。由实验二得出结论:棕黑色沉淀是CuI吸附I2形成的。
(无色)。由实验二得出结论:棕黑色沉淀是CuI吸附I2形成的。
②现象iii为______________。
③用化学平衡移动原理解释产生现象ii的原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2 = 2AB的能量变化如图所示,则下列说法正确的是
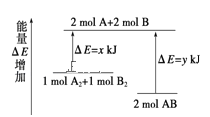
A.该反应是吸热反应
B.断裂 1molA-A 键和 1molB-B 键能放出xkJ 的能量
C.2mol AB 的总能量高于1mol A2和1mol B2和的总能量
D.断裂 2mol A-B 键需要吸收ykJ 的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂、钴、镍及其化合物在工业和医药等领域有重要应用。回答下列问题:
(1)筑波材料科学国家实验室科研小组发现了在5K下呈现超导性的晶体CoO2,该晶体具有层状结构。
①晶体中原子Co与O的配位数之比为_________。
②基态钴原子的价电子排布图为_______。
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于_____晶体;写出两种与CO具有相同空间构型和键合形式的分子或离子:_______。
(3)某镍配合物结构如图所示:
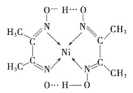
①分子内含有的化学键有___________(填序号).
A 氢键 B 离子键 C 共价键 D 金属键 E 配位键
②配合物中C、N、O三种元素原子的第一电离能由大到小的顺序是N> O>C,试从原子结构解释为什么同周期元素原子的第一电离能N>O_________。
(4)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属" ,其结构如图所示。

①"分子金属"可以导电,是因为______能沿着其中的金属原子链流动。
②"分子金属"中,铂原子是否以sp3的方式杂化?_________(填“是"或“否"),其理由是__________。
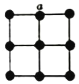
(5)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示,若金属铂的密度为d g·cm-3,则晶胞参数a=_______nm(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期主族元素,X、Y在周期表中的相对位置如图所示,Xn、Yn+、Z+具有相同的电子层结构,W的最内层电子数与最外层电子数之和等于次外层电子数。下列说法正确的是

A. 原子半径:r(X)<r(Y)<r(Z)<r(W)
B. X形成的氧化物的种类最多为4种
C. 最高价氧化物对应水化物的碱性:Z<Y
D. Y、Z、W对应的最高价氧化物的水化物之间能够两两相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物苯:常常作为工农业生产中的良好溶剂。
(1)若将苯倒入盛有碘水的试管中,振荡后静置,现象是__________________________,说明苯的密度比水_________,且________________。
(2)若将乒乓球碎片、食盐固体分别加入盛有苯的试管中,振荡后静置,现象是___________________,说明苯是很好的_____________________________。
(3)将盛有苯的两支试管分别插入100℃的沸水和0℃的冰水的现象是________________________,说明苯的沸点_________________,熔点_________。
人们对苯的认识有一个不断深化的过程。
(4)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出分子式为C6H6的一种含两个三键且无支链的链烃的结构简式_____________________________________。
(5)已知分子式为C6H6的有机物有多种,其中的两种为:
(I)![]() (II)
(II)![]() 这两种结构的区别表现在以下两方面:
这两种结构的区别表现在以下两方面:
①定性方面(即化学性质方面):(II)能___________(填字母),而(I)不能。
a. 被高锰酸钾酸性溶液氧化 b. 与溴水发生取代反应
c. 与溴发生取代反应 d. 与氢气发生加成反应
②定量方面(即消耗反应物的量的方面):1molC6H6与H2加成时:(I)需要H2______mol,而(II)需要H2_____mol。
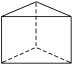
(6)今发现C6H6还可能有另一种如右图所示的立体结构,该结构的一氯代物有_________种;现代化学认为苯分子中碳碳之间的键是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粮食仓储常用磷化铝(A1P)熏蒸杀虫,A1P遇水即产生强还原性的PH3气体。国家标准规定粮食中磷物(以PH3计)的残留量不超过0.05 mgkg-1时为合格。某小组同学用如图所示实验装置和原理测定某粮食样品中碟化物的残留量。C中加入100 g原粮,E 中加入20.00mL2.50×lO-4molL-1KMnO4溶液的H2SO4酸化),C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中的溶液。
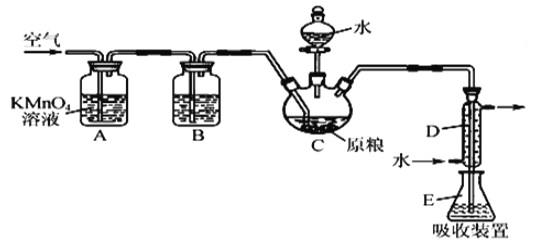
(1)装置A中的KMn04溶液的作用是_____。
(2)装置B中盛装焦性没食子酸的碱性溶液吸收空气中的O2。若去掉该装置,则测得的磷化物的残留量___(填“偏髙”“偏低”或“不变”)。
(3)装置E中PH3氧化成磷酸,MnO4-被还原为Mn2+,写出该反应的离子方程式:__________。
(4)收集装置E中的吸收液,加水稀释至250 mL,量取其中的25.00 mL于锥形瓶中, 用4.0×lO-5molL-1的Na2SO3标准溶液滴定,消耗Na2SO3标准溶液20.00mL,反应原理是 S02-+Mn04-+H+→S042-+Mn2++H20(未配平)通过计算判断该样品是否合格(写出计算过程)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)26H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为___。
(2)NO3-中氮原子轨道的杂化类型是___。
(3)与HNO2互为等电子体的一种阴离子的化学式为___。
(4)配合物[Mn(CH3OH)6]2+中配位原子是___。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有___。
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___。
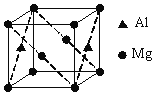
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酞含片是一种治疗消化系统疾病的药物,其有效成分的结构简式如图所示.下列对该有效成分的说法正确的是( )
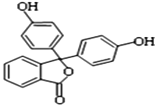
A. 核磁共振氢谱中有5个峰
B. 最多有15个碳原子共平面
C. 可能发生缩聚反应生成高分子化合物
D. 1mol该物质最多能与含4molNaOH的烧碱溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com