
����Ŀ�����ݱ�����һ��Ӳ�ijɷ�ΪCa5(PO4)3OH�����ʱ�����������Һ�д�������ƽ�⣺Ca5(PO4)3OH![]() 5Ca2+ +3PO43-+OH-����֪Ca5(PO4)3F(s)���ܽ�ȱ�Ca5(PO4)3OH(s)��С��Ϊ�˱������ݣ�������ؾ������˲�ͬ�Ĵ�ʩ�����´�ʩ�в��ܱ������ݵ���( )
5Ca2+ +3PO43-+OH-����֪Ca5(PO4)3F(s)���ܽ�ȱ�Ca5(PO4)3OH(s)��С��Ϊ�˱������ݣ�������ؾ������˲�ͬ�Ĵ�ʩ�����´�ʩ�в��ܱ������ݵ���( )
A. �ٳ���ʳ B. ���̼������
C. �������м�����������Ӽ� D. ������������������Ca2+��PO43-����
���𰸡�B
��������A���ٳ���ʳ������Ͳ������٣����������ݵ����ã�A��ѡ��B������������������OH����ƽ�������ƶ����ٽ����ݵĸ�ʴ�������������ݵ����ã�Bѡ��C���������м�����������Ӽ���������Ӧ5Ca2++3PO43��+F��=Ca5(PO4)3F���������ܽ�ȸ�С��Ca5(PO4)3F�����������ݵ����ã�C��ѡ��D��������������������Ca2+��PO43�����ӣ�ʹƽ��Ca5(PO4)3OH5Ca2++3PO43��+OH���������ƶ����ɱ������ݵ����ʣ�D��ѡ����ѡB��


 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��POC13�������뵼����Ӽ������άԭ�ϣ�ʵ�����Ʊ�POC13���ⶨ��Ʒ������ʵ��������£�
I.ʵ�����Ʊ�POC13��
������������Һ̬PCl3����ȡPOC13��ʵ��װ�ã����ȼ��г������ԣ���ͼ:

���ϣ���Ag+SCN-==AgSCN��:Ksp(AgCl)>Ksp(AgSCN)��
��PCl3��POC13�������Ϣ���±���
���� | �۵�/�� | �е�/�� | ��Է������� | ���� |
PCl3 | -112.0 | 76.0 | 137.5 | �����ܣ���Ϊ��ɫҺ�壬��ˮ�����ҷ�Ӧ���ɺ�������Ȼ��� |
POC13 | 2.0 | 106.0 | 153.5 |
(1)B����ʢ���Լ���________������ܵ�������_____________________��
(2)POC13��ˮ��Ӧ�Ļ�ѧ����ʽΪ____________________________��
(3)װ��B�����ó�����O2�⣬����_____________________________��
(4)��Ӧ�¶�Ҫ������60~65�棬ԭ���ǣ�____________________________��
II.�ⶨPOC13��Ʒ�ĺ�����
ʵ�鲽�裺
���Ʊ�POC13ʵ�����������ƿ�е�Һ����ȴ�����£�ȷ��ȡ30.7g POC13��Ʒ������ʢ��60.00 mL����ˮ��ˮ��ƿ��ҡ������ȫˮ�⣬��ˮ��Һ���100. 00 mL��Һ��
��ȡ10. 00 mL��Һ����ƿ�У�����10.00 mL 3.2mol/L AgNO3����Һ��
�ۼ�����������������ҡ����ʹ�������汻�л��︲�ǡ�
����XΪָʾ������0.2 mol/L KSCN��Һ�ζ�������AgNO3��Һ���ﵽ�ζ��յ�ʱ����ȥl0.00 mLKSCN��Һ��
(5)����������������������__________________________��
(6)�������XΪ____________________ ��
(7)��Ӧ��POC13�İٷֺ���Ϊ_________��ͨ��__________(�����)������߲�Ʒ�Ĵ��ȡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ�����
��1�������ǻ�����ϩ�ĵ���ʽ���ǻ� __________����ϩ __________��
��2����ϵͳ�������������л�������
![]() ___________________________��
___________________________��
��![]() ___________________________________��
___________________________________��
��3����Է�������Ϊ114����һ�ȴ���ֻ��һ�ֵ������Ľṹ��ʽ ___________�����ʵ�����Ϊ________________��
��4��ij��1���Ӻ���50�����ӣ�����ֻ����һ�ֽṹ��Ȳ������õ���������ļ���ʽΪ _____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƽ������о������ֵ����дʻ㣬������������ʵ���ɫ������ϵ����
A����ɫ���� B����ɫ���� C����ɫ��Ⱦ D����ɫʳƷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Է�Ǧ��(��Ҫ�ɷ���PbS,������ZnS��Fe��Ag)Ϊԭ������Ǧ���仯����Ĺ�����������:
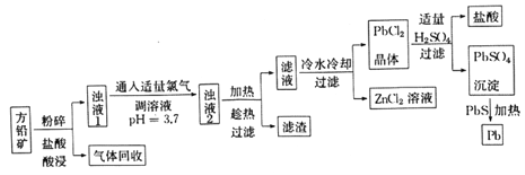
��ش���������:
��1�������������ȹ�������Ŀ����______����������Ҫ�ɷ���_________��
��2���ù��������п�ѭ�����õ�������____________��
��3����Һ1��ͨ����������ʱ,������Ӧ�����ӷ���ʽΪ____________��
��4����ҩ���ۡ����й�Ǧ��(Pb3O4)��������:���ξ��¿���,Ż��,���ʡ�����Ǧ���еμ�Ũ����ʱ,��������ɫ����,��д��������Ӧ�Ļ�ѧ����ʽ_________��
��5��ȡһ��������Pb2+��Cu2+�Ĺ�ҵ��ˮ,�����еμ�Na2S��Һ,��PbS��ʼ����ʱ����Һ��c(Pb2+)/c(Cu2+)=_______��[��֪Kp(PbS)=3.4��10-28,Kp(CuS)=1.3��10-36]
��6����Ǧ����Ǧ����ʹˮ�����ؽ���Ǧ�ĺ�����������������Ⱦ��ˮ��Һ��Ǧ�Ĵ�����̬��Ҫ��Pb2+��Pb(OH)+��Pb(OH)2��Pb(OH)3-��Pb(OH)42-������̬��Ũ�ȷ���x����ҺPH�仯�Ĺ�ϵ����ͼ��ʾ:
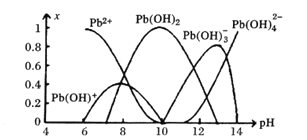
��̽��Pb2+������:��Pb2+����Һ����εμ�NaOH��Һ,��Һ�����,�����μ�NaOH��Һ�ֱ����;pH>13ʱ,��Һ�з�������Ҫ��Ӧ�����ӷ���ʽΪ________��
�ڳ�ȥ��Һ�е�Pb2+:����С����һ�������Լ���ȥ��ˮ�е�Ǧ��������������,ʵ������¼����:
���� | Pb2+ | Ca2+ | Fe3+ | Mn2+ |
����ǰŨ��(mg/L) | 0.100 | 29.8 | 0.12 | 0.087 |
������Ũ��(mg/L) | 0.004 | 22.6 | 0.04 | 0.053 |
�ɱ���֪���Լ�ȥ��Pb2+��Fe3+Ч����,���ñ����й�����˵��_________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ȷ����
A. ��CO2ͨ��BaCl2��Һ�������ͣ�������������ͨ��SO2,��������
B. �����£���Ӧ4Fe(OH)2(s)+2H2O(l)+O2(g)=4FeOH)3(s)���Է����У�����H<0
C. NH4Al(SO4)2��Һ�м�����������������Һ:NH4++OH-=NH3��H2O
D. ��ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���Cu(NO3)2���壬ͭ���Բ��ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10mL bmol��L��1��CH3COOH��Һ���μӵ������0.01mol��L��1��NaOH��Һ����ַ�Ӧ����Һ��c(CH3COO��)=c(Na+)������˵����ȷ����(��)
A. b��0.01
B. ��Ϻ���Һ��������ж�
C. CH3COOH�ĵ��볣��Ka��![]()
D. ��CH3COOH��Һ�еμ�NaOH��Һ�Ĺ����У�ˮ�ĵ���̶���С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҽ�����黼��״���״�IJ��˶�ʳ�������������ں����к��Ϸḻ�� �� ��
A. ��Ԫ�� B. ��Ԫ�� C. ��Ԫ�� D. пԪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������·�Ӧ�У�����˿��������ȼ�� �ڼ���̼������ͭ�Ļ�����̼���ƺ����ᷴӦ �ܼ��ȸ�����ع��� ��п��ϡ���ᷴӦ ����������Һ���Ȼ�����Һ��ϡ��������ӷ�Ӧ����___________�������Ӧ����ţ���ͬ��������������ԭ��Ӧ��___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com