
【题目】下列浓度关系正确的是
A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]
B.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-)
D.Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-) >c(H+)
【答案】D
【解析】
试题分析:A.氯水中只有一般分氯气溶解,故c(Cl2)=2[c(ClO-)+c(Cl-)+C(HClO)]等式左边若换成溶解的氯气才正确,故A错误;B.根据Cl2+H2O![]() HClO+H++Cl-,HCl完全电离,而HClO部分电离,可知正确的顺序c(H+)>c(Cl-)>c(ClO-)>c(OH-),故B错误;C.等物质的量的强碱与弱酸混合生成强碱弱酸盐溶液显碱性c(OH-)>c(H+),再根据溶液中电荷守恒可以判断c(Na+)>c(CH3COO-),故C错误;D.Na2CO3溶液中,钠离子浓度最大,因为碳酸根离子有一小部分水解生成碳酸氢根离子和氢氧根离子,显碱性,溶液中氢离子来源于水的电离,且电离程度较小,故离子浓度为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故D正确;故答案为D。
HClO+H++Cl-,HCl完全电离,而HClO部分电离,可知正确的顺序c(H+)>c(Cl-)>c(ClO-)>c(OH-),故B错误;C.等物质的量的强碱与弱酸混合生成强碱弱酸盐溶液显碱性c(OH-)>c(H+),再根据溶液中电荷守恒可以判断c(Na+)>c(CH3COO-),故C错误;D.Na2CO3溶液中,钠离子浓度最大,因为碳酸根离子有一小部分水解生成碳酸氢根离子和氢氧根离子,显碱性,溶液中氢离子来源于水的电离,且电离程度较小,故离子浓度为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故D正确;故答案为D。


科目:高中化学 来源: 题型:
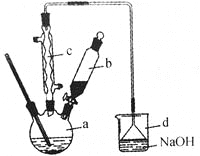
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g﹒cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须要做的是 (填入正确操作前的字母)
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为合理利用“垃圾”资源,提倡垃圾分类回收,生活中废弃的铁锅、铝制易拉罐等可以归为一类加以回收,它们属于
A. 有机物 B. 无机盐 C. 金属或合金 D. 难溶性碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应A(s)+3B(g) ![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置,能完成很多电化学实验。下列有关此装置的叙述中,错误的是( )

A. 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B. 若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流的阴极保护法
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处时,铁电极上的电极反应式为:Cu2++2e-===Cu
D. 若X为铜棒,Y为硫酸铜溶液,开关K置于N处时溶液中各离子浓度都不会发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定中和反应的反应热,计算时至少需要的数据是( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容④反应后溶液的质量
⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
A. ①②③⑥ B. ①③④⑥ C. ③④⑤⑥ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3个SO32-恰好将2个XO4-离子还原,SO32-被氧化为SO42-,则X元素在还原产物中的化合价是( )
A.+1 B.+2 C.+3 D. +4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.分离酒精和CCl4的混合物,可用分液法
B.从Na2CO3溶液中得到Na2CO3晶体,可用过滤法
C.从I2的CCl4溶液中得到CCl4 , 可用蒸馏法
D.分离NaCl和AgCl的混合物,可用萃取法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com