
����Ŀ����֪��Ӧ2X(g)+Y(g)![]() Z(g)��ij�о�С�齫4moX��2molY����һ�ݻ�������ܱ������У��ⶨ1min��X��ת���ʣ��õ������������ʾ�������ж���ȷ���ǣ� ��
Z(g)��ij�о�С�齫4moX��2molY����һ�ݻ�������ܱ������У��ⶨ1min��X��ת���ʣ��õ������������ʾ�������ж���ȷ���ǣ� ��
t/min | 2 | 4.5 | 5 | 6 |
X��ת���� | 30% | 40% | 70% | 70% |
A.���ŷ�Ӧ�Ľ��У����������ܶȲ�������
B.��Ӧ��5.5minʱ��v��(X)=v��(Z)
C.6minʱ��������ʣ��1.4 mol Y
D.����Ӧ�����У�������ѹǿ���ٸı䣬����˵���÷�Ӧ�Ѵﵽƽ��״̬
���𰸡�D
��������
A���÷�Ӧ�з�Ӧ����������Ϊ���壬����δƽ��ʱ����������������䣬�������ݣ����Ի��������ܶ�һֱ���䣬��A����
B�����ݱ������ݿ�֪5min��X��ת���ʲ��䣬˵����ʱ��Ӧ�Ѵﵽƽ�⣬���淴Ӧ������ȣ�v��(X)=v��(X)����v��(X)= 2v��(Z)������v��(X)= 2v��(Z)����B����
C��6minʱ��X��ת����Ϊ70%�����n(X)=4mol��70%=2.8mol�����ݷ���ʽ��֪��n(Y)=1.4mol������ʣ���YΪ2mol-1.4mol=0.6mol����C����
D���÷�Ӧǰ������ϵ��֮�Ͳ���ȣ�����δƽ��ʱ������������ʵ�����䣬����������䣬����ѹǿ��䣬ѹǿ����ʱ˵����Ӧƽ�⣬��D��ȷ��
�ʴ�ΪD��


 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. �����Ṳ���ĸ�ͬ���칹��(�������Ұ���������)
B. ��ͬ�����µķе㣺�Ҷ������Ҵ������飾����
C. CH3COOCH3�ں˴Ź��������������ֲ�ͬ���͵���ԭ��
D. ���ֲ�ͬ�İ����������۷�Ӧʱ�����ɲ�����4�ֵľۺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þ����һ�ֹ�ҵ���ϣ���Ҫ�ɷ���MgO(ռ40%)������CaO��MnO��Fe2O3��FeO��Al2O3��SiO2�����ʣ��Դ�Ϊԭ����ȡ������þ��������ӡȾ����ֽ��ҽҩ�ȹ�ҵ������þ������ȡMgSO4��7H2O������������

��������ش�����������
��1��ʵ��������1mo/L������800mL������18.4mol/L��Ũ���������ƣ���ȡŨ����ʱ����ʹ�õ���Ͳ�Ĺ��Ϊ____________
A.10mL B.20mL C.50mL D.100mL
��2�������NaClO����Mn2+��Ӧ��Mn2++ClO-+H2O=MnO2��+2H++Cl-������һ������Ҳ�ᱻNaClO�������÷�Ӧ�����ӷ���ʽΪ_________________��
��3����������Ҫ�ɷ��г�����Fe(OH)3��Al(OH)3���________________��
��4������������ǰ��������˲���Fe3+�Ƿ������������鷽����______________��
��5����֪MgSO4��CaSO4���ܽ�����±���
�¶�/�� | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
���������ǽ�MgSO4��CaSO4�����Һ�е�CaSO4��ȥ�������ϱ����ݣ���Ҫ˵������������ ���������ǽ���Һ��������Ũ������ȴ�ᾧ��__________����õ���MgSO4��7H2O��
��6��ʵ�����ṩ����þ�10g���õ���MgSO4��7H2OΪ17.22g����MgSO4��7H2O�IJ���Ϊ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ʈ����������ȼ��ʱ����������Ư���������С(ֱ��С��10-7m)�����׳���(��Ư����Сʱ��������)�����������SO2��O2�Ӵ�ʱ��SO2����ת��ΪSO3��ʹ��������������γ����ꡣ
(1)���й���SO2�������У���ȷ����_____��
A��SO2�ȿ�������������Ҳ��������ԭ�� B��SO2���Ǵ�����Ⱦ�� C��������SO2����Ҫ��Դ�������ų���β�� D��SO2����Ư���ԣ��������ʹʯ����Һ��ɫ
(2)���з�Ӧ�У�SO2�����˻�ԭ�Ե���_______��
A��SO2+H2OH2SO3 B��SO2+2NaOH=Na2CO3+H2O C��2SO2+O2![]() 2SO3 D��SO2+CaO=CaSO3
2SO3 D��SO2+CaO=CaSO3
(3)���ܼ��������̼�Ͷ���������Լ���________��
A��Ʒ����Һ B������ʯ��ˮ C����ˮ D�����Ը��������Һ
(4)��������Σ���������굼�µ�_______��
A����ɺ����ֺ� B����ʴ������ C��������� D��������ľ��ή
(5)����SO2ͨ�벻ͬ��Һ��ʵ���������ý��۲���ȷ����_______��
��Һ | ���� | ���� | |
A | ��HCl��BaCl2��FeCl3��Һ | ������ɫ���� | SO2�л�ԭ�� |
B | H2S��Һ | ������ɫ���� | SO2�������� |
C | ����KMnO4��Һ | ��ɫ��Һ��ɫ | SO2��Ư���� |
D | Na2SiO3��Һ | ������״���� | ���ԣ�H2SO3>H2SiO3 |
(6)�������������;���ɲ�ȡ���е���Щ��ʩ___________��
������ú��ȼ�� �ڰѹ����̴���� ��ȼ������ �ܷɻ��������Ƚ�ͨ���߲������ȼ�ϣ�����Ȼ���� �ݿ�������Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���Ӧ�ķ���ʽ����������
A. ������Һ�����ԣ�H2S ![]() 2H+��S2�C
2H+��S2�C
B. ��NO2������������ˮ�У���ɫ��dz��2NO2(g) (����ɫ) ![]() N2O4 (g) (��ɫ) ��H��0
N2O4 (g) (��ɫ) ��H��0
C. �����ȼ������H���C890.3 kJ��mol�C1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ�� CH4(g)��2O2(g)��CO2(g)+2H2O(l) ��H���C890.3 kJ��mol�C1
D. �����������Һ��ϡ�����ϳ��ֻ��ǣ�S2O32�C��2H+��S ��SO2 ��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ֽС���άͪ����Һ������άͪͨ�������HI3�γɾ�άͪ�⣬��ṹ��ʾ��ͼ��ʾ������˵����ȷ����
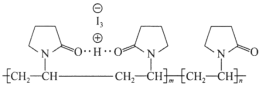 (ͼ�����߱�ʾ���)
(ͼ�����߱�ʾ���)
A.C��N��Oԭ�ӵĵ縺����������
B.��άͪ���к������Ӽ������ۼ�������Ȼ�ѧ��
C.��άͪ������ˮ��ԭ������ˮ���Ӽ��γ����
D.�����еĺ�N��Ԫ��һ����ƽ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�������ͼ��ʾװ����ȡ�϶���������������֪������ˮ�Ȼ��ƿ����Ҵ��γ�������ˮ��CaCl2��6C2H5OH��
���й��л���ķе㣺
�Լ� | ���� | �Ҵ� | ���� | �������� |
�е㣨�棩 | 34.7 | 78.5 | 118 | 77.1 |
����˵����ȷ����
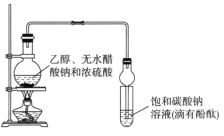
A.װ�������ιܼ��������������ܷ�ֹ����
B.��Ӧ��������Թ��е������ǣ���Һ�ֲ㣬�²���ɫ��״Һ�壻�ϲ���Һ��ɫ��dz
C.�Ӵ��Թ��з���������������л�����һ�������Ҵ������Ѻ�ˮ��Ӧ�ȼ�����ˮ�Ȼ��ƣ����˷�����Ҵ�
D.��������ˮ�����ƣ�Ȼ����������ռ�118�����ҵ���֣��Եõ��ϴ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����W��X��Y��Z���ֽ���������װ�ý���ʵ�顣����˵������ȷ���ǣ� ��
װ�� |
|
|
|
���� | ����W�����ܽ� | Y���������� | W����������� |
A.װ�ü���X��ԭ�������
B.װ������Y�缫�ϵķ�ӦʽΪCu2++2e=Cu
C.װ�ñ�����Һ��c(H+)����
D.���ֽ����Ļ��ǿ��˳��ΪZ��W��X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ե���Ϊ��Ҫԭ�Ϻϳ�һ�־��й���ζ������C�ͻ�����D�ĺϳ�·������ͼ��ʾ��
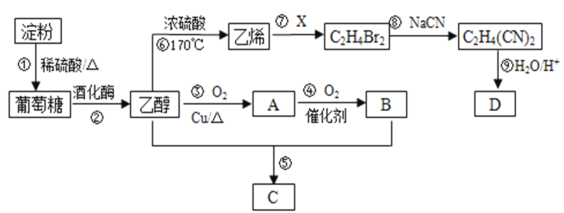
��ش��������⣺
(1)A�Ľṹ��ʽΪ________��B�����еĹ���������Ϊ________��
(2)��Ӧ�۵Ļ�ѧ����ʽΪ_______��
(3)��Ӧ�ݵĻ�ѧ����ʽΪ_________��
(4)��֪D����Է�����Ϊ118����������ֻ����һ�ֹ����ţ�����̼������Ԫ�ص����������ֱ�Ϊ40.68%��5.08%������Ϊ��Ԫ�أ���D�Ļ�ѧʽΪ______����ṹ��ʽΪ_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com