
【题目】中国人自古就有泡药酒的习惯。药酒多选用50-60度的白酒,将中药材浸泡在酒中,经过一段时间,中药材中的有效成分(主要是有机物)溶解在酒中,此时即可过滤去渣后饮用。泡药酒的原理属于

A.萃取B.结晶C.干燥D.置换
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确的是( )
①KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;1∶6
②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;2∶3
③SiO2+3C![]() SiC+2CO↑;1∶2
SiC+2CO↑;1∶2
④3NO2+H2O=2HNO3+NO;2∶1
A.①③B.②③
C.②④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一中重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示。请回答下列问题:
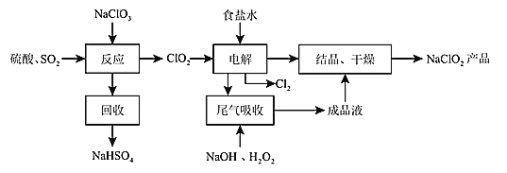
(1)NaClO2中Cl元素的化合价为_____________;
(2)写出“反应”步骤中生成ClO2的化学方程式________________________。
(3)“尾气吸收”步骤中发生的反应为2NaOH + H2O2 + 2ClO2 = 2NaClO2 + O2↑ + 2H2O ,其中氧化剂与还原剂的物质的量之比为_________;若有3 mol 电子发生转移,则有__________L(标准状况下)O2生成。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。则NaClO2的有效氯含量为_____(结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KNO3固体样品中含有少量的KCl、BaCl2杂质,为了提纯KNO3并分离得到BaCl2,进行如下实验操作:

(1)加入过量K2CO3所发生反应的离子方程式为_________________________________;
(2)结合下图各物质的溶解度曲线可知操作③的名称是_________________;

(3)有人认为操作③之前无需加入过量的酸b,也能得到纯净的固体1,你认为该观点是否正确?并做出解释______________________________________。
(4)用制得的 KNO3固体配制 200 mL0.2mol/L KNO3 溶液。
①本实验用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、量筒、还有_______________;
②下列情况会使所配制的KNO3 溶液的浓度偏高的是______________(填字母)。
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水
C.定容时仰视刻度线 D.定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,对可逆反应A+3B![]() 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断错误的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断错误的是
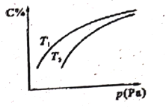
A.若正反应方向Q<0,则T1>T2
B.A可能为气体
C.压强增大时,混合气体的平均相对分子质量增大
D.B不一定为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3COOH是中学化学中常用的一元弱酸,请回答下列问题:
(1)设计简单实验证明CH3COOH为弱酸__。
(2)向0.1mol/L CH3COOH溶液中加蒸馏水稀释至100mL,在稀释过程中,下列量的变化是(“增大”、“减小”、“不变”或“不能确定”):
n(H+)=___,![]() =___,
=___,![]() =__,c(OH-)=___。
=__,c(OH-)=___。
(3)OH-浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是__(填写序号)
①反应需要的时间:CH3COOH>HCl
②开始反应的速率:HCl>CH3COOH
③参加反应的锌粉的物质的量:CH3COOH=HCl
④反应过程的平均速率:CH3COOH>HCl
⑤盐酸中有锌粉剩余
⑥CH3COOH溶液中有锌粉剩余
(4)向饱和食盐水中滴加一定浓度的盐酸,对出现现象的预测可能正确的是__。
A.白色沉淀 B.液体分层 C.无明显现象 D.黄绿色气体
(5)现有下列溶液:①纯水;②pH=10的NaOH溶液;③pH=3的醋酸溶液;④pH=10的CH3COONa溶液。试比较四种溶液中水的电离程度的大小关系__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酯的合成路线如下图所示
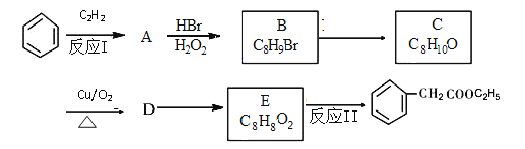
(1)反应Ⅰ反应类型为___________________; D中含氧官能团为_____________写名称)。
(2)反应Ⅱ的反应条件为:_________________。
(3)C→D的化学反应方程式为________________________________________。
(4)写出一种满足下列条件的E的同分异构体的结构简式为__________________________。
①能发生银镜反应 ②含苯环且苯环上一溴代物两种 ③不能与钠反应
(5)写出B合成![]() 的合成路线。合成路线常用的表示方式为:_______________
的合成路线。合成路线常用的表示方式为:_______________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水系钠离子电池安全性能好、价格低廉、对环境友好,有着巨大的市场前景。某钠离子电池工作原理如图,电池总反应为:2NaFePO4F + Na3Ti2(PO4)3![]() 2Na2FePO4F+ NaTi2(PO4)3
2Na2FePO4F+ NaTi2(PO4)3
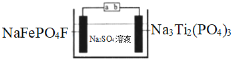
下列说法错误的是
A.充电时,a接电源正极
B.放电时,溶液中的Na+在NaFePO4F电极上得电子被还原
C.充电时,阴极上的电极反应为NaTi2(PO4)3+2Na++2e﹣=Na3Ti2(PO4)3
D.理论上,该电池在充电或放电过程中溶液中的c(Na+)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)Fe2(SO4)3(写出电离方程式)_____
(2)铝和氢氧化钠溶液混合(写出反应的离子方程式)_____
(3)2H++CO32﹣═H2O+CO2↑(改写成化学方程式)________
(4)除去NaHCO3溶液中混有少量 Na2CO3溶液的离子反应方程式_____.
Ⅱ.有一瓶溶液只含Cl﹣、CO32﹣、SO42﹣、Na+、Mg2+、Cu2+六种离子中的某几种通过实验:
①原溶液![]() 白色沉淀;
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解.
(1)试分析原溶液中一定含有的离子是_____,一定不含有的离子是_____,
(2)有的同学认为实验③可以省略,你认为是否正确_____(填是或否),理由是_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com