
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A. 常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
B. 4.0g由H218O与D2O组成的混合物中所含中子数为2NA
C. 标准状况下,11.2LHF含有0.5NA个HF分子
D. 电解精炼铜时转移了NA个电子,阳极溶解32g铜
【答案】B
【解析】
A.常温下,铝片投入足量的浓硫酸中,铝发生钝化,铝失去的电子数小于0.3NA,故A错误;
B.H218O与D2O的摩尔质量均为20g/mol,则4.0g由H218O与D2O组成的混合物的物质的量为:![]() =0.2mol,一个H218O分子含有10个中子,一个D2O分子也含有10个中子,所以0.2mol混合物含有中子为:0.2mol×10=2mol,即所含中子数为2NA,故B正确;
=0.2mol,一个H218O分子含有10个中子,一个D2O分子也含有10个中子,所以0.2mol混合物含有中子为:0.2mol×10=2mol,即所含中子数为2NA,故B正确;
C.标准状况下氟化氢不是气体,11.2L HF不是0.5mol,故C错误;
D.粗铜中含有锌、铁、银等杂质,锌、铁先失电子,反应完成后,铜再失电子,所以电解精炼铜时转移了NA个电子, 阳极溶解铜小于32 g,故D错误;
本题答案为B。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】(1)下列物质①H2O,②CuO,③CuSO4,④NaOH,⑤氨水,其中属于氧化物的是__________,(请填序号,下同)属于盐的是__________,属于混合物的是__________,属于电解质的是__________。
(2)在氮的化合物中,红棕色、有刺激性气味的有毒气体是__________,(填写化学式)
(3)根据反应 MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,回答下列问题:还原剂是__________,还原产物是__________,氧化剂是__________,氧化产物是__________。
MnCl2+Cl2↑+2H2O,回答下列问题:还原剂是__________,还原产物是__________,氧化剂是__________,氧化产物是__________。
(4)纯净的H2在Cl2中燃烧发出__________色火焰。
(5)金属钠切开后,光亮的金属断面__________,说明常温下钠能够跟__________反应,生成__________;钠投入水中,钠__________水面上,并四处游动,发出响声,这说明__________,熔成一个闪亮的小球,最后向烧杯中滴加酚酞,溶液__________。
(6)配平:①_____HNO3(稀)+____Cu=_____Cu(NO3)2+____H2O+ NO↑
②___H2SO4(浓)+_____C![]() _____CO2↑+_____SO2↑+_____H20
_____CO2↑+_____SO2↑+_____H20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素 R 的最高价氧化物的水化物分子式是 HnRO2n﹣2,则在气态氢化物中 R 元素的化合价是( )
A.3n﹣10B.12﹣3nC.3n﹣4D.3n﹣12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N键断裂的同时,有3个H﹣H键断裂
②一个N≡N键断裂的同时,有6个N﹣H键断裂
③其他条件不变时,混合气体平均相对分子质量不再改变
④恒温恒容时,体系压强不再改变
⑤NH3、N2、H2的体积分数都不再改变
⑥恒温恒容时,混合气体密度保持不变
⑦正反应速率v(H2)=0.6molL﹣1min﹣1,逆反应速率v(NH3)=0.4molL﹣1min﹣1
A. 全部 B. ②③④⑤ C. ②③④⑤⑦ D. ③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图是研究二氧化硫性质的微型实验装置(实验时用另一表面皿扣在上面)。现用75%硫酸溶液和亚硫酸钠晶体反应制取SO2气体并进行实验,实验现象很明显。下列说法中错误的是

A.品红溶液褪色
B.紫色石蕊溶液先变红后褪色
C.酸性KMnO4溶液紫色褪去
D.含酚酞的NaOH溶液红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同位素在化学研究方面有重要用途,化学家利用18O成功研究了某化学反应的历程。下列关于18O与16O的叙述错误的是
A.18O 与16O 的物理性质相同
B.18O 与 16O的化学性质相同
C.18O 与 16O的质子数相同
D.18O与 16O的中子数不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,下列溶液的pH或微粒的物质的量浓度关系错误的是
A. 某溶液中由水电离出的c(H+)=1×10-amol·L-1,若a>7时,该溶液pH一定为14-a
B. 0.1mol·L-1的KHA溶液,其pH=10,c(K+)>c(HA-)>c(OH-)>c(A2-)
C. 将0.2mol·L-1的某一元酸HA溶液和0.1mol·L-1NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(HA)>c(Na+)>c(A-)
D. 等体积、等物质的量浓度的Na2CO3溶液与 NaHCO3溶液混合:2c(Na+)=3c(CO32-)+3c( HCO3-)+3c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双极膜电渗析一步法盐制酸碱的技术进入到了工业化阶段,某科研小组研究采用BMED膜堆(如图所示),模拟以精制浓海水为原料直接制备酸和碱。BMED膜堆包括阳离子交换膜、阴离子交换膜和双极膜(A、D)已知:在直流电源的作用下,双极膜内中间界面层发生水的解离,生成H+和OH-。下列说法不正确的是
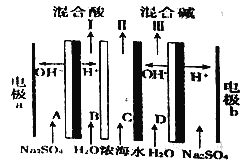
A. 电极b连接电源的负极 B. Ⅱ口排出的是淡水
C. 电解质溶液采用Na2SO4溶液可避免有害气体的产生 D. C为阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知甲烷的热值为56kJ/g ,写出甲烷完全燃烧生成稳定的物质的热化学方程式:______________________________
(2)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为______________________;x为____________。
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为______________________;x为____________。
(3)下列说法中可以充分说明反应: P(g)+2Q(g)![]() 2R(g)+S(s),在恒温恒容下已达平衡状态的是 (__________)
2R(g)+S(s),在恒温恒容下已达平衡状态的是 (__________)
A.P和R的生成速率相等
B.反应容器内总的物质的量保持不变
C.反应容器中的压强不随时间的变化而变化
D.反应容器内P、Q、R、S四者共存
E. 反应器中摩尔质量保持不变
(4)如图为某种甲烷燃料电池示意图,工作时电子流向如图所示。

电极B的名称___________,发生_________反应。写出电极A的电极反应式:__________,电极A附近pH如何变化?_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com