
【题目】将等质量混合的铜、锌和铁三种金属组成的混合物Wg加入到FeCl3和盐酸组合的混合液中,充分反应后,则下列说法正确的是
A. 若无固体剩余,则溶液中一定有的金属离子是Fe3+
B. 若无固体剩余,不可能有的离子是H+、Fe2+、Cu2+
C. 若剩余固体![]() g,则溶液中一定没有Fe3+、一定有H+
g,则溶液中一定没有Fe3+、一定有H+
D. 若剩余固体![]() g,则溶液中一定有Fe2+、Zn2+
g,则溶液中一定有Fe2+、Zn2+
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3![]() H++ H2PO3-。亚磷酸与足量NaOH溶液反应,生成Na2HPO3。
H++ H2PO3-。亚磷酸与足量NaOH溶液反应,生成Na2HPO3。
(1)写出亚磷酸与少量NaOH溶液反应的离子方程式:____________________。
(2)某温度下,0.100 0 mol·L-1的H3PO3溶液pH的读数为1.6,即此时溶液中c(H+)=2.5×10-2mol·L-1,除OH-之外其他离子的浓度由大到小的顺序是______________________,该温度下H3PO3电离平衡的平衡常数K=________。(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(3)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中c(Na+)________c(H2PO3-)+2c(HPO32-)(填“>”“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl﹣的物质的量最多的是( )
A.200mL 2mol/L MgCl2溶液
B.150mL 5mol/L KClO3溶液
C.标准状况下,13.44L的HCl气体
D.29.25gNaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2 . 某同学在实验室中对NH3与NOx反应进行了探究:收集足量NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度下按图示装置进行实验. 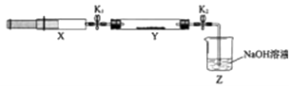
操作步骤 | 实验现象 | 解释原因 |
打开K1 , 推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中 | ②反应的化学方程式 |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③ | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述中不正确的是( )
A. 传统陶瓷经高温烧结而成,其强度很高,抗摔能力很强
B. 钢化玻璃比普通玻璃有更高的强度,常用于制造汽车或火车的车窗
C. 目前中、美、日等国家掌握的陶瓷发动机技术,使热效率大幅度提高
D. 石英玻璃制成的光导纤维是一种新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氨的喷泉实验形成的原理解释正确的是
A. 氨水呈碱性 B. 氨气极易溶于水,烧瓶内外形成压强差
C. 氨气易液化 D. 氨气溶于水后形成的溶液易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中不属于氧化还原反应的是( )
A.3CuS+8HNO3=3Cu(NO3)2+2NO↑+3S↓+4H2O
B.3Cl2+6KOH=5KCl+KClO3+3H2O
C.3CCl4+K2Cr2O7=2CrO2C12+3COCl2+2KCl
D.2KMnO4 ![]() ?K2MnO4+MnO2+O2↑
?K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2LNaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,回答下列问题: 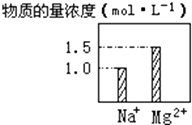
(1)该混合溶液中,Na+的物质的量为mol,MgCl2的物质的量为mol,Cl﹣的物质的量为mol.
(2)该混合溶液中含溶质的总质量为g.
(3)将该混合溶液加水稀释至体积为 1L,稀释后溶液中Cl﹣的物质的量浓度为molL﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com