
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:
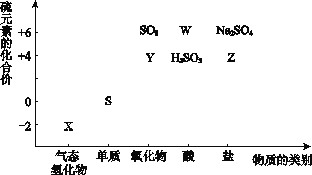
(1)Y的化学式为_________,检验Y所用的试剂是________________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为__________________。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是_______(填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4d.SO2 + Na2SO4
(4)将X与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为__________。
【答案】SO2 品红溶液 Cu + 2H2SO4(浓)![]() CuSO4+ 2H2O + SO2↑ b 1∶2
CuSO4+ 2H2O + SO2↑ b 1∶2
【解析】
(1)根据+6价的形式,Y应是+4价的氧化物,即SO2,因为SO2能使品红溶液褪色,因此检验SO2时,常用品红溶液;
(2)W是H2SO4,浓硫酸具有强氧化性,与铜发生反应,Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(3)Na2S2O3中S的价态为+2价,根据氧化还原反应中不同价态的同种元素参加氧化还原反应,向中间价态靠拢,
a、S的价态分别是-2、0,不符合,故错误;
b、S的价态分别是+4价、0价,符合题目,故正确;
c、S的价态分别显+4价、+6价,不符合,故错误;
d、S的价态+4价、+6价,不符合,故错误;
(4)X为H2S,两者发生氧化还原反应,2H2S+SO2=3S+2H2O,因此氧化剂和还原剂的物质的量比值为1:2。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】经检测,某工业废水显酸性,且废水中含有大量Na+、Cu2+、Cl-、SO42-、NO3-,
(1)下列离子中,不可能大量存在于该废水中的是___(填序号)。
A.K+ B.Fe3+ C.Ag+ D.HCO3-
(2)若向上述废水中加入大量的过氧化钠固体,观察到的现象为___;相关的离子方程式为___。
(3)若工业废水中只含有H+和Na+、Cu2+、Cl-、SO42-、NO3-,经分析测得,H+、Cu2+、Cl-、SO42-、NO3-的物质的量浓度分别为:0.1mol·L-1、0.05mol·L-1、0.2mol·L-1、0.1mol·L-1、0.1mol·L-1,则Na+的物质的量浓度为___。
(4)设计实验方案除去原废水中的Cu2+和SO42-(用流程图表示)(提示:加入的试剂要过量)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A~D均含同种元素,都是中学化学中常见的物质,它们之间可发生如图所示的反应(除A~D外的其他物质均已略去)。
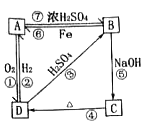
(1)写出相应物质的类别。
物质 | B | C | D |
类别 | ___ | __ | __ |
(2)上述反应①到⑥中,属于离子反应的有___个。
(3)①D→A转化的化学方程式:__。
②B→C转化的离子方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
Ⅰ.工业生产纯碱的工艺流程示意图如图:
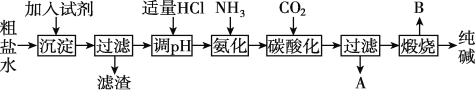
(1)为除去粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入试剂顺序合理的是____。
A.碳酸钠、氢氧化钠、氯化钡
B.碳酸钠、氯化钡、氢氧化钠
C.氢氧化钠、碳酸钠、氯化钡
D.氯化钡、氢氧化钠、碳酸钠
(2)工业生产纯碱工艺流程中,碳酸化时产生的现象是____;碳酸化时没有析出碳酸钠晶体,其原因是____。
(3)碳酸化后过滤,滤液A最主要的成分是____(填写化学式),检验这一成分的阴离子的具体方法是____。
(4)煅烧制取Na2CO3在____(填字母序号)中进行。
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.氧化铝坩埚
Ⅱ.纯碱在生产生活中有广泛的用途。
(5)工业上,可用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是

A. Cl2和苛性钾溶液在不同温度下可能发生不同反应
B. 反应中转移电子数为是0.21 NA
C. 原苛性钾溶液中KOH的物质的量无法确定
D. 生成物中Cl- 的物质的量为 0.21 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al混合物投入400mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
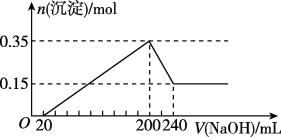
(1)原混合物中Mg和Al的质量之比为____。
(2)生成的H2在标准状况下的体积为____。
(3)加入NaOH溶液的物质的量浓度为____。
(4)稀硫酸的物质的量浓度为____。
(5)写出NaOH体积在200-240mL之间所发生的离子反应方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对三联苯是一种有机合成中间体,工业上合成对三联苯的化学方程式为![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 上述反应属于取代反应
B. 对三联苯分子中至少有16个原子共平面
C. 对三联苯的一氯取代物有4种
D. 0.2 mol对三联苯在足量的氧气中完全燃烧消耗5.1 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。如图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
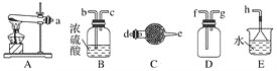
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接__、___接__,__接h;实验室用A装置制取NH3的化学方程式为___。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是___,试写出制纳米级碳酸钙的化学方程式:___。
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度、压强下,向密闭容器中投入一定量N2和H2,发生反应:N2+3H2![]() 2NH3 △H<0。
2NH3 △H<0。
(1)反应开始阶段,v(正)______(填“>”“<”或“=”)v(逆),随后v(正)逐渐______ (填“增大”或“减小”,下同),v(逆)逐渐______,反应达到平衡时,v(正)______ (填“>”“<”或“=”)v(逆)。
(2)达到平衡后,若正反应速率用v(N2)表示,逆反应速率用v’(H2)表示,则v(N2)=____v’(H2)。
(3)下列措施中能加快反应速率并提高氢气的转化率的是______(填字母)。
A.其他条件不变时,压缩容器体积 B.其他条件不变时,升高反应体系温度
C.使用合适的催化剂 D.保持容器体积不变,充入一定量的氮气
(4)实际生产中往往需要将温度控制在一个合适的范围,分析温度不宜过高也不宜过低的原因是______________________________________。
(5)写出合成氨反应N2+3H2![]() 2NH3的平衡常数表达式:____________________,升高温度时K值______(填“增大”“减小”或“不变”)。
2NH3的平衡常数表达式:____________________,升高温度时K值______(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com